
中枢神经系统(CNS)疾病的诊断长期以来面临着生物标志物匮乏的困境,尤其在多发性硬化症(MS)中,现有标志物如寡克隆带(OCB)和κ游离轻链(kFLC)在OCB阴性患者中敏感性和特异性仍存在不足,存在较高的误诊和漏诊问题。脑脊液(CSF)作为直接反映中枢神经系统病理状态的重要体液,在神经系统疾病的诊断中具有核心地位。
2026年2月25日,德国马克斯·普朗克生物化学研究所Matthias Mann团队在《Cell》(IF=42.5)发表了题为“Large-scale proteomics across neurological disorders uncovers biomarker panel and targets in multiple sclerosis.”的最新成果,通过高通量质谱技术对5045例脑脊液样本进行蛋白质组学检测,系统解析了多种神经系统疾病的蛋白质谱差异,发现并验证了一个22蛋白组合用于多发性硬化症(MS)的精准诊断,在OCB阴性患者中表现优异,并通过绝对定量质谱法打通了其临床转化链路。

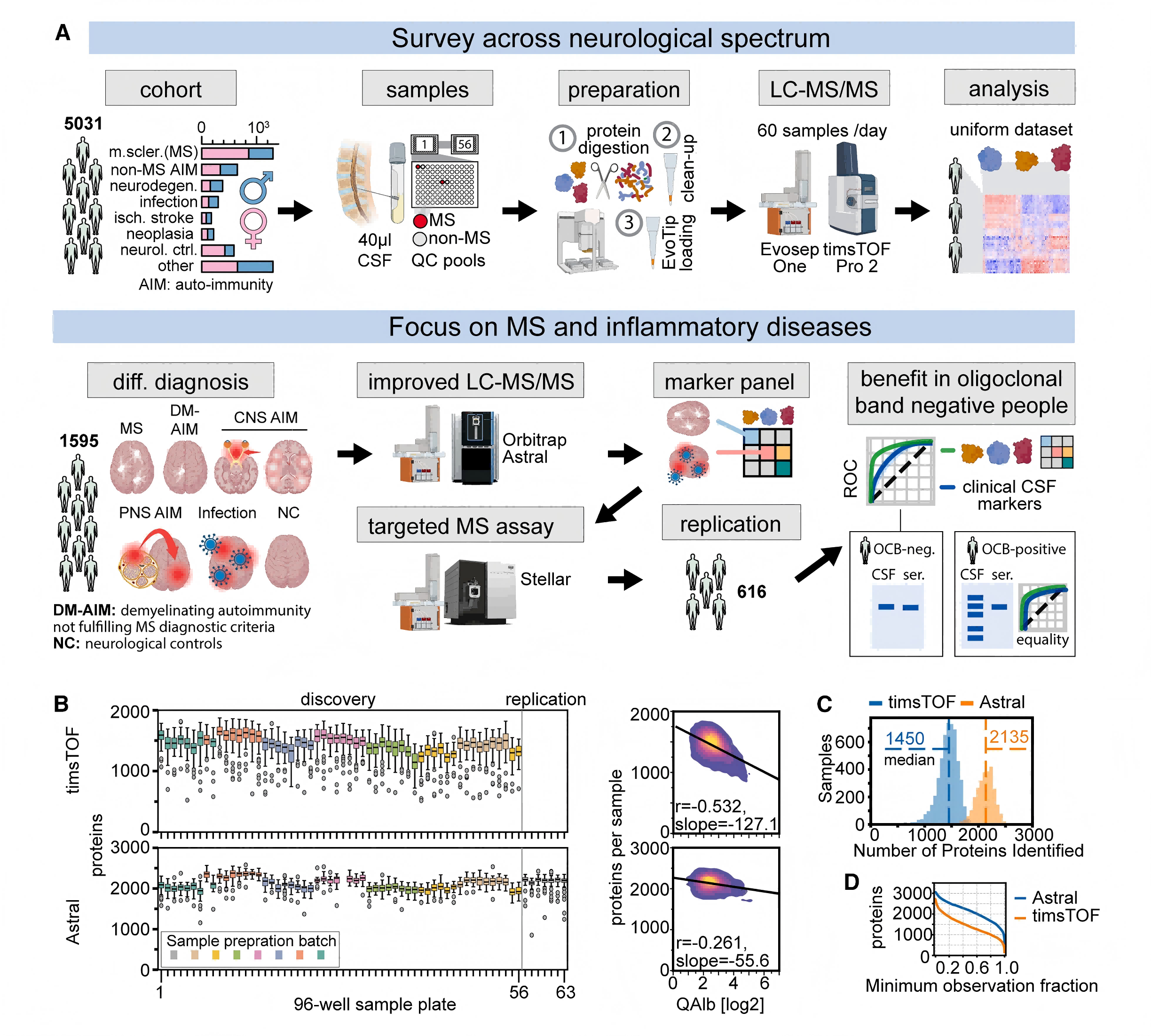
图1 研究设计和蛋白质组学数据集特征
研究样本
1. 队列设计:
| 队列类型 | 样本量 (例) | 检测平台 | 采集方式 | 鉴定深度 (蛋白/样本) | 核心用途 |
| 全局发现队列 | 5045 | timsTOF Pro2 | DIA | ~1,500 | 神经系统疾病全景图谱构建 |
| 深度发现子集 | 1595 | Orbitrap Astral | DIA | ~2,100 | 多发性硬化症标志物筛选 |
| 靶向验证队列 | 616 | Stellar | PRM | 22 | 独立样本验证标志物诊断性能 |
2. 样本分布
1)全局发现队列
来自不同神经系统疾病患者的5045例脑脊液样本,包含:
| 疾病 | 例数 |
| 多发性硬化症(MS) | 1343例 |
| 其他自身免疫性疾病(AIM) | 641例 |
| 神经退行性疾病 | 391例 |
| 感染性疾病 | 300例 |
| 肿瘤 | 241例 |
| 脑卒中 | 178例 |
| 神经系统对照 | 599例 |
| 其他中枢神经系统疾病 | 1352例 |
2)深度发现子集
来自不同神经系统疾病患者的1595例脑脊液样本,包含:
| 疾病 | 例数 |
| 多发性硬化症(MS) | 755例 |
| 其他自身免疫性疾病(AIM) | 373例 |
| 感染性疾病 | 195例 |
| 神经系统对照 | 272例 |
3)靶向验证队列
来自不同神经系统疾病患者的616例脑脊液样本,包含:
| 疾病 | 例数 |
| 多发性硬化症(MS) | 220例 |
| 其他自身免疫性疾病(AIM) | 204例 |
| 感染性疾病 | 37例 |
| 神经系统对照 | 155例 |
研究亮点速递
1. 规模制胜:纳入5000+例多种神经系统疾病脑脊液样本,成功构建全球最大脑脊液蛋白质组学图谱。
2. 范式革新:DIA无偏发现+PRM靶向验证+临床质谱绝对定量,展示质谱从科研到临床的完整路径。
3. 精准打击:攻克临床难题,22蛋白标志物组合破解寡克隆带(OCB)阴性多发性硬化症诊断困境。
4. 未卜先知:提出基于蛋白质组的“伪时间”多发性硬化症进展模型,预测未来3~15年的疾病轨迹。
研究结果
1.血脑脊液屏障(BCB)损伤主导脑脊液蛋白质组变异
为解析脑脊液蛋白质组的变异来源与疾病特征,通过多元线性回归与XGBoost机器学习模型构建,发现血脑脊液屏障(BCB)损伤是蛋白质组变异的首要因素,其解释的变异度约为疾病诊断的3倍,且BCB损伤随年龄增加而加重。在疾病研究中,该混杂因素需通过白蛋白比值(QAlb)校正。
校正后,疾病特征得以凸显:疾病相关扰动在关联疾病间高度相关,反映共享的炎症与细胞损伤机制。其中,多发性硬化症及其他自身免疫病以适应性免疫(免疫球蛋白)富集为特征。尽管多发性硬化症以免疫球蛋白G重链恒定区强烈上调为标志,但其与其他炎症性疾病的鉴别仍是最大挑战,XGBoost算法构建的多分类预测模型显示多发性硬化症与其他自身免疫疾病的鉴别最具挑战性(MS vs DM-AIM的ROC-AUC仅0.76)。SHAP富集分析显示适应性免疫能够预测多发性硬化症,这与多发性硬化症的自身免疫病理机制一致。这凸显了开发多蛋白组合标志物的必要性。
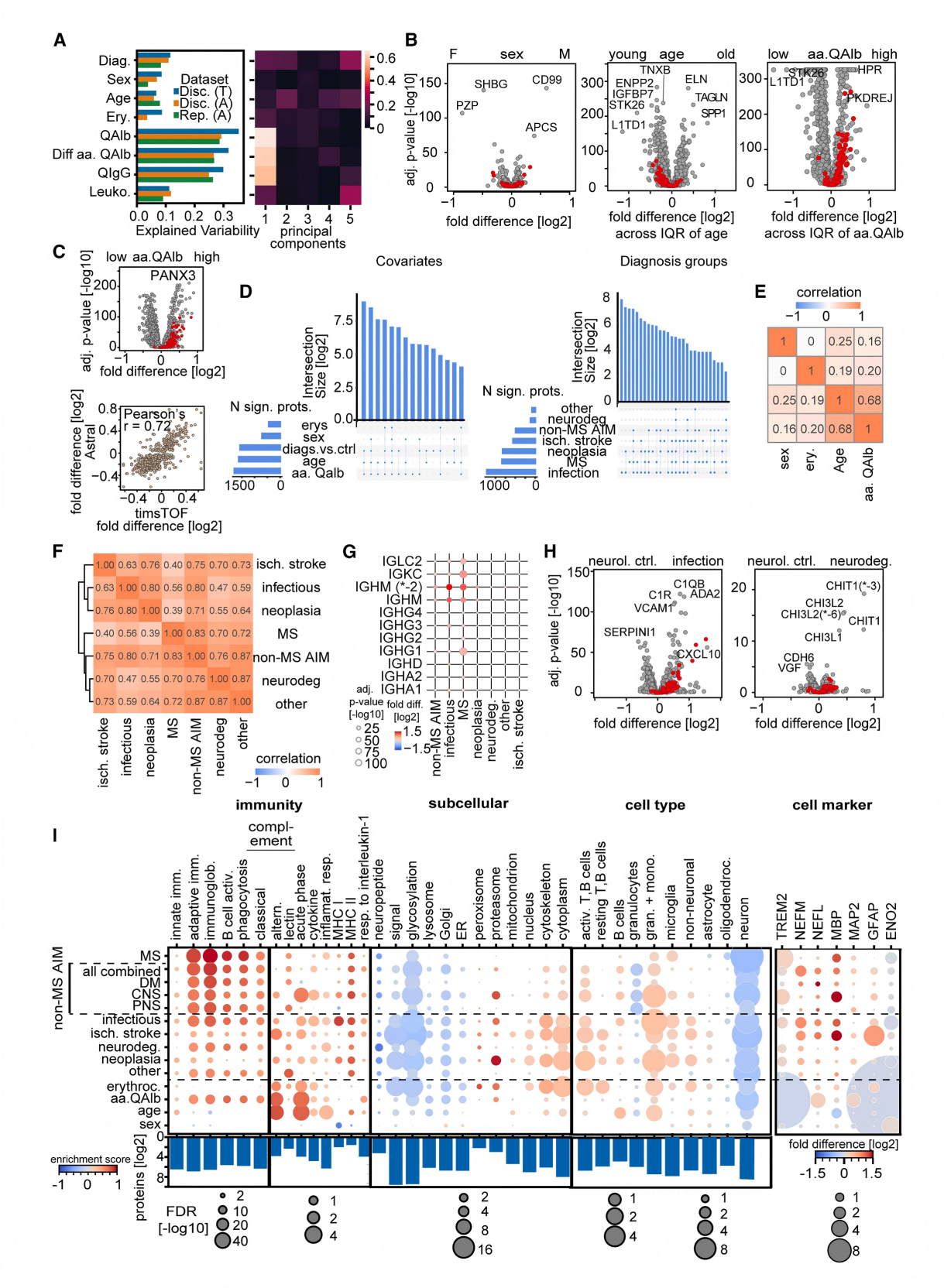
图2 诊断和协变量对脑脊液蛋白质组的影响
2.质谱法精准识别多发性硬化症相关蛋白,准确性得亲和力平台验证
在多发性硬化症与所有其他神经系统疾病的比较中,仅77个蛋白显著差异表达,其中近3/4为免疫球蛋白。非免疫球蛋白的新发现包括具有治疗靶点潜力的蛋白,如RYR2(兰尼碱受体2)和CSF1R(集落刺激因子1受体)抑制剂已在其他疾病中获批或处于临床试验阶段。与Olink数据的比较显示,质谱平台具有媲美免疫检测的定量一致性,重叠蛋白的组间变化倍数相关性良好(Pearson r=0.73),同时具备远超免疫检测的覆盖广度,在CSF蛋白检测方面具有竞争力。
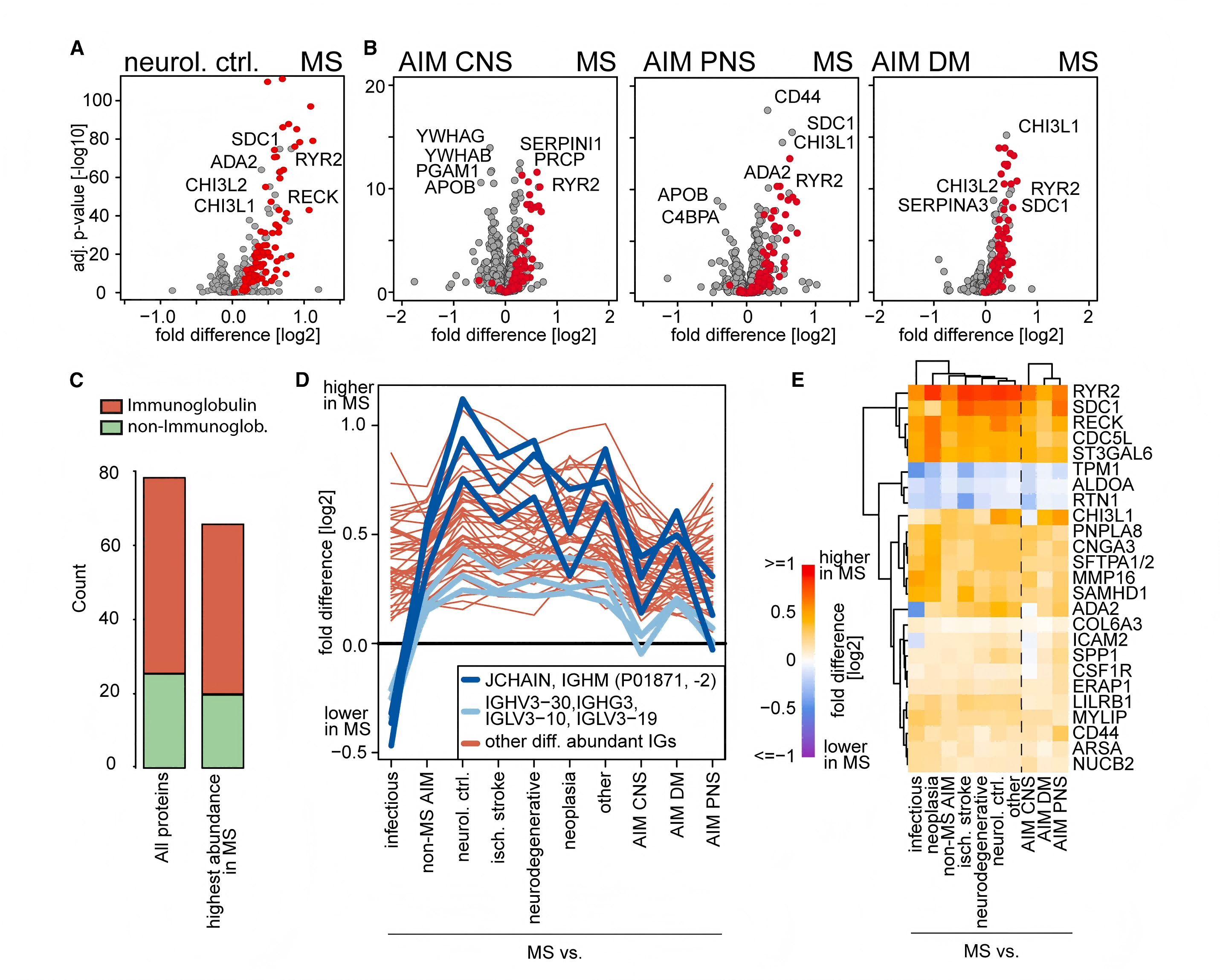
图3 多发性硬化症相关的脑脊液蛋白质组改变
3.基于蛋白质组的“伪时间”模型捕捉多发性硬化症发病的分子连续谱
为量化多发性硬化症的严重程度,该研究创新性地引入"伪时间"概念,通过SHAP值总和计算每个样本的伪时间位置,成功捕捉了从神经对照到多发性硬化症的分子连续谱,伪时间与年龄相关多发性硬化症严重程度评分(ARMSS)显著相关(Pearson r=0.18-0.28, p<0.0001)。重要的是,伪时间不因年龄、性别、红细胞污染、蛋白鉴定深度、BCB损伤指标(QAlb)等混杂因素而偏倚。这一基于蛋白质组的分期系统为多发性硬化症的精准分层提供了新工具,特别适用于横断面队列的预后评估。
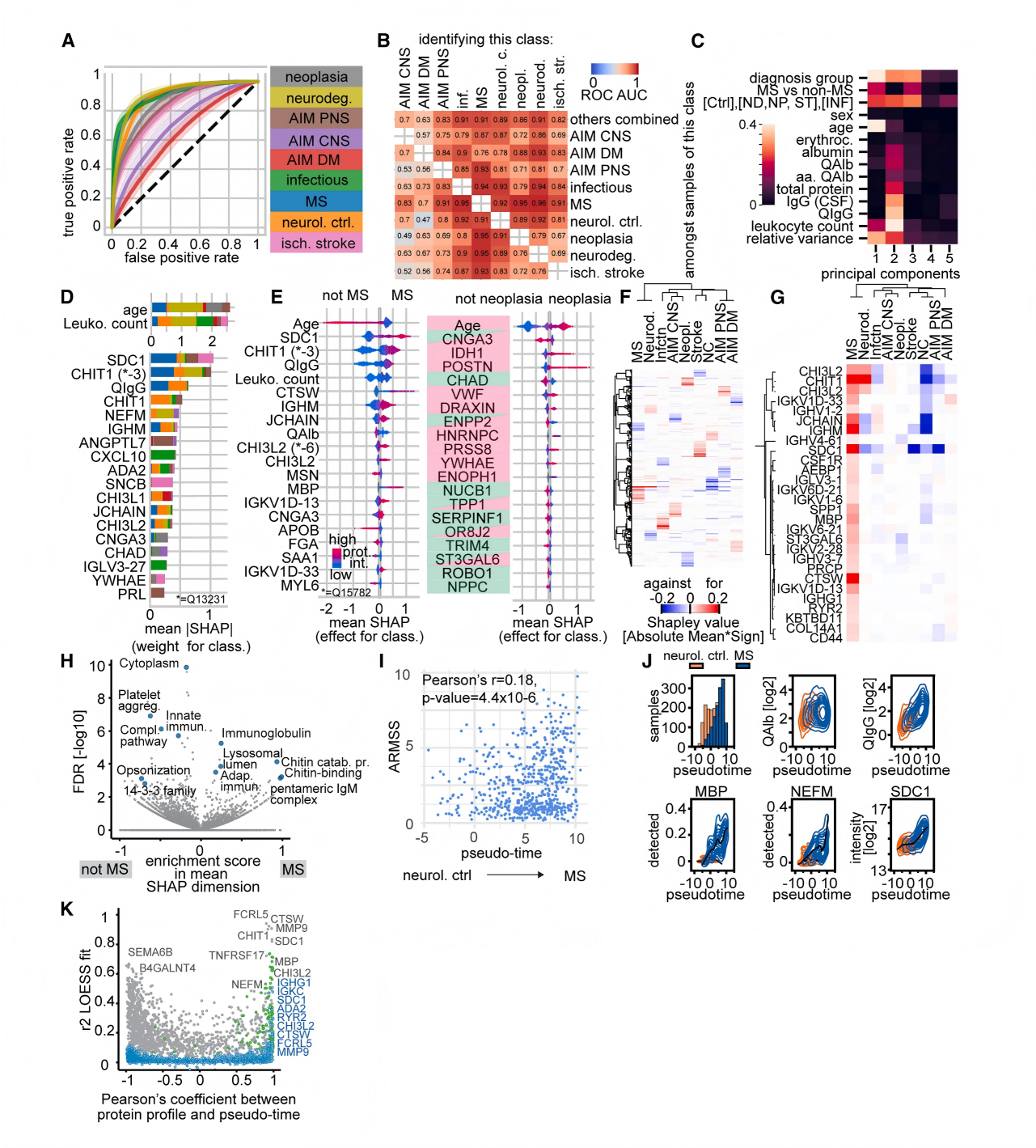
图4 多发性硬化症与神经系统对照的多类疾病预测和伪时间分析调查
4.多发性硬化症组合蛋白标志物解决OCB阴性多发性硬化症诊断难题
为鉴别多发性硬化症与其他炎症性中枢神经系统疾病,特别解决OCB阴性多发性硬化症的诊断难题,从发现队列中选择约1600例的分层子集使用Orbitrap Astral平台重新测量,以获得更高深度的蛋白质组数据(>2000蛋白/样本),使用XGBoost构建分类模型与临床参考模型进行头对头比较,并在独立的616例验证队列中进行验证。研究发现,30蛋白组合标志物模型(最终精简为22蛋白)在所有OCB状态下均与参考模型相当或更优,特别是在OCB阴性多发性硬化症的鉴别中。
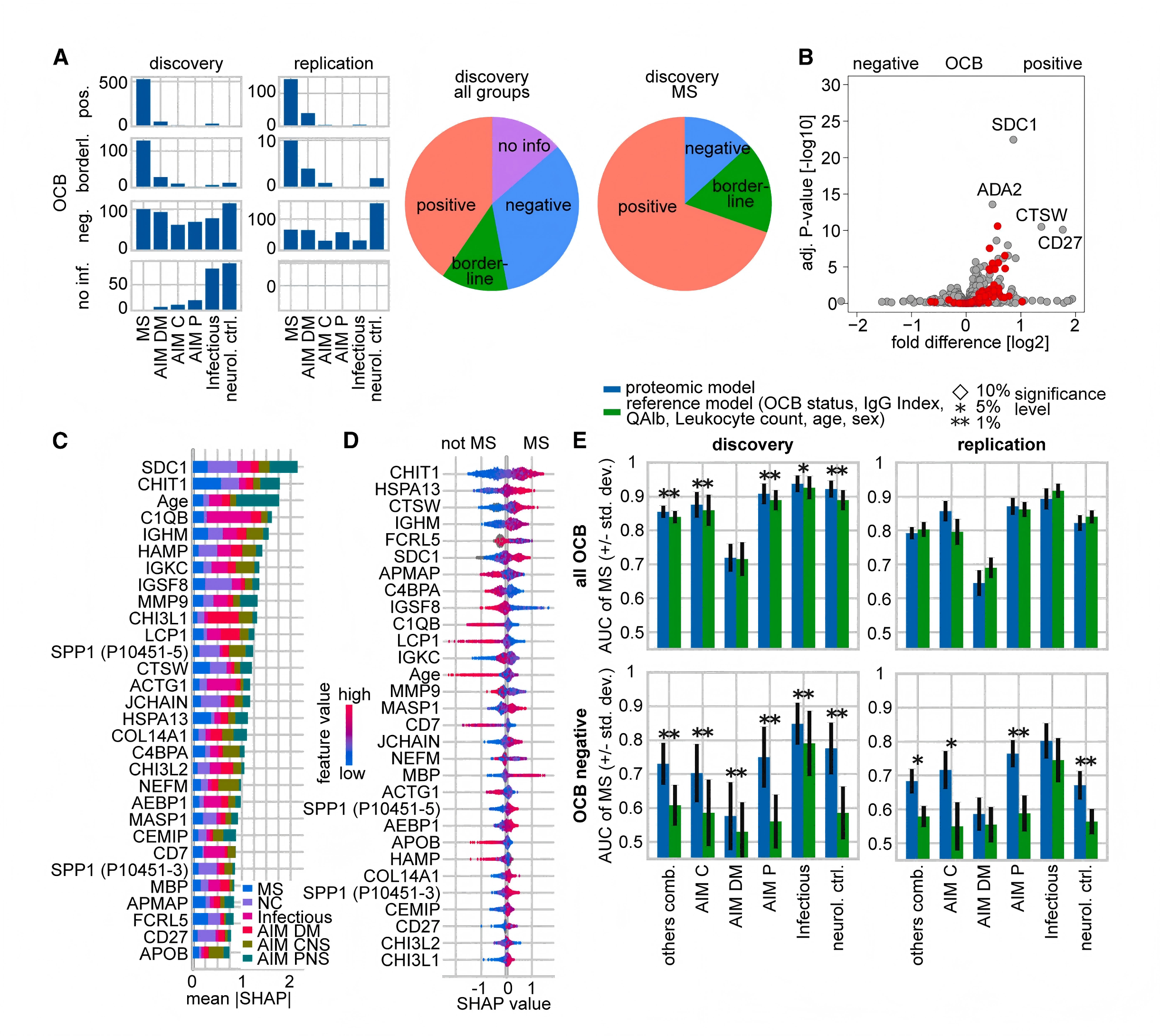
图5 蛋白质组学区分寡克隆带(OCB)阳性和阴性多发性硬化症与中枢神经系统炎症
5.临床应用级靶向检测方法开发,打通临床转化的“最后一公里”
为实现临床转化,在Stellar质谱仪上建立靶向平行反应监测(PRM)检测方法,针对22个标志物蛋白的22个肽段合成重同位素标记(¹³C/¹⁵N)肽段作为内标以实现绝对定量,成功建立了临床兼容的靶向质谱检测方法,定量结果与发现阶段DIA数据高度一致(Pearson r=0.77-0.96),分类性能与发现阶段相当,在OCB阴性多发性硬化症中保持对临床参考模型的优势(ROC-AUC提升0.02-0.1)。由于采用多蛋白组合和内标归一化,CSF上样量减少30%或60%不影响分类性能。这一靶向方法为临床实验室采用质谱技术进行MS诊断检测奠定了基础,展示了蛋白质组学生物标志物临床转化的可行性路径。
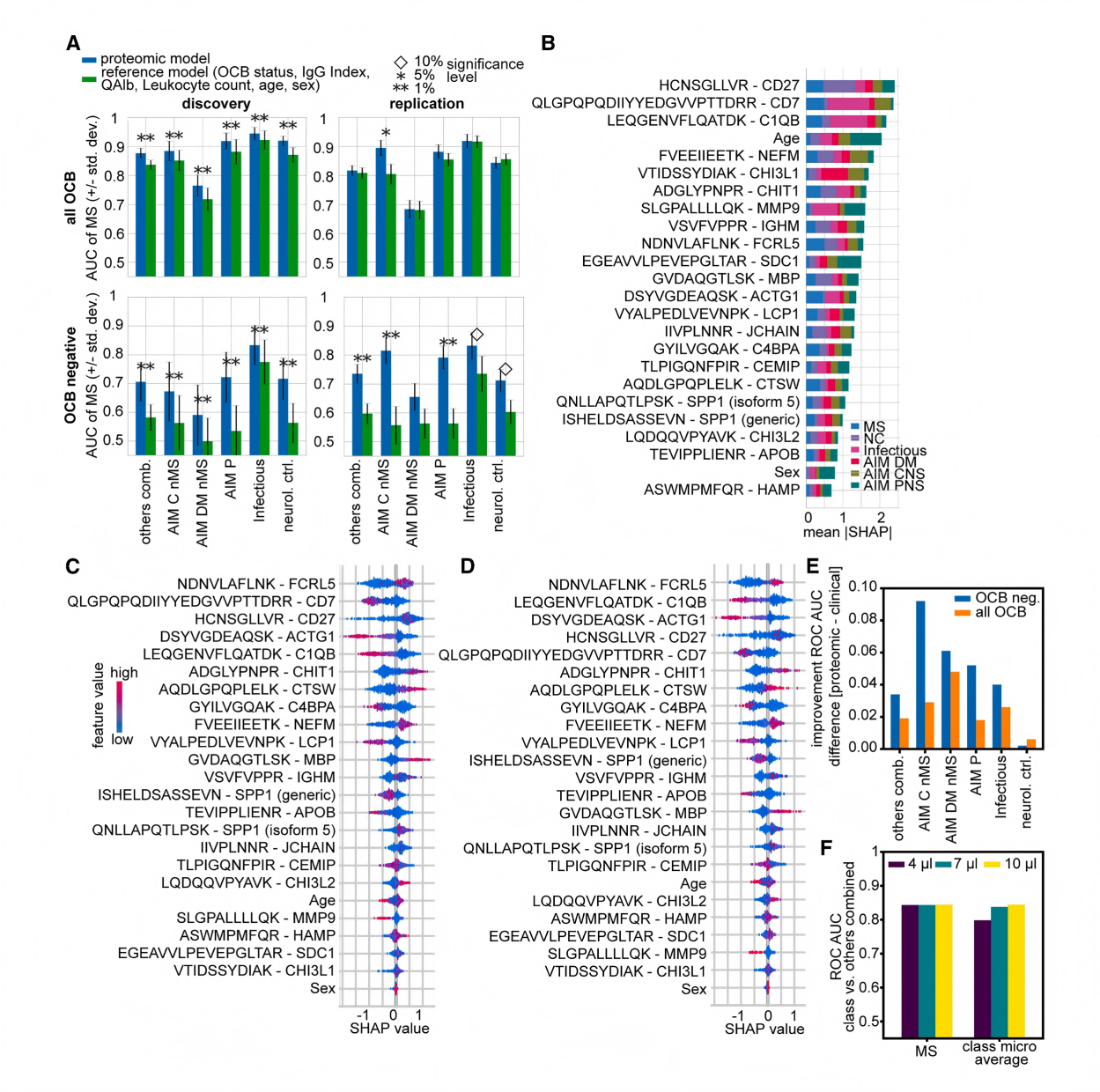
图6 针对22种蛋白的靶向检测以分离OCB阳性和阴性多发性硬化症与中枢神经系统炎症
6.“伪时间”模型实现多发性硬化症未来疾病轨迹预测
为解析复发缓解型多发性硬化症(RRMS)与进展型多发性硬化症(PMS,包括原发进展型PPMS和继发进展型SPMS)的分子差异,利用Orbitrap Astral数据进行机器学习分类,并通过降采样策略控制年龄与白细胞计数的混杂影响,生成年龄/白细胞分层子集。比较全数据集和分层子集的结果,发现RRMS富集适应性免疫标志,PMS则以先天免疫、TGF-β信号和胶质细胞耗竭标志为主,后者与神经退行性疾病特征重叠,印证了“进展独立于复发活动”的概念。FCRL5与CTSW同时出现在诊断标志物组合和PMS特征中,提示其在MS全程中的关键作用。进一步基于分类模型SHAP值构建蛋白质组伪时间,发现该伪时间与ARMSS评分显著相关(r=0.21–0.28),即使ARMSS在CSF采样后长达15年才获得;后续转化为SPMS的RRMS患者基线伪时间显著高于未转化者(中位转化时间3年,伪时间与转化时间负相关r=-0.73)。该蛋白质组分期系统可在诊断时预测未来数年的疾病轨迹,为早期识别高进展风险患者、指导阶段性治疗策略调整提供了强有力的分子工具。
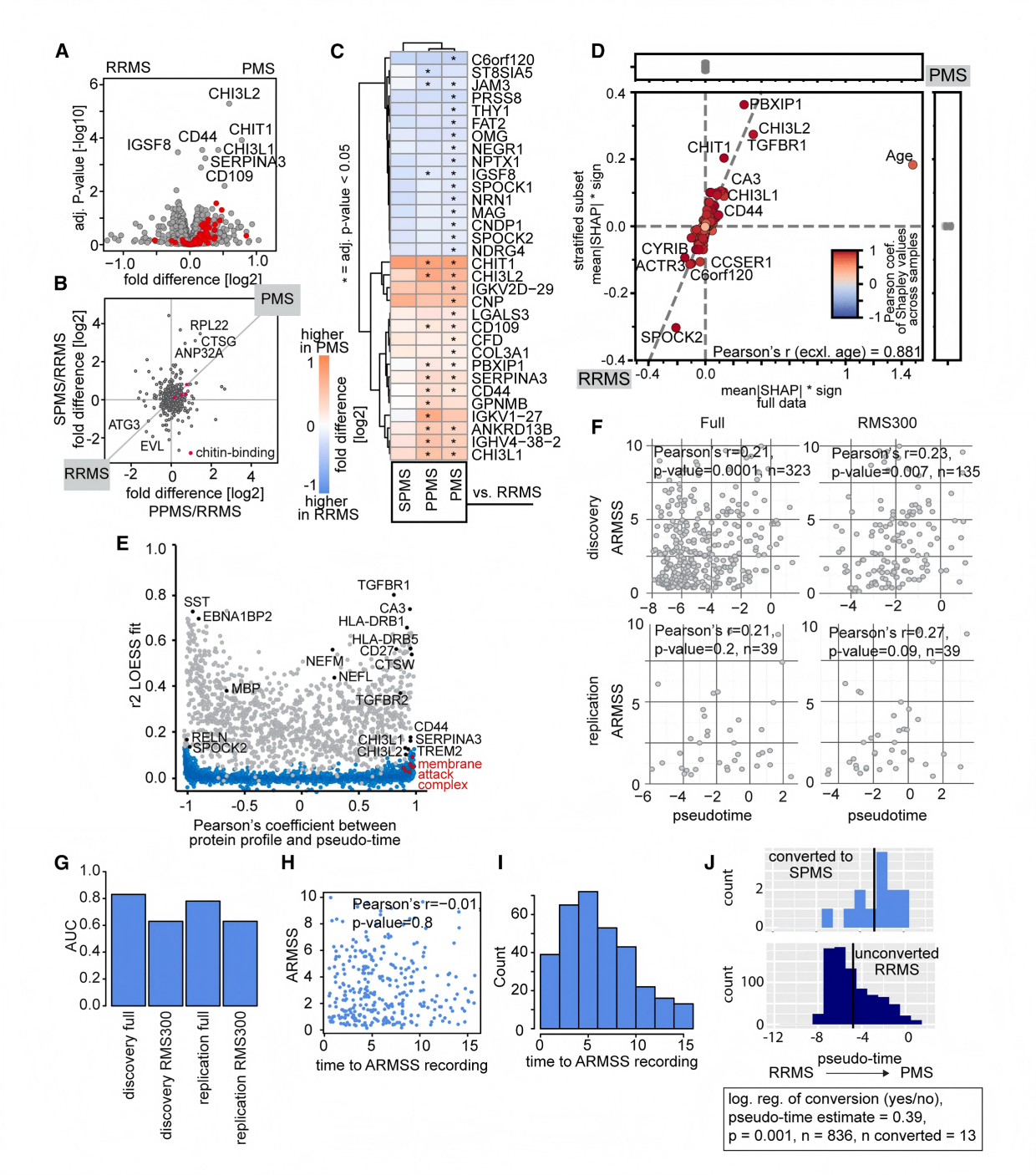
图7 复发和PMS的CSF改变及病程转换
研究结论
本研究通过大规模、高通量的脑脊液蛋白质组学分析,系统性地描绘了多种神经系统疾病的蛋白质组图谱,尤其在多发性硬化症的诊断和机制研究中取得了突破。研究识别出一个22蛋白组合用于多发性硬化症的精准诊断,特别是在OCB阴性患者中表现优异,并通过靶向质谱法实现了其临床转化。此外,研究还揭示了与疾病进展相关的蛋白质轨迹和潜在药物靶点。体液蛋白质组在疾病标志物发现、机制解析、预后建模和药物靶点筛选中发挥了核心作用,为精准神经病学提供了强有力的技术平台和数据基础。
参考文献
[1] BADER J M, MAKAROV C, RICHTER S, et al. Large-scale proteomics across neurological disorders uncovers biomarker panel and targets in multiple sclerosis [J]. Cell, 2026.
