
阿尔茨海默病(AD)作为高发神经退行性疾病,核心病理为蛋白错误折叠、异常聚集,且病理改变远早于临床症状出现,早期精准诊断是临床刚需。但现有诊断依赖脑脊液穿刺、PET-CT,侵入性强、成本高,无法大规模筛查;常规血浆标志物仅关注蛋白丰度差异,忽略核心构象改变,灵敏度不足,且APOE基因型、性别等关键影响因素,也缺乏蛋白结构层面的系统解析。
近日,美国斯克里普斯研究所、加州大学圣地亚哥分校及堪萨斯大学等机构的研究团队,在《Nature Aging》(IF:19.4)期刊发表标题为“Structural signature of plasma proteins classifies the status of Alzheimer’s disease”的研究论文,该研究立足血浆蛋白构象变化,结合结构蛋白质组与机器学习方法,开发无创高精准AD诊断标志物体系。

样本信息
本研究纳入520例血浆样本,来自两个独立队列:
KU ADRC队列(n = 320):含完整临床与认知评分,50例样本长期纵向随访,用于模型动态验证,其中50例为纵向随访样本(最长255天)。
UCSD队列(n = 200):提供性别、年龄及脑脊液(CSF)Aβ和tau数据,用于病理验证。
研究分组:包含健康对照(NOR)、轻度认知障碍(MCI)和AD患者,分层纳入不同APOE基因型、性别、神经精神症状程度样本,排除混杂干扰。
实验技术
共价蛋白谱(CPP)技术(基于赖氨酸暴露程度的蛋白质结构定量技术,又称为二甲基标记技术)、LC-MS/MS、机器学习(18种算法)
研究亮点速递
首次系统描绘AD进展中血浆蛋白质结构组变化,发现结构变化比表达变化更具区分度。
揭示APOE ε4基因型对蛋白质结构的广泛影响,特别是C1QA和SERPINA3的构象变化。
发现神经精神症状与蛋白质结构变化存在性别依赖性关联。
基于C1QA、CLUS和ApoB的3条肽段构建深度学习模型,实现AD分期的高精度分类(三分类准确率83.44%)。
模型与脑室体积、CSF生物标志物、MMSE/CDRSUM评分显著相关,并在纵向样本中验证其预测能力。
研究结果
1、AD患者血浆蛋白质结构特征分析
研究方法:采用CPP技术对血浆879个核心肽段(对应109个蛋白)的赖氨酸可及性进行定量检测,对比NOR、MCI、AD三组样本的蛋白质可及性均值、结构变异系数(CV),对比蛋白结构变异与表达变异差异。
研究结果:随疾病进展梯度(健康→MCI→AD),血浆蛋白赖氨酸可及性呈逐级显著下降趋势(93.2% → 92.0% → 91.1%),提示疾病进展中蛋白折叠异常、赖氨酸位点被包裹;蛋白结构CV值逐步升高(7.4%→8.1%→8.8%),提示结构异质性增强;三组样本间蛋白表达丰度无统计学差异,证实蛋白质结构变化较丰度变化更能精准反映AD疾病状态,具备更强的疾病分类潜能。
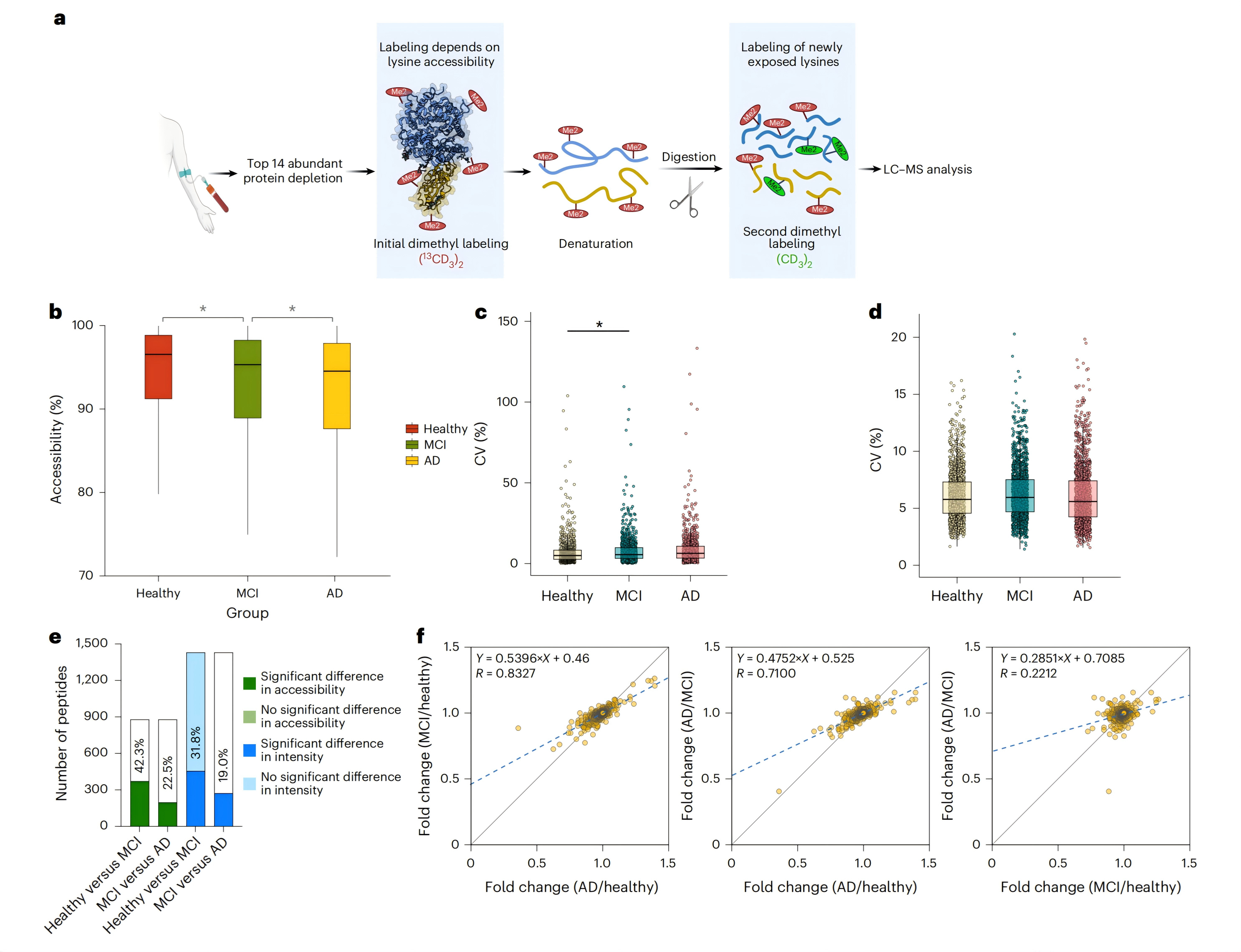 图1 879条肽的可及性分布
图1 879条肽的可及性分布
2、APOE基因型对血浆蛋白构象的调控机制
研究方法:以APOE ε3/ε3基因型为参照,采用多元线性回归分析不同基因型对应的蛋白赖氨酸可及性差异,结合蛋白结构模拟解析其分子调控机制。
研究结果:APOE ε4/ε4纯合子携带者体内91个肽段(43种蛋白)的赖氨酸可及性显著降低,且ε4等位基因剂量与蛋白结构异常程度呈正相关;ApoE ε4可介导关键蛋白构象改变,从蛋白质结构层面揭示了该基因型为AD高危因素的分子机制。
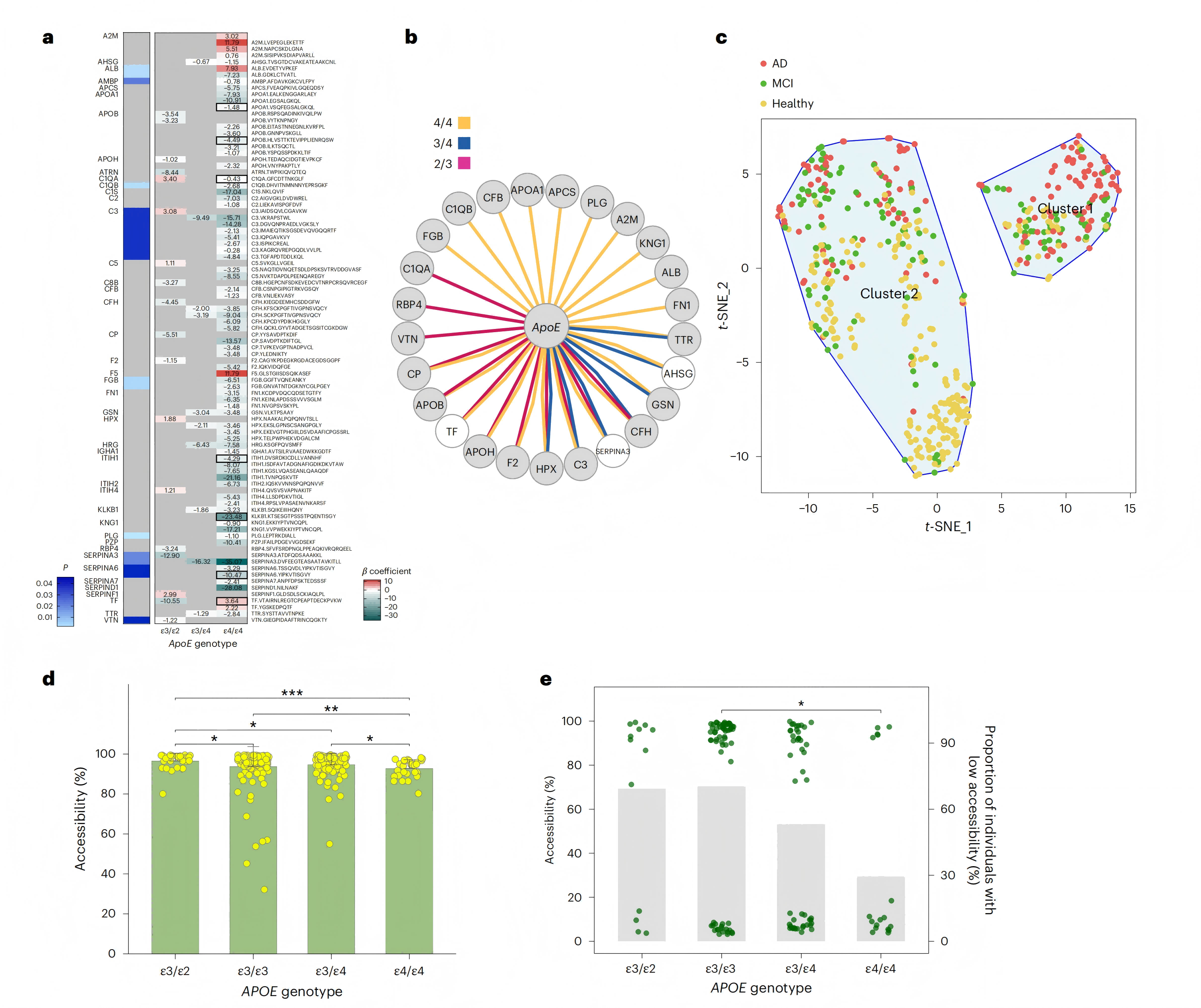
图2 受APOE基因型影响的蛋白质结构
3、性别与神经精神症状对蛋白构象的影响
研究方法:量化12项神经精神症状评分(NPS评分),采用线性回归分析可及性与NPS的关联,并检验性别交互作用。
研究结果:AD患者NPS评分与蛋白可及性呈显著负相关,症状越重,蛋白构象异常越明显;女性AD患者NPS相关蛋白结构变化更显著,诊断区分度更高;筛选出APCS、ApoD、CLUS、C1S等10种与NPS相关且无性别差异的AD核心蛋白,富集于淀粉样变性和AD相关通路。ITIH2的构象变化在男性中对MCI vs AD的区分能力显著优于女性(AUROC 0.838 vs 0.625)。
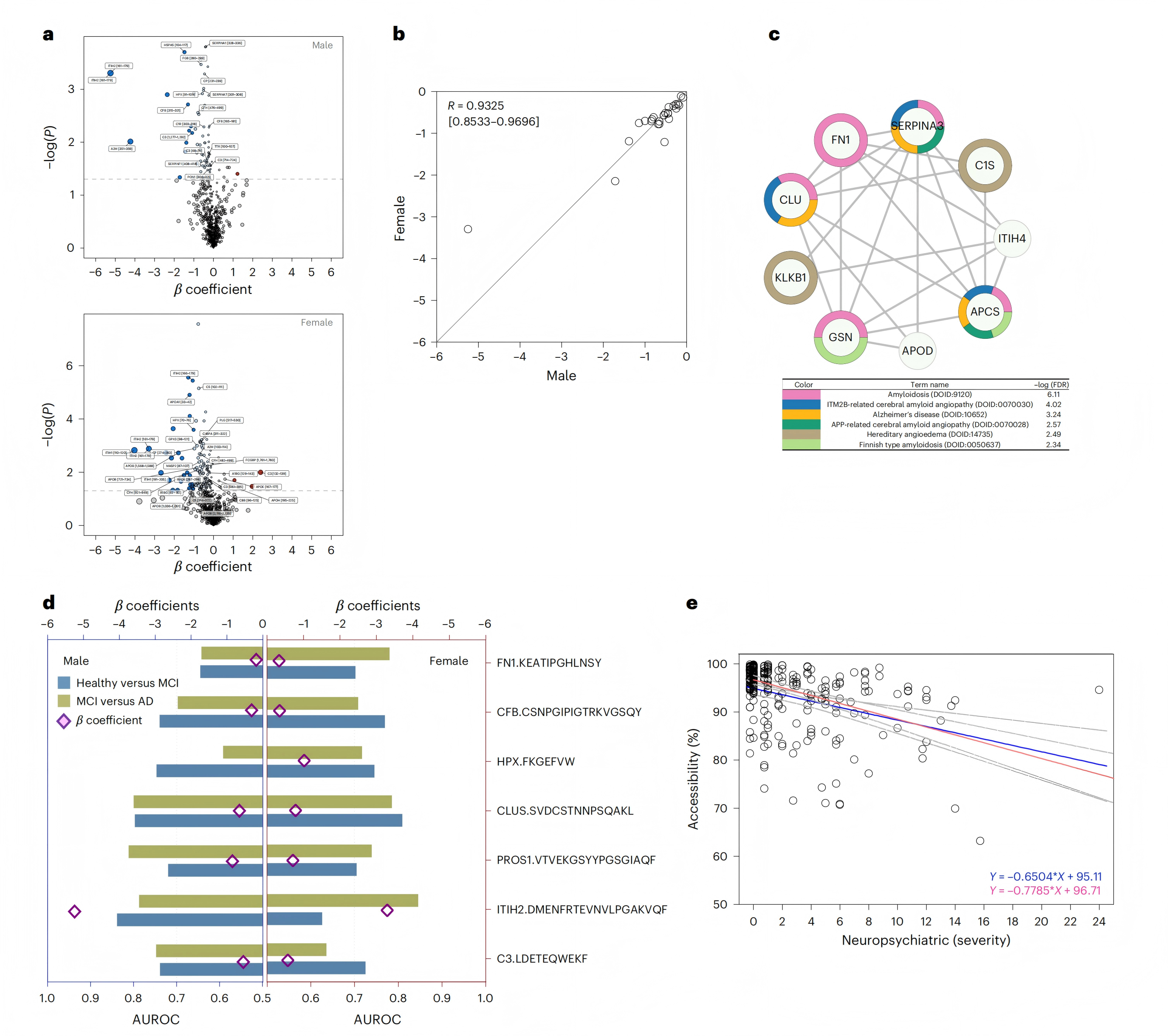 图3 蛋白质结构与NPS的性别依赖性关联
图3 蛋白质结构与NPS的性别依赖性关联
4、构建基于蛋白质结构的深度学习多标志物模型
研究方法:将470例样本按2:1分为训练集(313例)和测试集(157例),纵向样本(50例)用于验证。采用18种机器学习算法建模。
研究结果:深度学习模型表现最佳,测试集三分类准确率达83.44%(训练集88.49%),筛选C1QA(GFCDTTNKGLF)、CLUS(SVDCSTNNPSQAKL)、ApoB(AVLCEFISQSIKSF)三条肽构建三标志物诊断panel,三组样本分类准确率达83.44%,二分类诊断AUC值均高于0.93;而基于表达量(强度)的相同蛋白模型三分类准确率仅为64.3%,全蛋白表达模型也仅为65.0%,凸显结构信息的诊断价值。纵向随访样本检测准确率达86%,诊断效能显著优于传统丰度组学模型。
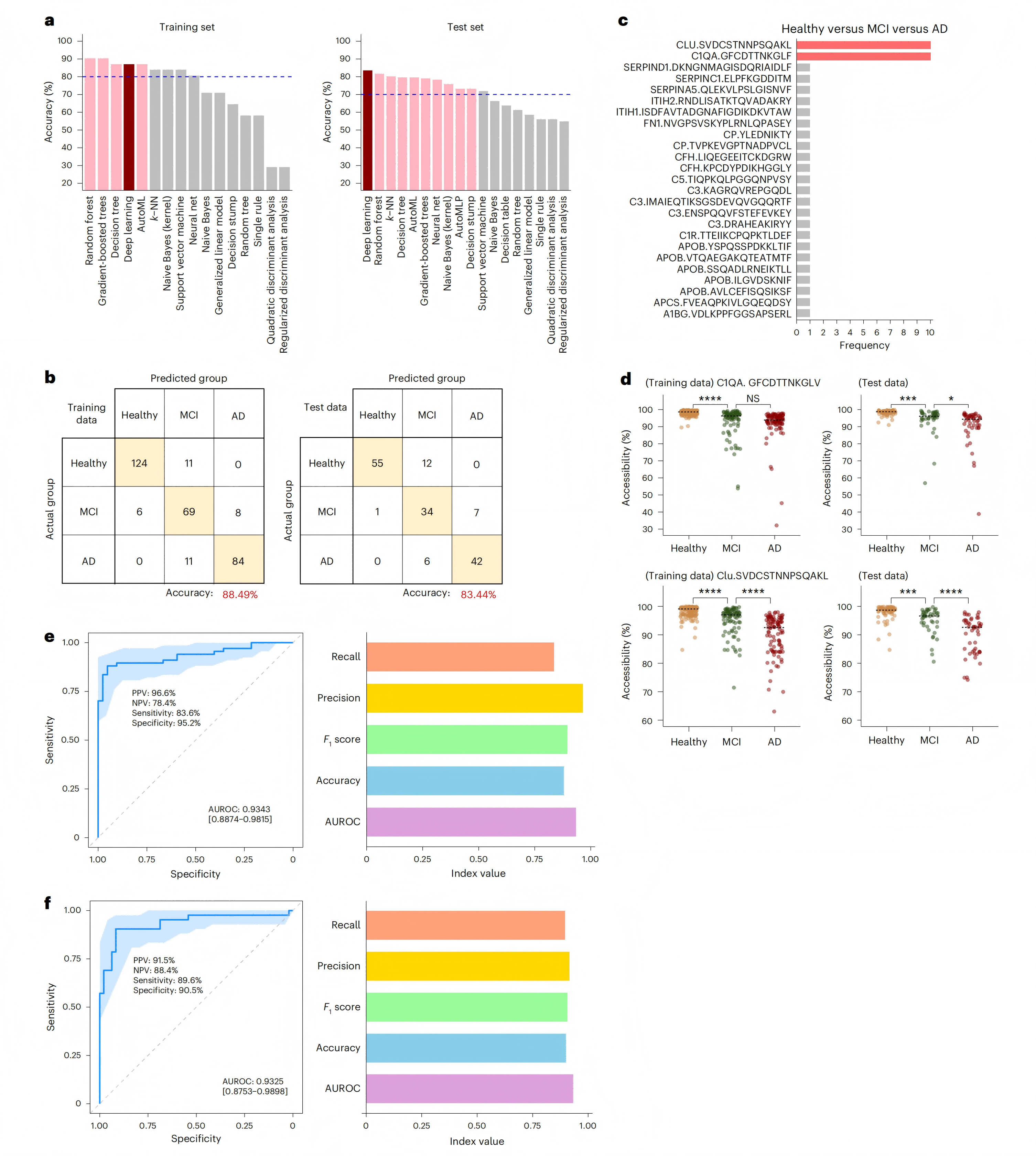 图4 利用深度学习算法生成多结构标记模型
图4 利用深度学习算法生成多结构标记模型
5、模型与临床指标、脑影像、CSF生物标志物显著相关
研究方法:将模型输出的“AD置信分数”与MMSE、CDRSUM、脑室体积、CSF指标进行相关性分析。
研究结果:构AD置信分数与MMSE呈强负相关(R = -0.800),与CDRSUM呈强正相关(R = 0.850);与第三脑室体积显著正相关(R = 0.48),提示与脑萎缩相关;与CSF Aβ42(R = -0.36)、p-tau181(R = 0.40)、t-tau(R = 0.60)等指标显著相关;尽管相关性中等,但结构信息与浓度信息互为补充,提供了不同的生物学视角。
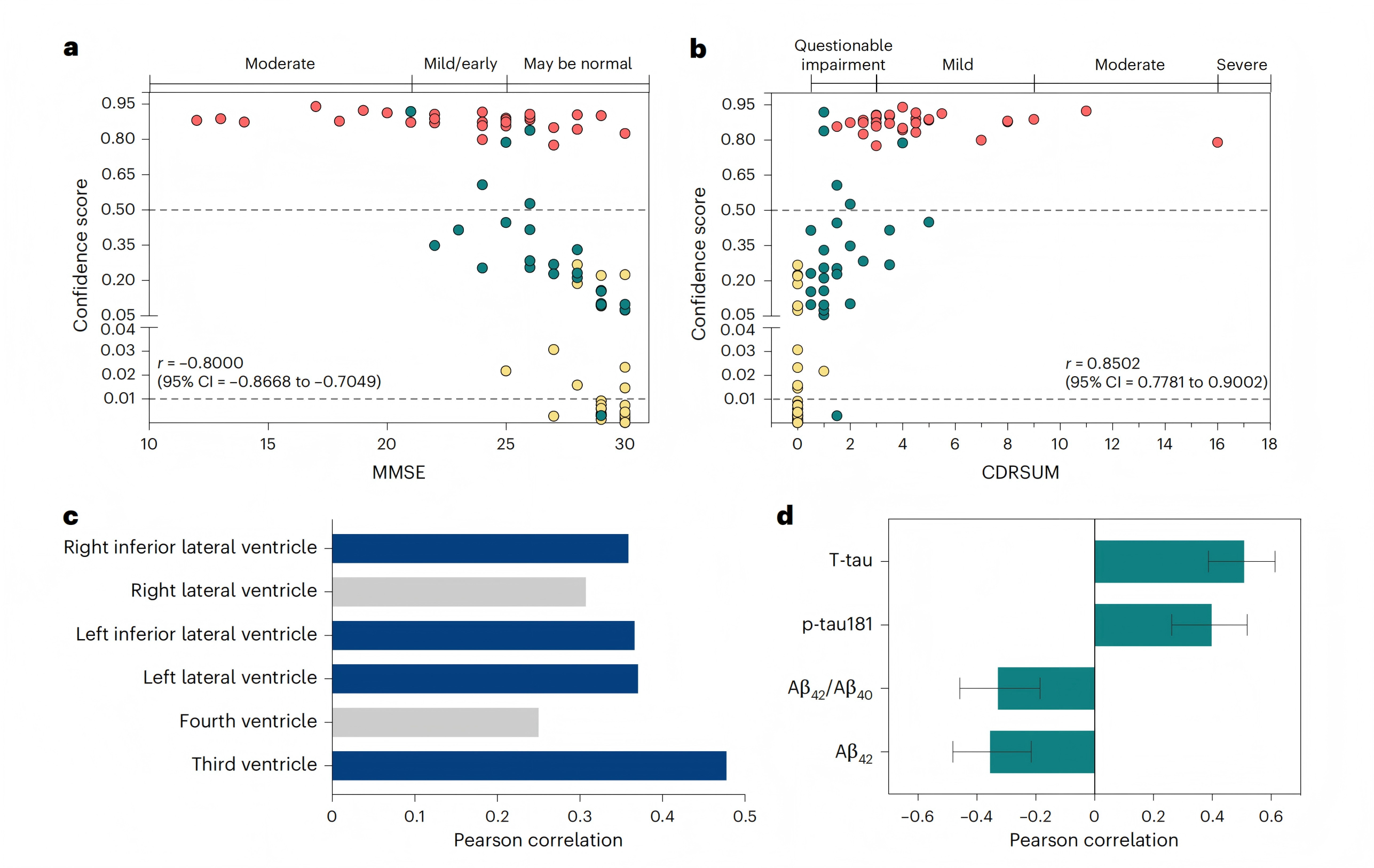 图5 多标记panel与病理变化的关联
图5 多标记panel与病理变化的关联
6、纵向样本验证模型的预测能力
研究方法:对50例纵向样本(最长255天)进行分类评估。
研究结果:理模型分类准确率达86.0%;在诊断状态发生变化的个体中,AD置信分数显著上升(P = 0.0019);仅CLUS的SVDCSTNNPSQAKL在诊断转变组中可及性显著下降,提示其可能作为疾病进展的动态标志物。
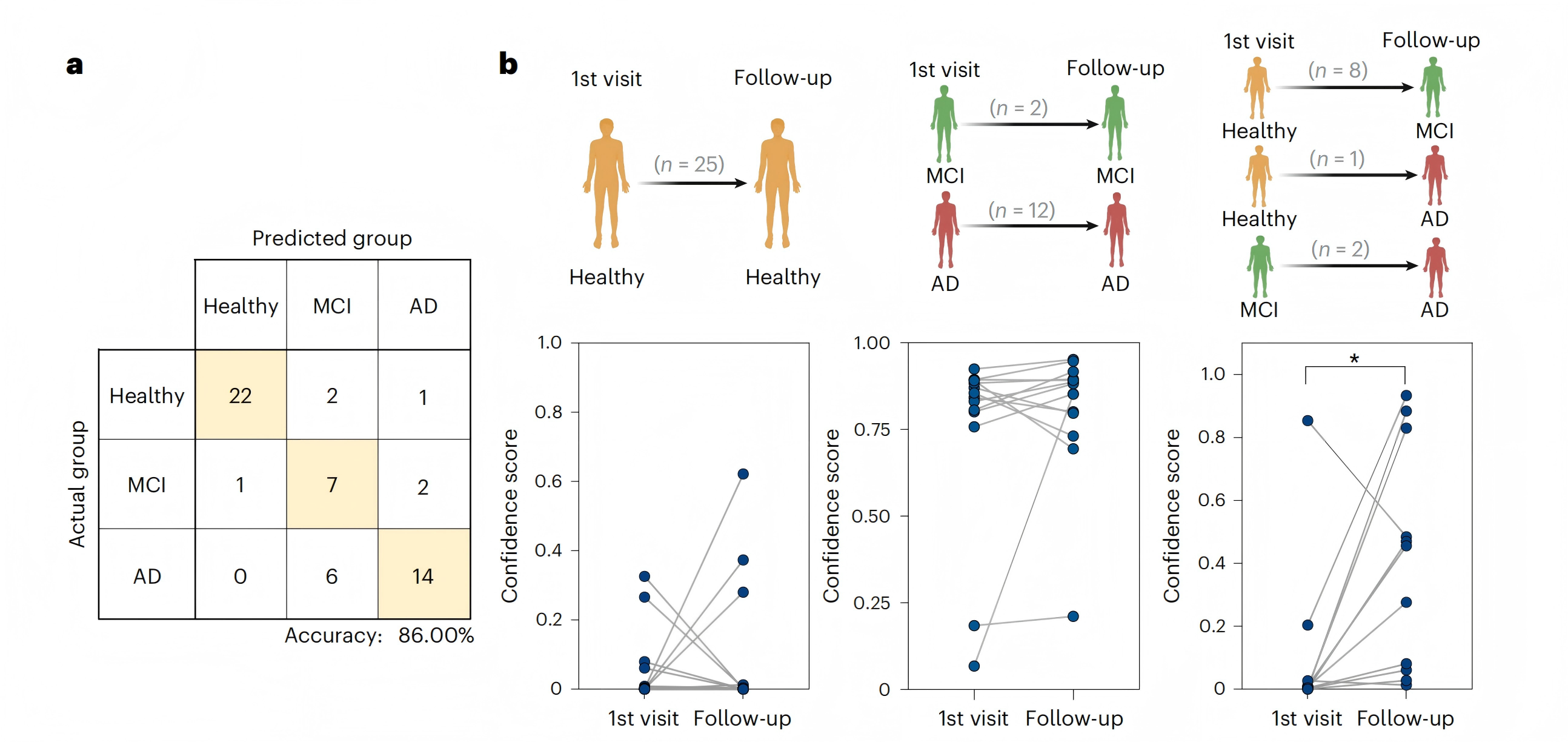 图6 验证多标记模型的随访纵向样本
图6 验证多标记模型的随访纵向样本
研究结论
本研究首次基于血浆蛋白质结构变化,系统揭示了AD进展过程中与APOE基因型和神经精神症状相关的构象扰动。
通过深度学习构建的C1QA-CLUS-ApoB结构三标志物模型,具备无创、高精准、可动态监测的优势,可有效区分健康人群、MCI患者与AD患者,适用于大规模临床早期筛查与病程监测。
结构蛋白质组学联合机器学习算法,为神经退行性疾病无创生物标志物开发提供了全新的结构导向型液体活检策略,以及可复制的标准化研究范式,具备极高的临床转化与科研拓展价值。
参考文献与全文链接
[1] Son A, Kim H, Diedrich JK, et al. Structural signature of plasma proteins classifies the status of Alzheimer's disease. Nat Aging. 2026 Feb 27. doi: 10.1038/s43587-026-01078-2.
技术服务延伸
高深度血浆蛋白组解析,标准化技术体系支撑
作为血浆蛋白质组学领域的专业服务商,青莲百奥依托高深度、标准化、可验证、一站式的完整技术体系,为科研工作提供全方位支持。凭借专利磁珠技术深度富集血浆蛋白,搭配自动化实验流程,稳定产出高质量、大队列可靠数据,为后续深入研究奠定坚实基础。

聚焦构象差异挖掘,助力疾病标志物创新研究
围绕蛋白构象差异解析、疾病特异性标志物开发等关键科研需求,青莲百奥提供专业化技术方案,涵盖限制性酶切质谱分析技术(Lip MS)与二甲基标记质谱分析技术,助力科研人员精准解析蛋白结构变化,高效推进标志物筛选与分子机制研究,赋能高质量科研成果高效落地。