在再生医学领域,3D生物打印技术为组织工程带来了前所未有的机遇。然而,3D生物打印组织替代物在临床应用中面临着两大主要挑战:异物反应(FBR)和血管化不足。FBR会导致植入物与宿主组织之间的纤维化隔离,而血管化不足则限制了组织的营养和氧气供应,影响功能恢复。解决这些问题的关键在于调节免疫反应、减轻FBR并促进血管生成。
2025年5月14日,中国人民解放军总医院研究团队在《Biofabrication》(IF=8.2)期刊上发表了一篇题为“Bioprinted M2 macrophage-derived extracellular vesicle mimics attenuate foreign body reaction and enhance vascularized tissue regeneration”的研究文章,该研究提出了一种创新的工程策略,利用膜挤压法制备巨噬细胞来源的细胞外囊泡模拟物(EVMs),并将其应用于3D生物打印组织替代物中,以减轻FBR并促进血管化组织再生。研究结合了蛋白质组学技术,深入分析了M2巨噬细胞来源的EVMs的功能成分和作用机制,揭示了其在免疫调节和组织再生中的潜在应用价值。

样本信息
细胞:小鼠巨噬细胞(J774A.1)、血管内皮细胞(C166)、成纤维细胞(L929)
动物模型:C57BL/6小鼠皮下植入实验、全层皮肤缺损模型
实验技术
M2-EVMs制备:IL-4诱导M2巨噬细胞→膜破碎→纳米级挤压→超速离心纯化
3D生物打印:明胶-海藻酸盐水凝胶负载EVMs,低温打印+钙离子交联
多组学分析:蛋白质组学(LC-MS/MS)、转录组测序(RNA-seq)
功能验证:划痕实验、血管形成实验、免疫荧光染色
研究亮点
1. 揭示了3D生物打印支架的刚性与巨噬细胞极化之间的关系:研究发现3D生物打印支架的刚性会加剧异物反应和纤维化,而柔软支架则促进抗炎的M2型巨噬细胞极化,减轻炎症。
2. 开发了M2型巨噬细胞来源的细胞外囊泡模拟物(EVMs)作为生物墨水添加剂:M2-EVMs在体外实验中表现出良好的生物活性,可抑制纤维化、促进血管生成并调节巨噬细胞极化。
3. 在体内模型中验证了M2-EVMs的改善效果:在小鼠模型中,M2-EVMs显著减轻炎症,减少纤维囊形成,促进血管化和组织再生,展现出良好的促再生效果。
研究结果
一、巨噬细胞极化失衡加剧3D生物打印支架刚性介导的异物反应(FBR)
小鼠皮下植入实验显示,刚性支架引发更严重的FBR,表现为更高的纤维囊厚度和胶原沉积。软支架周围以M2型巨噬细胞为主,硬支架周围以M1型巨噬细胞为主,表明FBR加剧与M1型巨噬细胞相关。转录组测序显示,硬支架上调基因富集于炎症通路,而软支架中M2型巨噬细胞标志物和抗炎因子上调。软支架的血管化能力更强,表明M2型巨噬细胞有助于缓解硬支架植入后的FBR和血管化不足问题。
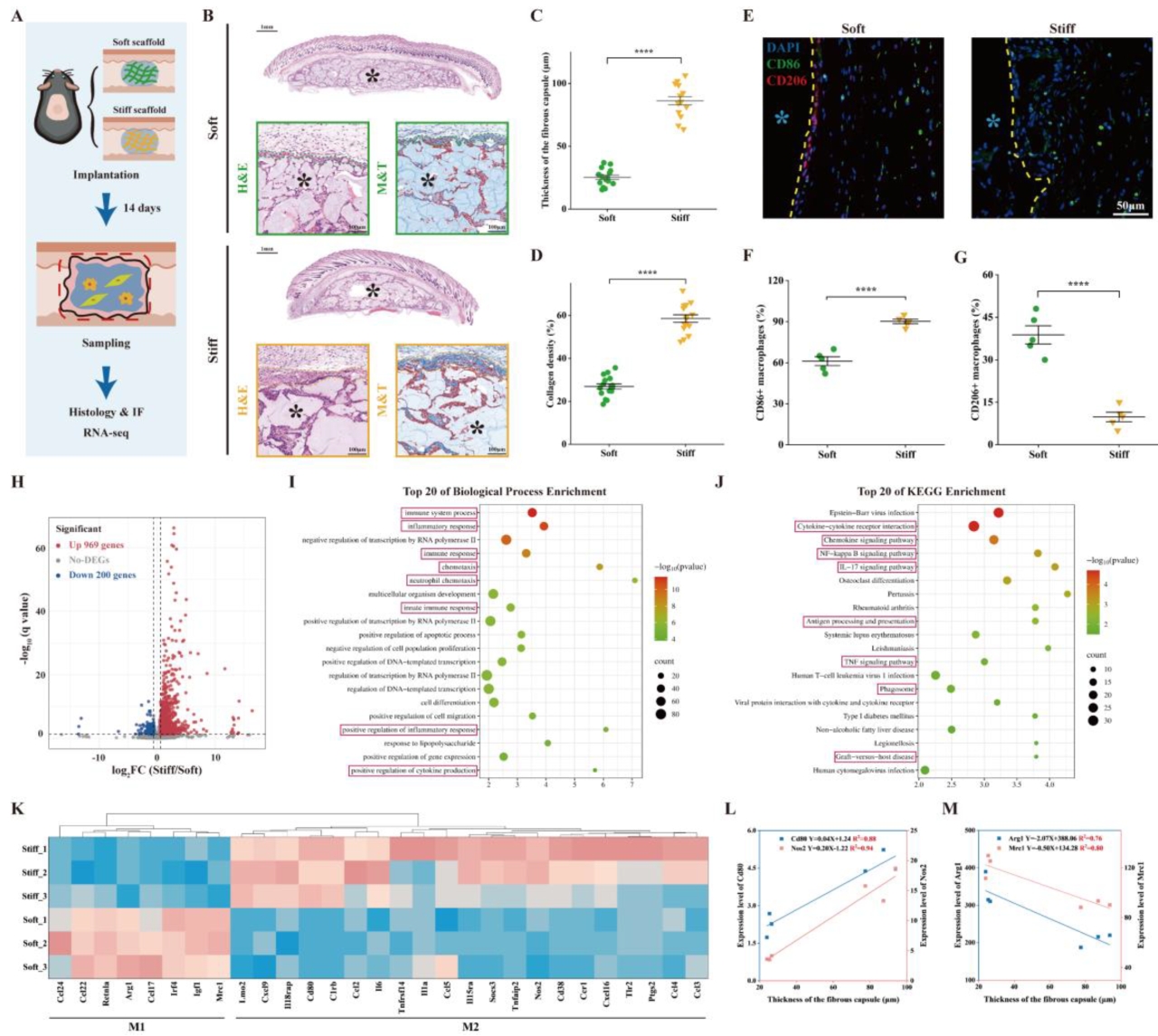
图1 巨噬细胞极化失衡加剧3D生物打印支架硬度介导的异物反应
二、巨噬细胞来源的EVMs的制备与表征
本研究通过膜挤压法制备了M1和M2型巨噬细胞来源的EVMs,并验证了其表型稳定性。经LPS/IFN-γ和IL-4诱导及超速离心纯化后,EVMs粒径均一,呈典型杯状结构,保留了巨噬细胞标志物(如CD14、TLR4)。在5×10¹⁰颗粒/mL浓度下,EVMs无细胞毒性,显著促进血管内皮细胞增殖,且被选为后续实验浓度。血管内皮细胞对EVMs的摄取能力高于成纤维细胞和巨噬细胞,显示出更高的亲和力。
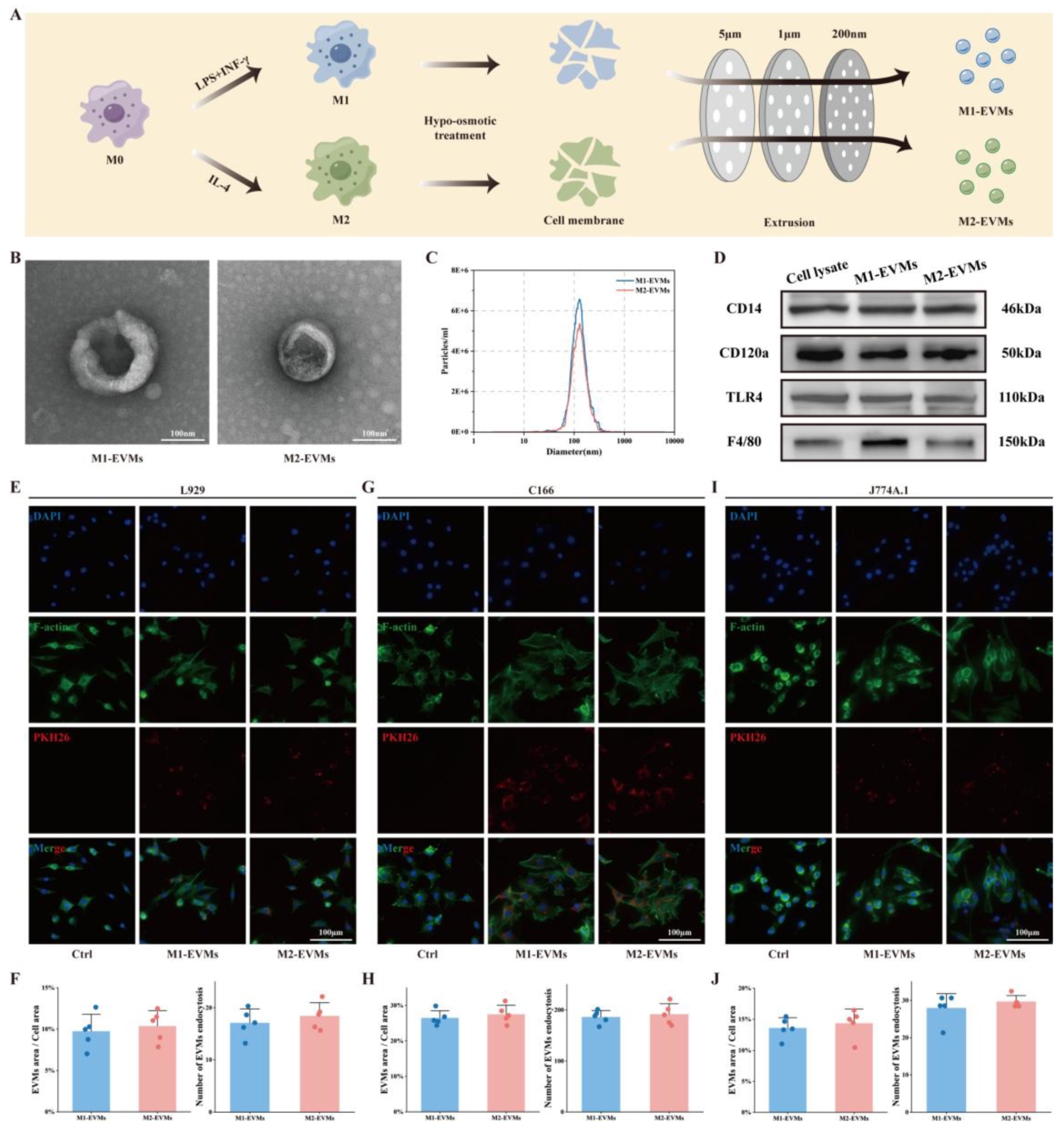
图2 极化巨噬细胞来源EVMs的制备流程与表征结果
三、巨噬细胞来源EVMs的蛋白质组学分析
蛋白质组学分析显示,M2-EVMs与M1-EVMs存在显著差异。M2-EVMs的上调蛋白主要涉及囊泡生成、信号转导和细胞反应,且在血管生成相关蛋白表达上显著高于M1-EVMs,表现出更强的促血管生成潜力。相反,M1-EVMs的下调蛋白主要与炎症反应、细胞因子反应和抗原呈递相关,可能引发更严重的FBR和纤维化。此外,M2-EVMs在对外源物和机械刺激的反应相关GO项中表达较低,表明其对外源性高硬度植入物的反应性较低。KEGG通路分析显示,M2-EVMs在宿主抗移植物通路中的表达水平较低,缺乏相关组分,进一步强调了其在避免FBR中的关键作用。
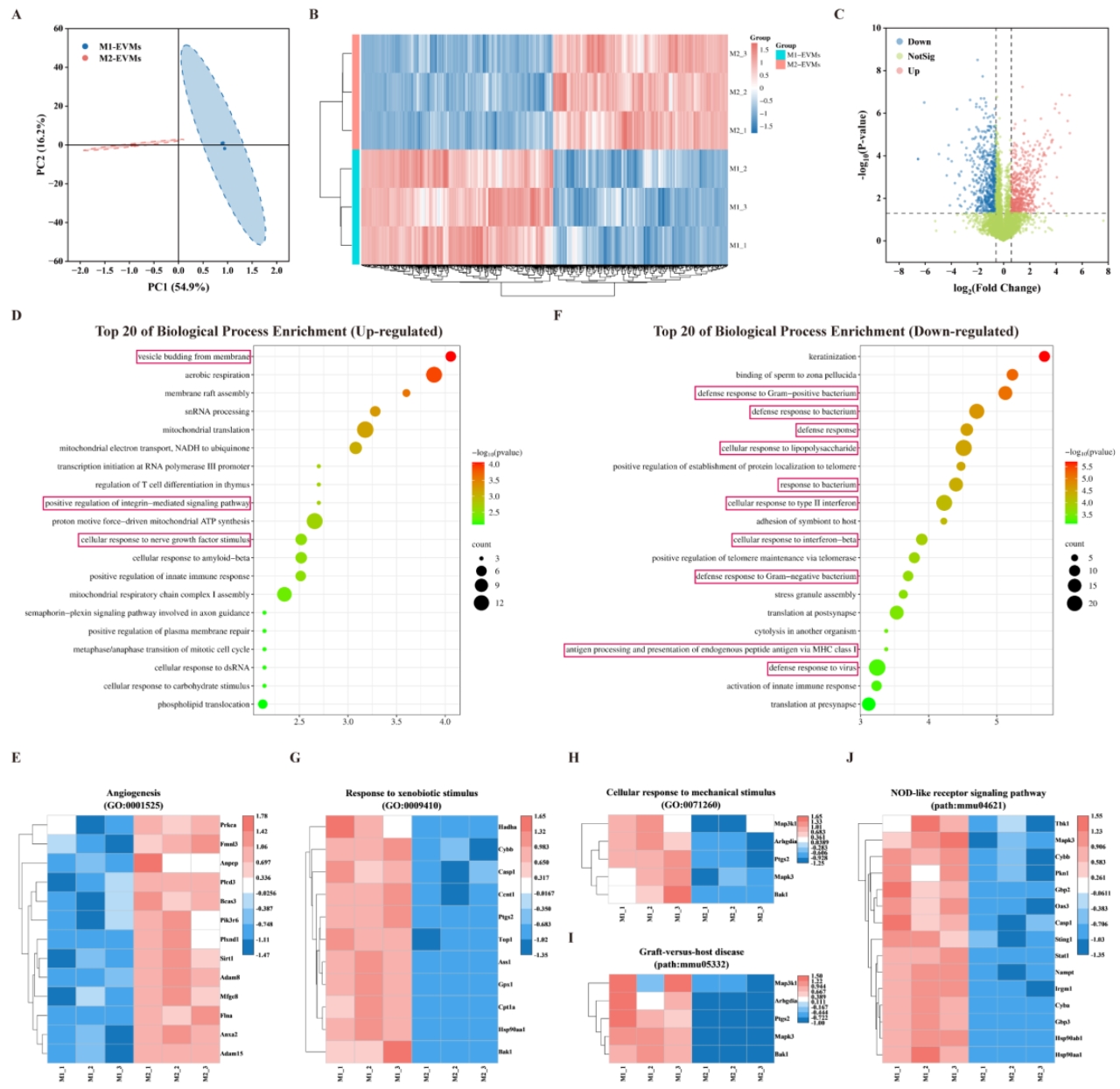
图3 M1和M2-EVMs的蛋白质组学分析
四、巨噬细胞来源的EVMs在体外调节纤维化、血管生成和巨噬细胞极化
体外实验表明,M2-EVMs具有多重调控功能:抑制纤维化(减少α-SMA和Vimentin表达,降低YAP-1阳性细胞比例),促进血管生成(增强内皮细胞迁移和血管网络形成),调控巨噬细胞极化(诱导M2型极化,上调IL-10,下调IL-1β/IL-6)。这些结果证实M2-EVMs通过“抑制纤维化-促进血管新生-调控免疫极化”的三重机制,为组织再生创造有利微环境。
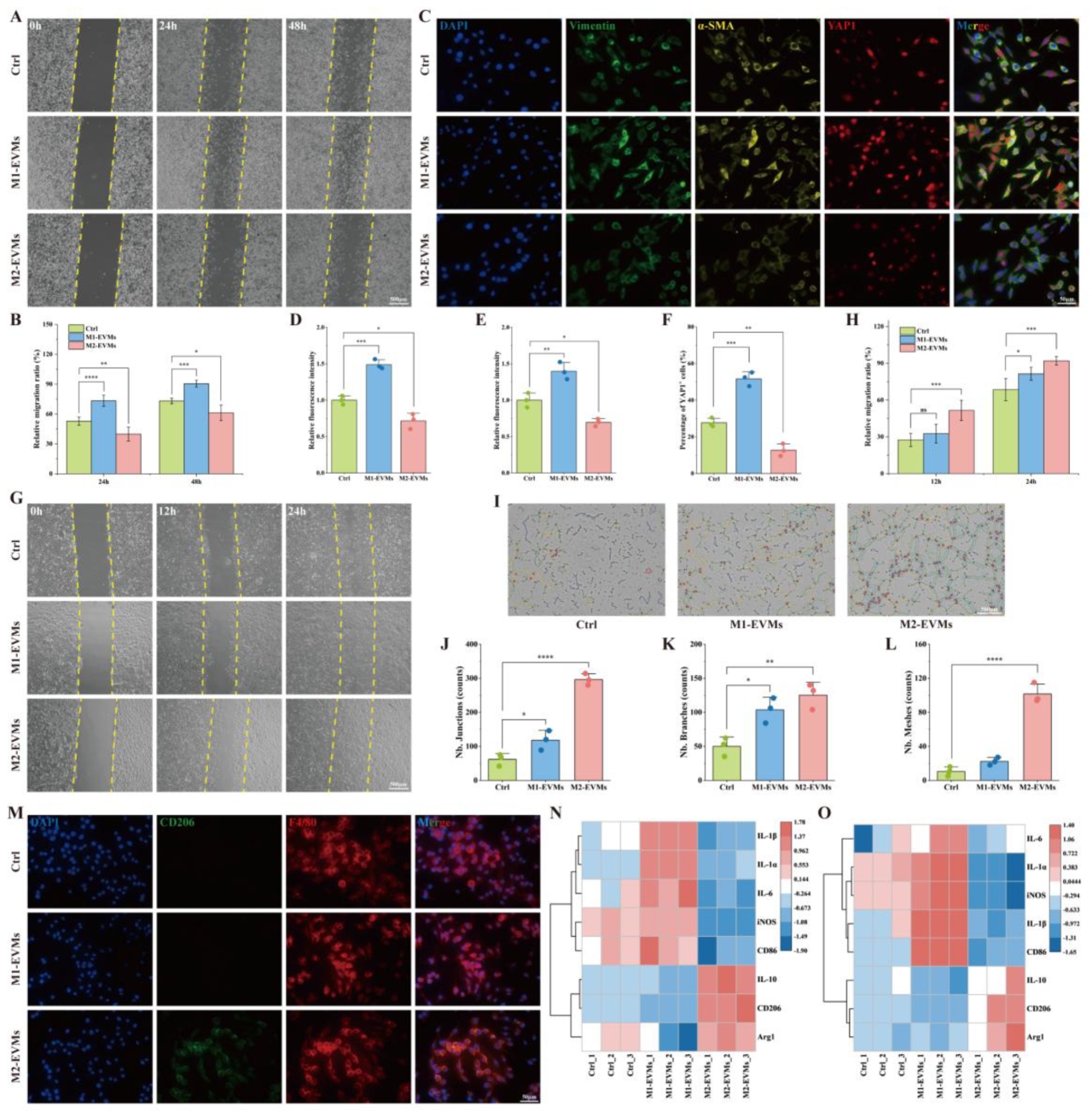
图4 M1和M2巨噬细胞来源EVMs对靶细胞的体外作用
五、含巨噬细胞来源EVMs的生物墨水的特性
研究发现,将巨噬细胞来源的EVMs添加到刚性海藻酸钠-明胶生物墨水中后,生物墨水的流变学特性、微观结构和力学性能均未显著改变,且EVMs在3D打印支架中能稳定存在并均匀分布。细胞活性与功能测试显示,EVMs的添加未影响细胞存活率或分布,但M1-EVMs促进了成纤维细胞的纤维化表型,而M2-EVMs则抑制了纤维化,并显著增强了血管内皮细胞的促血管生成能力及巨噬细胞的抗炎表型转化。这些结果与2D环境中的验证一致,证明了EVMs作为生物墨水添加剂的稳定性和广泛应用潜力。
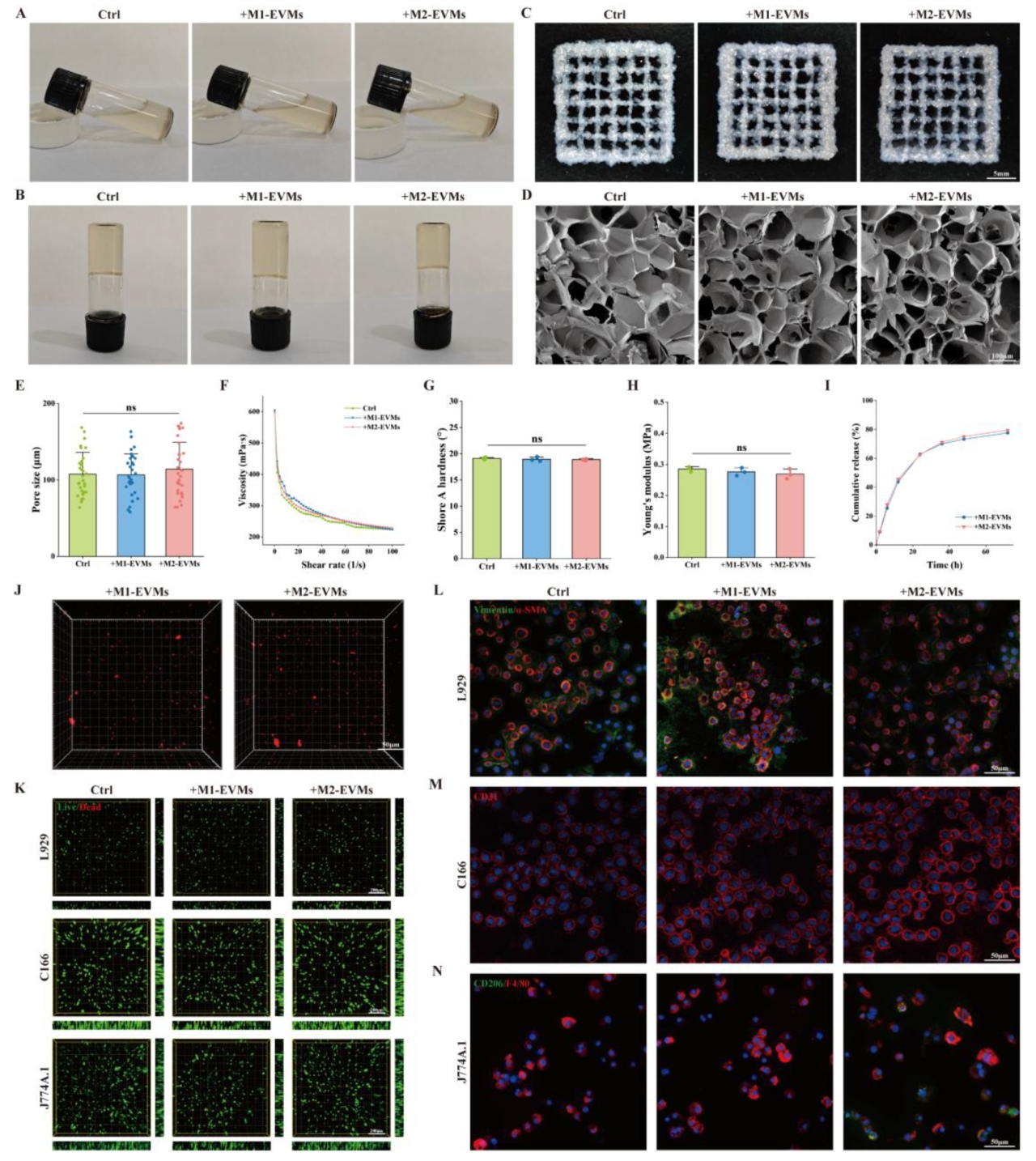
图5 M1和M2-EVMs对生物墨水的性质和靶细胞功能的影响
六、巨噬细胞来源的EVMs在体内有效调节FBR和巨噬细胞极化
小鼠皮下植入实验显示,M2-EVMs显著减轻异物反应性炎症(FBR),降低纤维囊厚度并增加M2型巨噬细胞数量,而M1-EVMs加剧炎症。第14天,炎症减轻,M2-EVMs组纤维囊厚度最低,且M2型巨噬细胞比例稳定,表现出良好的生物学功能。
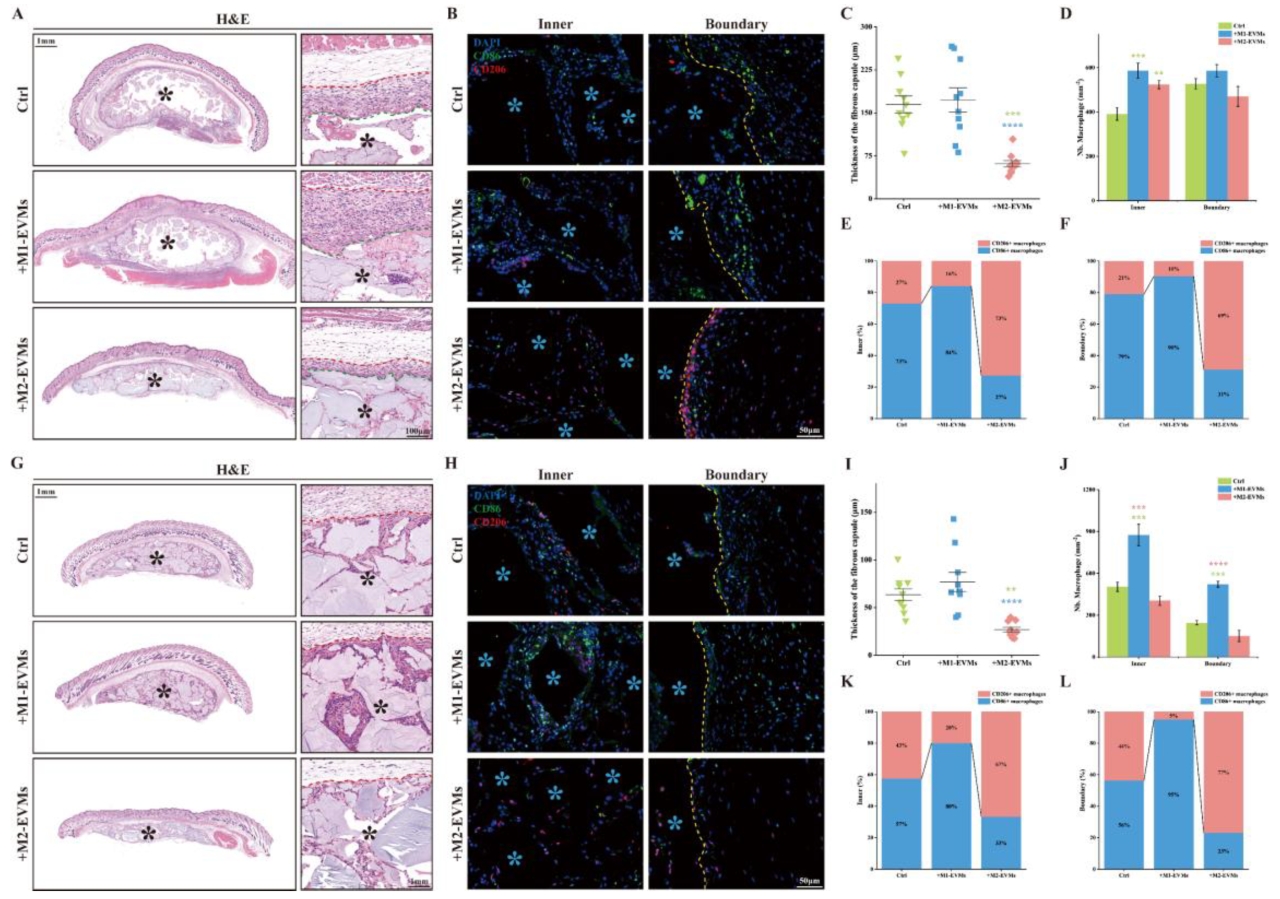
图6 M1-EVMs和M2-EVMs对皮下植入模型中FBR和巨噬细胞极化的影响
七、巨噬细胞来源的EVMs在体内有效调节了纤维化和血管化
体内实验显示,M2-EVMs显著调节纤维化和血管化。第7天,M2-EVMs组胶原层最稀疏且能招募血管生长;第14天,其胶原纤维更稀疏,支架与组织融合更紧密,而对照组和M1-EVMs组纤维囊更致密、纤维化更严重。M2-EVMs有效抑制纤维化并保持血管存在,促进支架存活和整合,表现出减轻炎症、抑制纤维化、促进M2型巨噬细胞极化和促进血管生成的显著疗效。
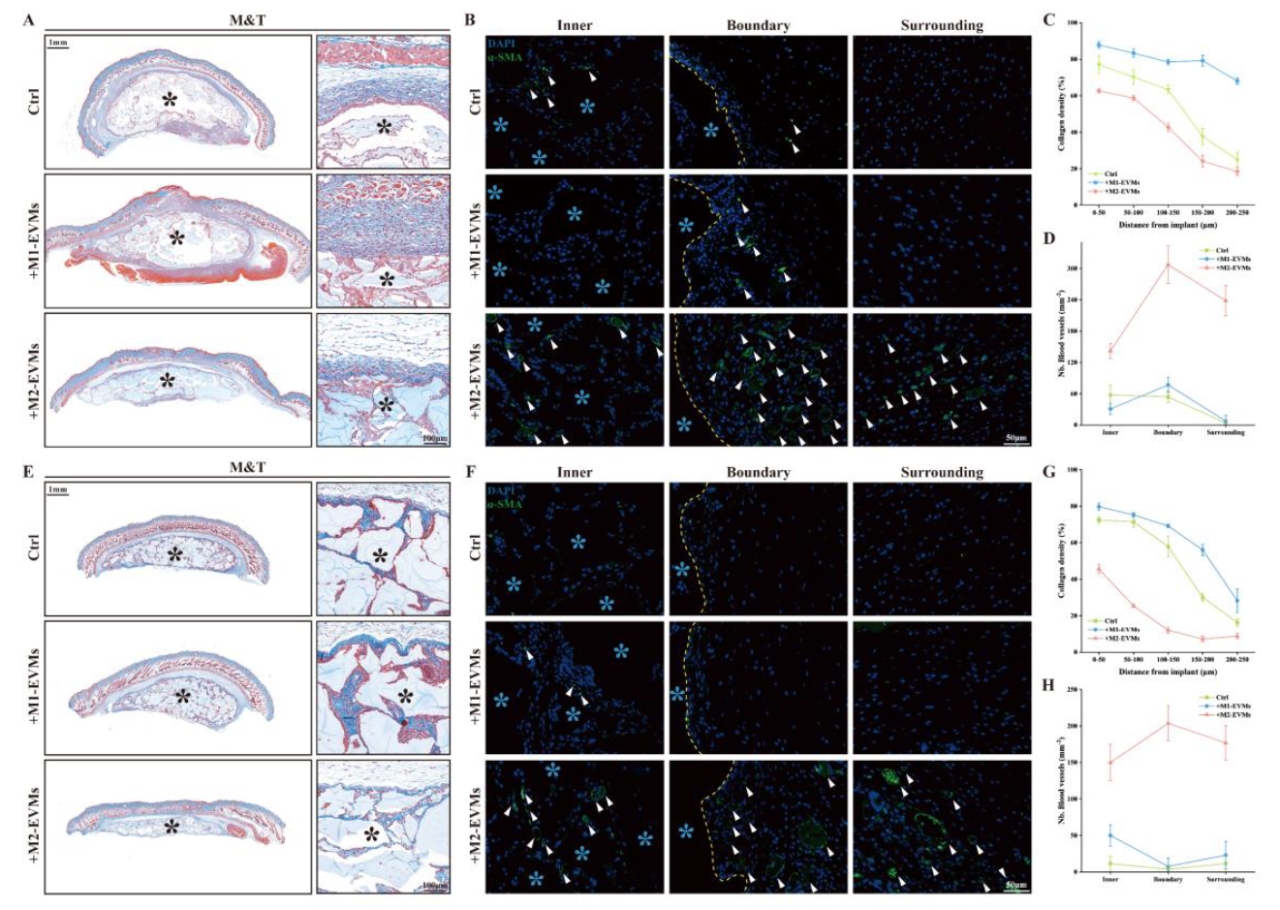
图7 M1和M2型巨噬细胞来源的EVMs对皮下植入模型中胶原沉积和血管生成的影响
八、巨噬细胞来源的EVMs对3D生物打印支架治疗皮肤伤口效果的影响
在小鼠全层皮肤伤口模型中,M2-EVMs显著加速了3D生物打印支架的伤口愈合。第7天伤口面积缩小且上皮化明显,第10天完全上皮化,第14天毛发再生显著。H&E染色显示M2-EVMs组炎症反应最轻,炎症层厚度仅为M1-EVMs组的约1/10,且上皮舌爬行距离最长。免疫荧光染色表明M2-EVMs显著增加M2型巨噬细胞比例。第14天,M2-EVMs组胶原沉积均匀且较少,显著促进血管和毛囊再生,而M1-EVMs组表现出更多纤维化和瘢痕样结构。
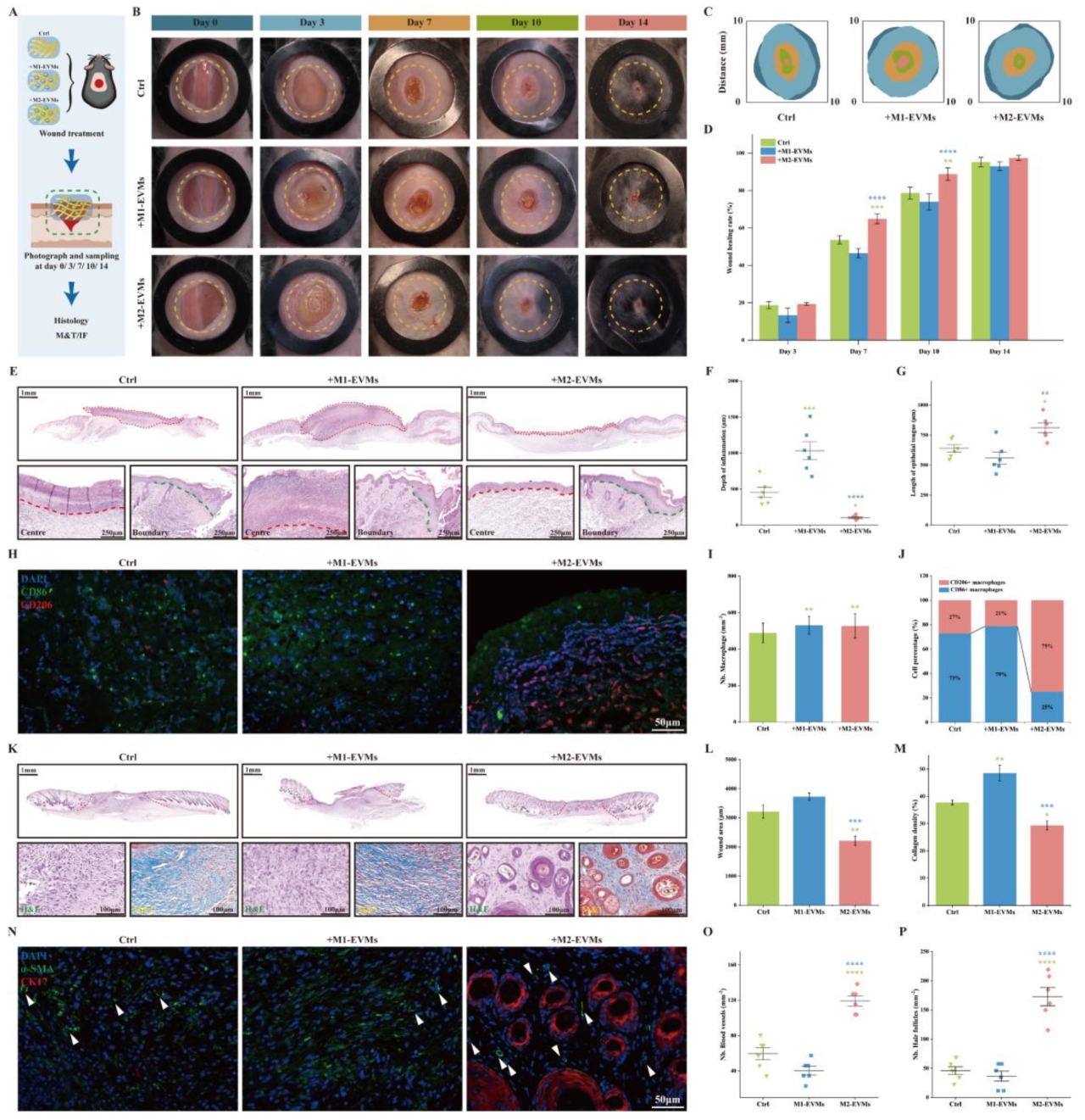
图9 M1-EVMs和M2-EVMs在伤口治疗模型中对伤口愈合的影响
研究结论
该研究通过制备M2巨噬细胞来源的细胞外囊泡模拟物(M2-EVMs),证实其能有效抑制异物反应(FBR)、减少纤维化、促进血管生成,并调节巨噬细胞向抗炎表型极化。
作为3D生物墨水的添加剂,M2-EVMs在皮下植入和皮肤伤口模型中显著改善组织再生,为生物打印组织的功能优化和临床应用提供了新策略。
青莲百奥细胞外囊泡蛋白组解决方案
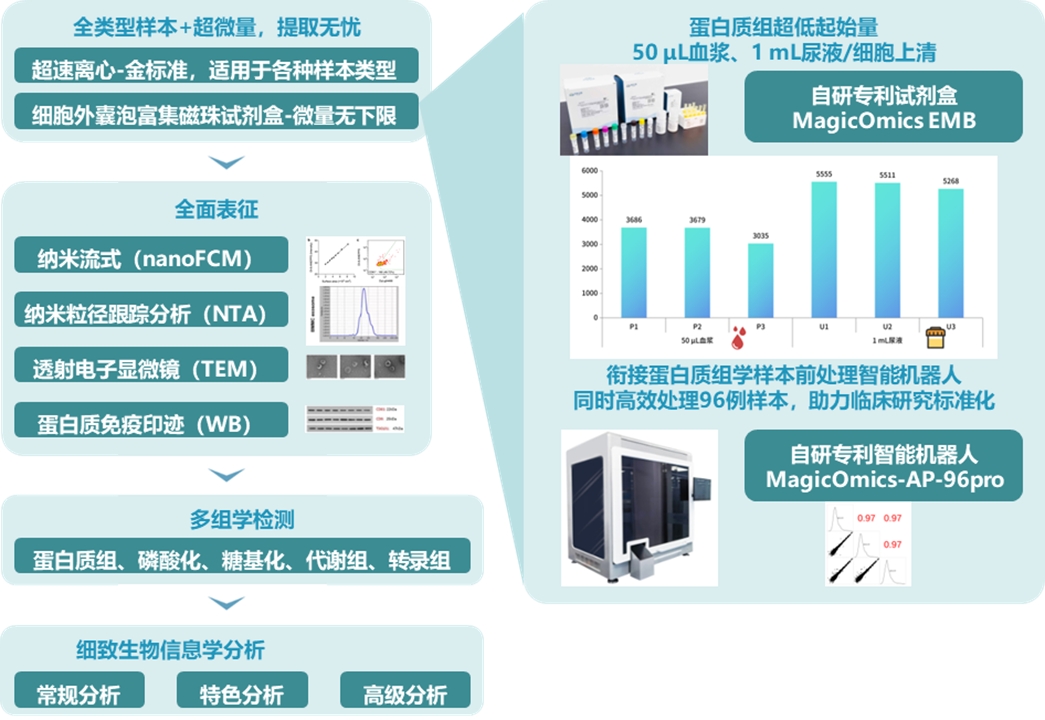
青莲百奥针对细胞外囊泡(EV)研究中的两大难点与需求——分离与表征,提供高通量标准化解决方案,包含超速离心法与独家专利产品MagicOmics EMB三大富集方案,电镜、Western Blot标志物检测、纳米粒径分析(NTA)、纳米流式分析四大表征方案,联合持续深耕的高深度蛋白质组学检测技术、自动化高通量前处理机器人与AI赋能的三大高级分析报告,轻松承接不同样本来源细胞外囊泡的检测、表征及大队列标志物研究项目。步骤虽繁必不敢省人工,试剂虽贵必不敢减物力,青莲百奥助您在科研的海洋中乘风破浪~
参考文献
[1] Zhang C, Fu Z, Liu Q, et al. Bioprinted M2 macrophage-derived extracellular vesicle mimics attenuate foreign body reaction and enhance vascularized tissue regeneration[J]. Biofabrication. 2025 May 14;17(3). doi: 10.1088/1758-5090/add49f.
青莲百奥合作文章
青莲百奥深度参与众多前沿研究,与中国医学科学院、中国科学院、军事医学研究院、国家蛋白质科学中心、四川大学华西医院等顶尖科研机构通力合作,累计发表SCI论文近200篇,累计影响因子(IF)超1500。多项重磅研究成果发表于《Nature》《Science Translational Medicine》《Nature Communications》等国际顶级期刊。