热蛋白质组学(TPP)——由欧洲分子生物学实验室Mikhail Savitski团队开发的革命性技术,近期又立新功!这次,它联手马克斯-普朗克研究所,在神经退行性疾病ALS(渐冻症)的治疗领域实现重大突破!
TPP最新研究成果
发表时间:2025年5月14日
期刊:Nat Chem Biol(IF=12.9)
发表单位:马克斯-普朗克研究所Richard J Wheeler教授团队和TPP开发者欧洲分子生物学实验室Mikhail Savitski团队
主要内容:热蛋白质组学(TPP)揭示肌萎缩侧索硬化(ALS)的治疗新靶点
肌萎缩侧索硬化(ALS)是一种致命的神经退行性疾病,目前治疗选择有限。ALS患者中,TDP-43/FUS等蛋白因应激颗粒(SG)异常聚集,像“胶水”一样黏在细胞质里,导致神经元死亡。传统方法难以追踪这些过程,而TPP技术首次像“分子摄像机”一样,捕捉到小分子药物-硫辛酰胺(lipoamide)如何通过调控氧化还原状态,精准“溶解”这些致病团块,并让蛋白“回家”(回到细胞核)恢复功能!
应激颗粒(黄色)像太阳系的星星一样环绕在细胞核(蓝色)周围(来源于网络,侵权删)
样本信息
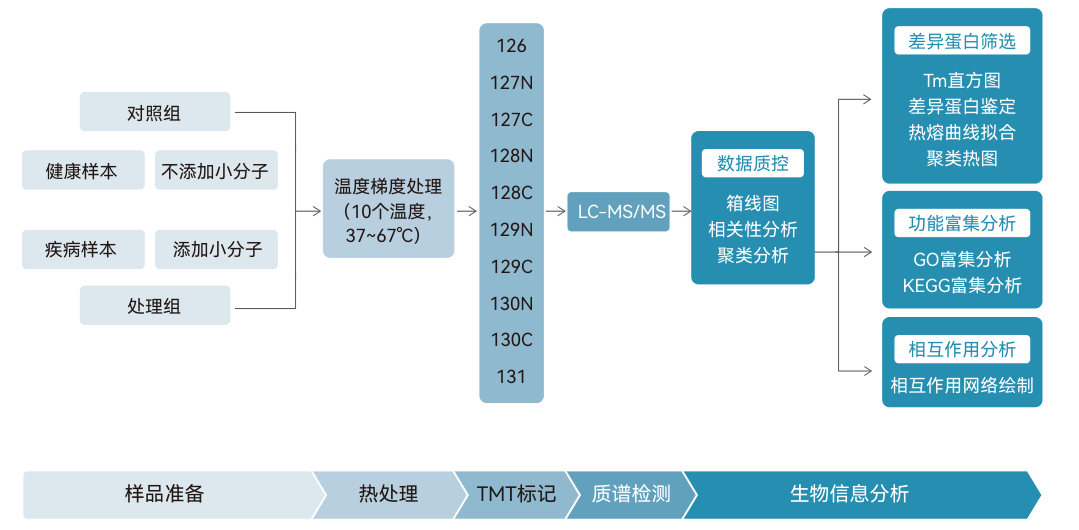
研究使用HeLa细胞进行TPP实验,将样本分为以下4组处理。
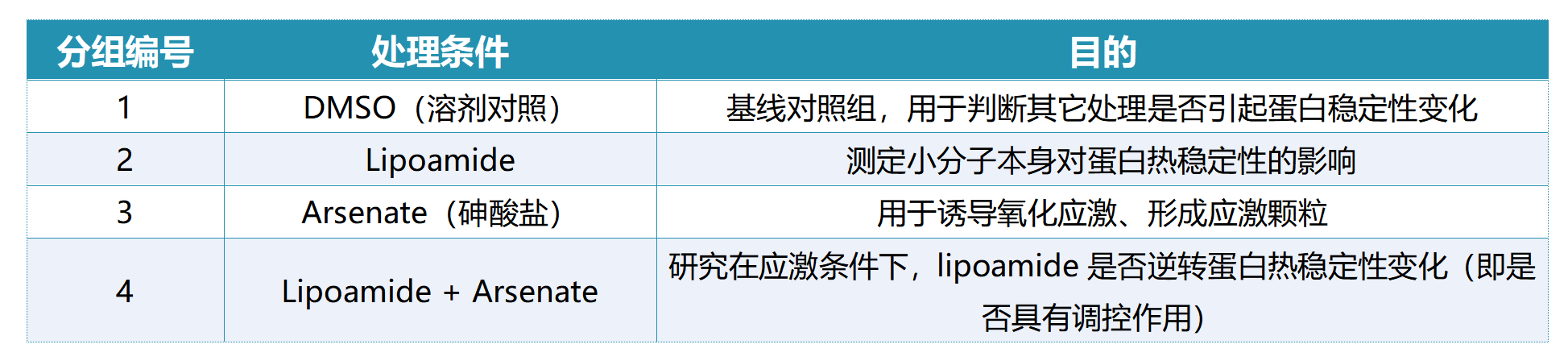
研究亮点
样本创新:在活细胞中直接观测小分子对蛋白热稳定性的动态影响(对照组+应激组全覆盖)
从“细胞垃圾”到治疗靶点:应激颗粒异常固化→困住TDP-43/FUS→神经元死亡。TPP揭示lipoamide可精准溶解致病颗粒,保留正常功能。
老药新用:lipoamide本身是已用于糖尿病的安全药物,临床转化潜力巨大!
研究结果
一、1600种小分子筛选发现:lipoamide精准靶向ALS应激颗粒
使用HeLa细胞系,通过自动化图像分析技术筛选了1600种小分子化合物,评估它们对砷酸盐诱导的应激颗粒形成的影响。最终,lipoamide(硫辛酰胺)凭借出色表现脱颖而出:
预防应激颗粒形成:10µM剂量可显著阻止G3BP1、PABPC1等蛋白形成应激颗粒;
促进应激颗粒解聚:对已形成的应激颗粒也有“解冻”能力,打破ALS中常见的“异常聚集陷阱”;
高特异性:不影响P体、Cajal体或DNA损伤焦点,作用专一、靶向明确。
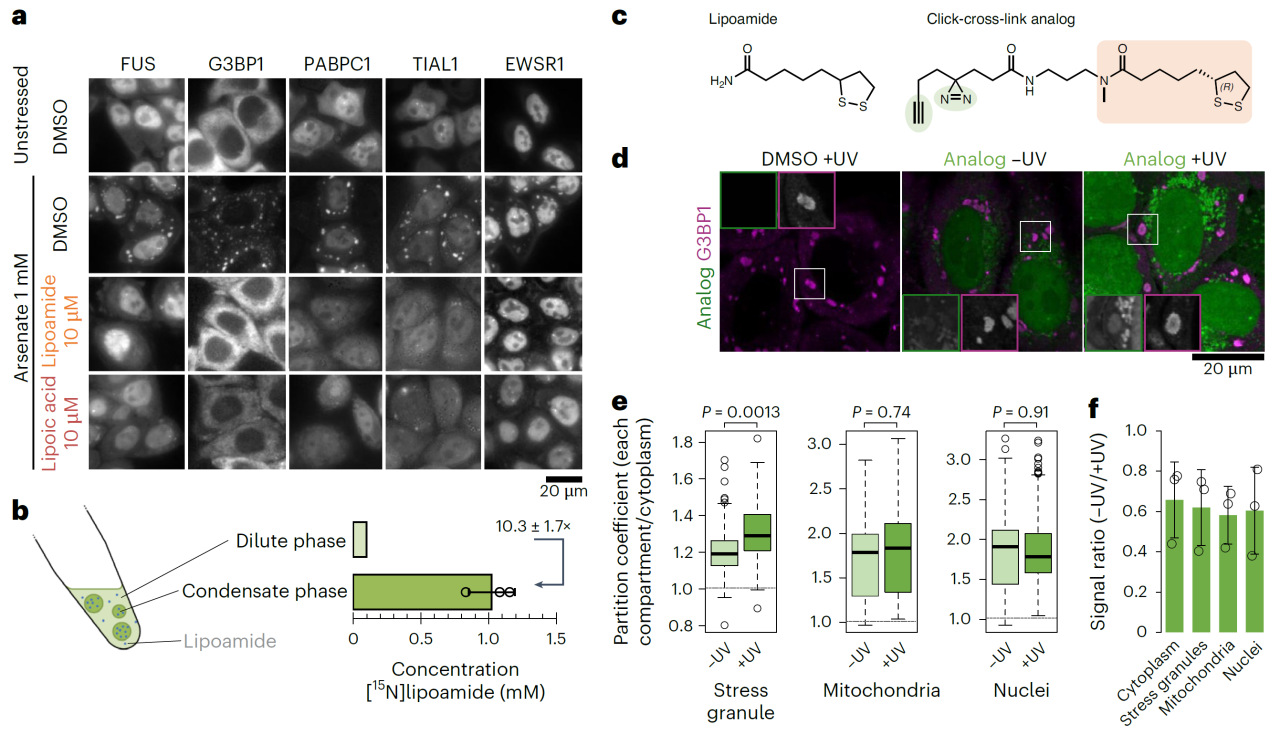
lipoamide通过进入应激颗粒(condensates)来减少细胞质中应激颗粒蛋白的凝聚
二、结构-活性关系研究(SAR)助力药物优化
为了确定硫辛酰胺的活性需要哪些化学特征,作者团队合成了一组lipoamide类似物,并测试了其构效关系(SAR)。结果发现,dithiolane环是活性所必需的,而其他部分(如酰胺基团)的修饰可以提高活性。一些单取代的酰胺类似物显示出比lipoamide更高的活性,部分类似物效力提升5倍以上,表明通过化学修饰可以进一步提高lipoamide的效力。
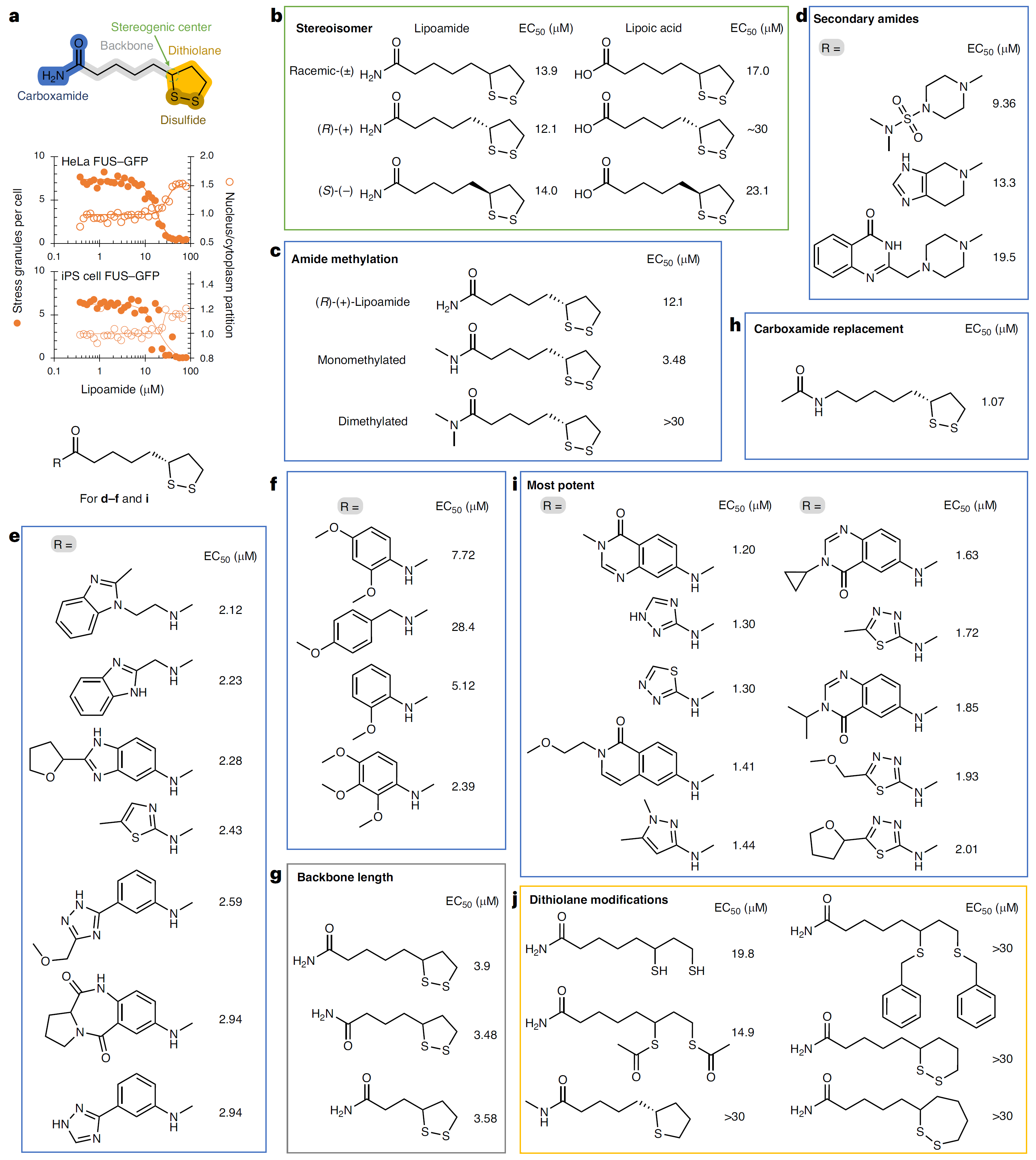
SAR表明硫酰胺活性依赖于dithiolane环
三、热蛋白质组学揭示lipoamide的核心靶点
通过热蛋白质组学分析(TPP),发现lipoamide能够稳定含有内在无序区域(IDRs)的蛋白质,特别是SFPQ和SRSF1,其一旦敲除,就无法发挥药效;这意味着lipoamide的作用是机制明确、靶点清晰的精准干预。
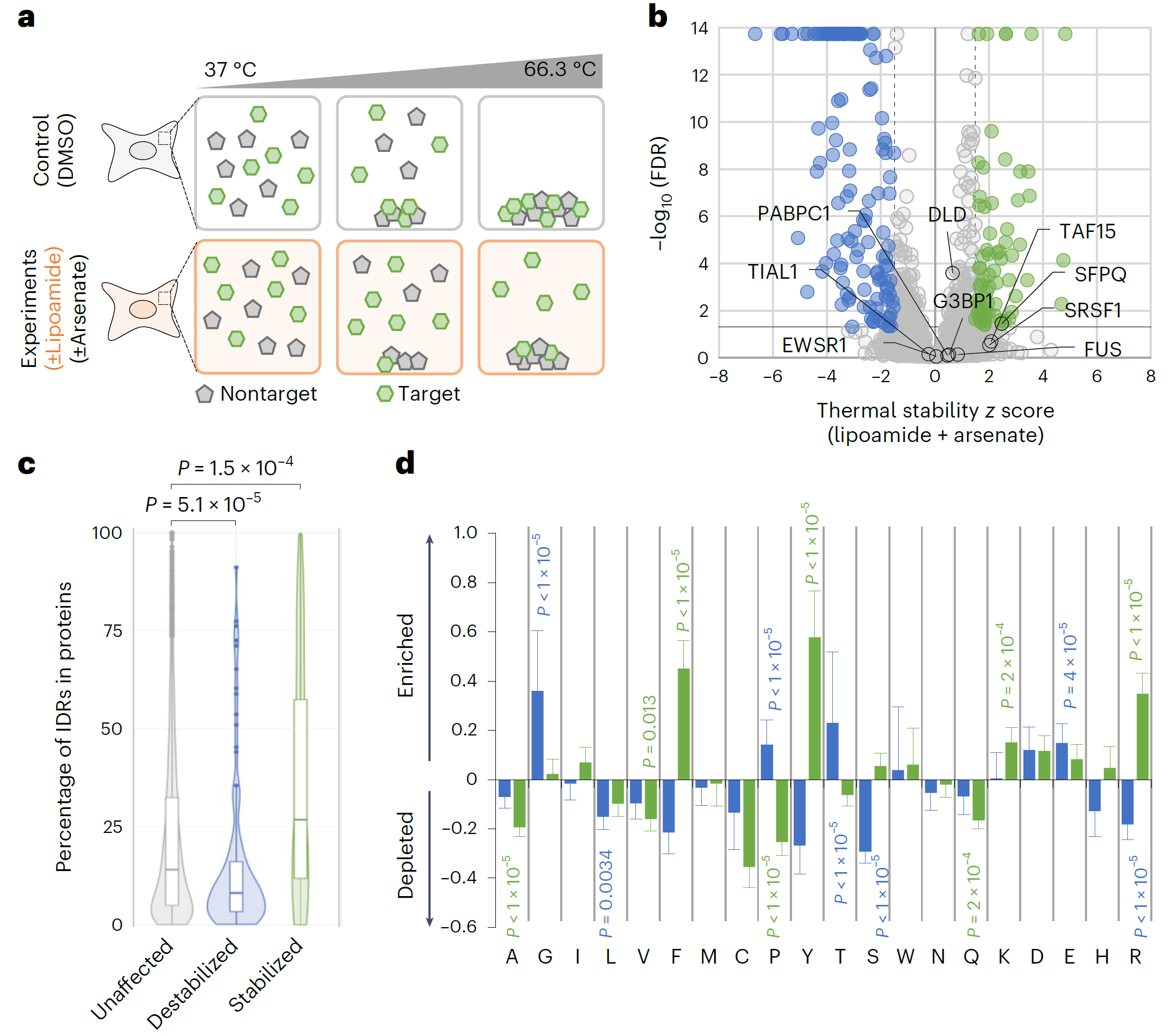
热蛋白质组学揭示lipoamide的作用靶点
四、Lipoamide对核功能的恢复:不仅是位置转移,更是功能复苏
在ALS中,关键蛋白FUS与TDP-43本应驻守在细胞核中,承担DNA修复与RNA剪接调控等核心任务,却因异常应激颗粒被“困”于细胞质,既功能缺失,又毒性堆积。Lipoamide可帮助ALS中异常滞留细胞质的FUS和TDP-43蛋白重新回到细胞核,恢复其DNA修复和转录调控功能,并改善运动神经元中的DNA损伤修复缺陷。这一作用通过调节应激颗粒动态实现,展现了治疗潜力。
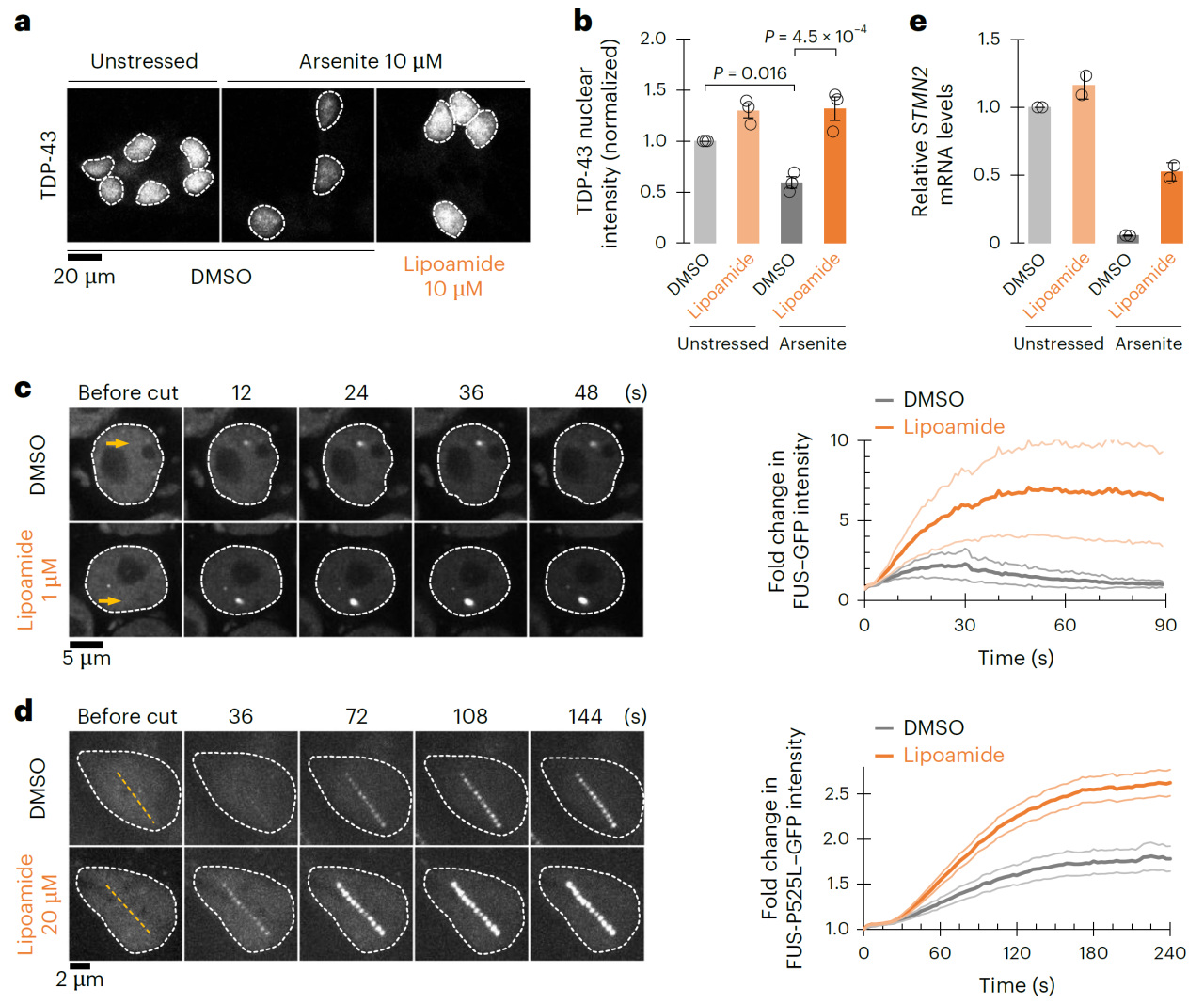
硫酰胺改善FUS和TDP-43的核定位
五、Lipoamide在ALS模型中的治疗效果
细胞模型
在iPS细胞衍生的运动神经元中,lipoamide能够改善由ALS相关突变(如FUS-P525L)引起的神经退行性表型,包括增加神经突的生长和改善轴突运输。这些结果表明,lipoamide在细胞水平上具有改善ALS相关病理的潜力。
动物模型
线虫:lipoic acid能够减少应激颗粒蛋白PAB-1的聚集。这一结果进一步证实了lipoamide在减少蛋白质聚集方面的效果。
果蝇:lipoamide或lipoic acid能够改善由ALS相关突变(如FUS-P525L和TDP-43-M337V)引起的运动缺陷。这些结果表明,lipoamide在动物模型中也具有改善ALS相关病理的潜力。
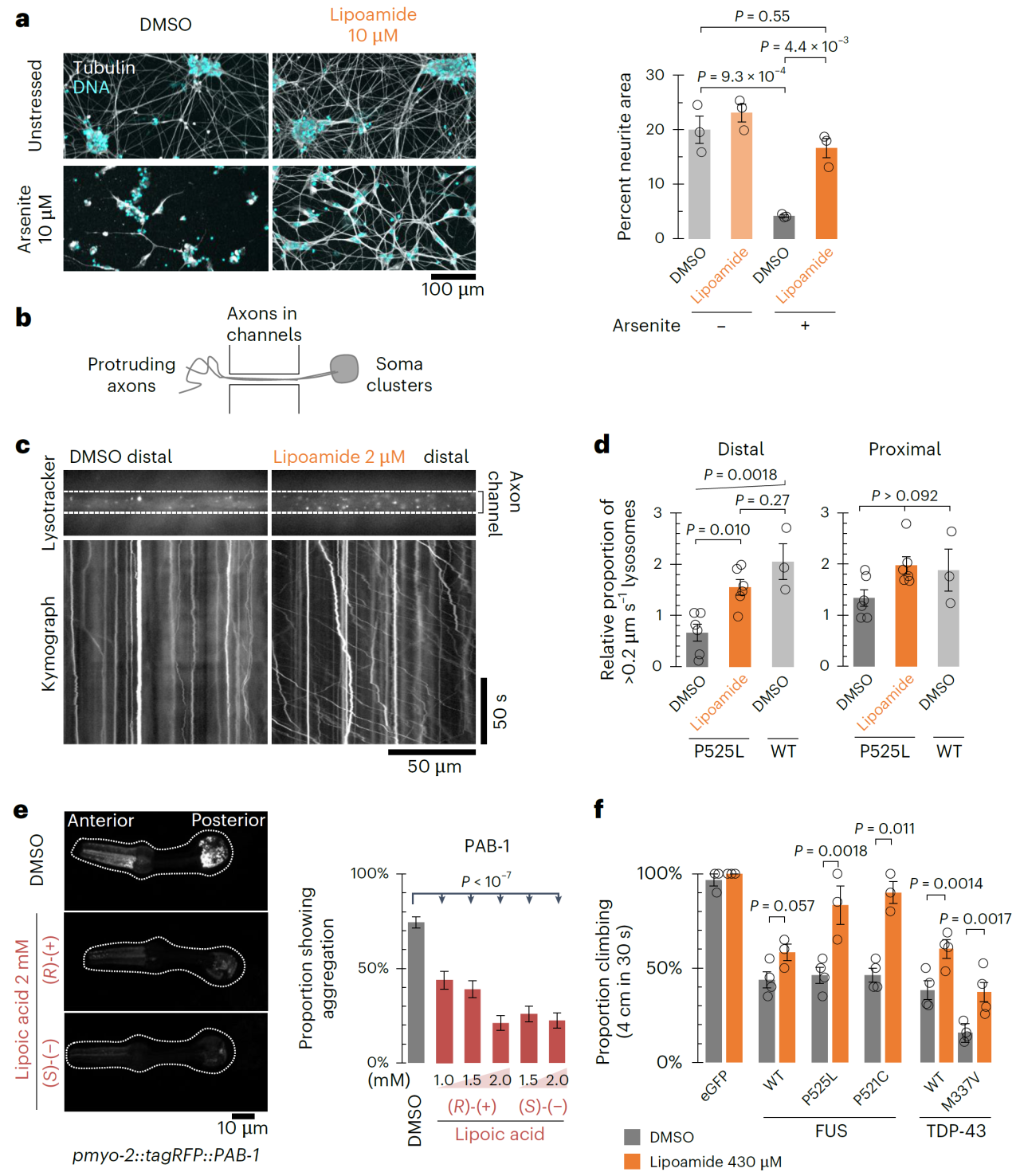
Lipoamide改善ALS iPS细胞衍生的MN和动物疾病模型中的细胞适应性
研究结论
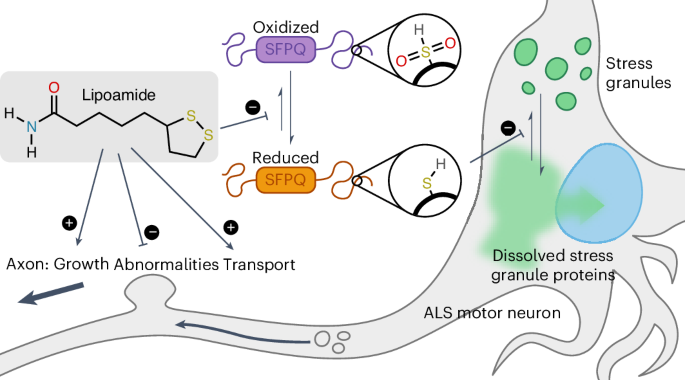
该研究通过热蛋白质组学(TPP)发现硫辛酰胺通过氧化还原调控应激颗粒蛋白SFPQ,特异性溶解应激颗粒并恢复ALS相关蛋白的核功能,从而在细胞和动物模型中缓解ALS病理表型。其良好的耐受性和已有临床应用基础(如糖尿病神经病变)为其作为ALS治疗候选分子提供了潜力。
青莲百奥热蛋白质组学解决方案
青莲百奥与TPP的渊源起于2019年
国内首家提供TPP药物靶点服务[2]
国内首家与客户合作发表研究成果实现转化[2]
5年发展积累近百个项目经验
青莲百奥不断创新,推出升级服务,致力于将先进技术转化为具有实际价值的成果。青莲百奥始终与客户携手前行,共同探索和发展药靶研究技术。

参考文献
[1] UECHI H, SRIDHARAN S, NIJSSEN J, et al. Small-molecule dissolution of stress granules by redox modulation benefits ALS models [J]. Nature Chemical Biology, 2025.
[2] HU C, ZHANG J, CUI R, et al. The enhancement effect of small molecule Lyb24 reveals AzoR as a novel target of polymyxin B [J]. Biomedicine & Pharmacotherapy, 2023.