免疫原性细胞死亡(ICD)是一种能够激活宿主持久性抗肿瘤免疫应答的调控性细胞死亡方式。其核心特征表现为通过释放损伤相关分子模式(DAMPs)吸引免疫细胞攻击肿瘤,因此成为癌症治疗领域的研究热点。然而,目前大多数化疗药物主要通过直接杀伤癌细胞来发挥作用,而如何有效激活机体的抗癌免疫反应仍然是一个重大挑战。尽管一些ICD诱导剂已被证实能够通过自噬途径触发ICD,但负责自噬介导的ICD的具体分子靶点尚未阐明。
2025年4月25日,广西师范大学化学与药学学院黄克斌/梁宏教授团队在Journal of the American Chemical Society (IF 14.4) 在线发表了题为“Oxoisoaporphine Alkaloid Iridium(III) Derivative: An Immunogenic Cell Death Inducer That Engages the Autophagy-Dependent Regulator Cathepsin D”的研究论文。该研究通过热蛋白质组学(TPP)技术鉴定新型的铱(III)配合物2a的主要靶蛋白,发现该配合物与溶酶体蛋白酶组织蛋白酶D(Cat D)相互作用,并通过抑制Cat D活性,激活LKB1-AMPK-ULK1信号轴,进而诱导自噬依赖性ICD,并在体内外展现出显著的抗肿瘤效果。这一发现不仅为自噬介导的ICD提供了新的见解,也为基于金属配合物的新型抗癌疗法开发奠定了基础。

研究材料
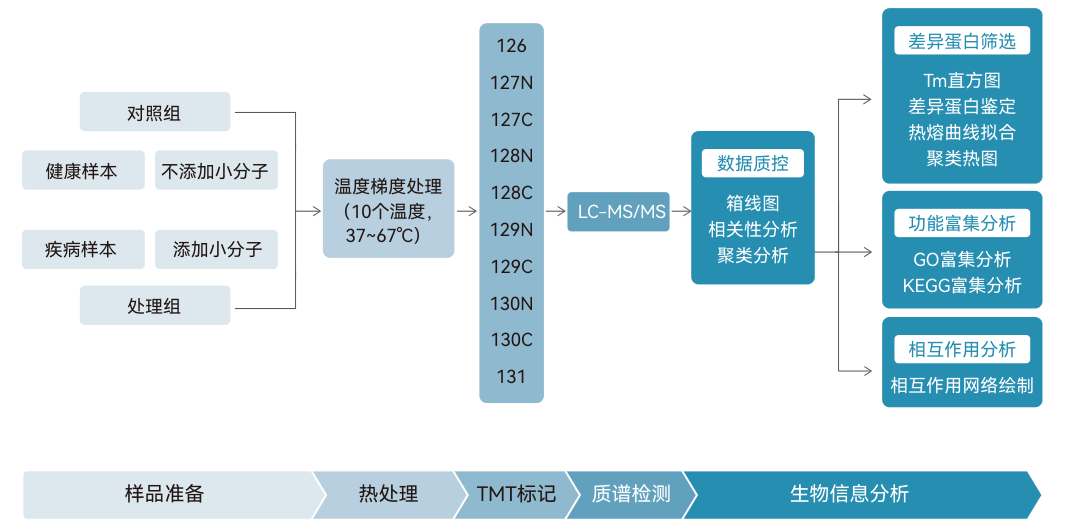
小鼠三阴性乳腺癌(TNBC)细胞系(4T1)(2a孵育组vs对照组,n=2)分别进行温度梯度(37℃、42℃、47℃、51℃、55℃、59℃、63℃、67℃)处理
研究方法
热蛋白质组学(TPP)技术
文章亮点
创新型ICD诱导剂2a:引入氧代异阿朴啡生物碱(La),新型铱(III)配合物2a展现出优异的细胞毒性和ICD诱导活性;
发现关键靶点CatD:首次利用热蛋白组学技术揭示CatD是2a诱导自噬依赖性ICD的主要作用靶点;
自噬依赖性ICD新机制:2a通过抑制CatD激活相关信号通路,揭示了Cat D在自噬依赖性ICD中的关键作用。
重要成果
一、新型ICD诱导剂的开发与功能评价
作者此前报道了一种环金属化铱(III)配合物(1a),其通过BiP蛋白诱导ICD,本研究在在保留1a的N-杂环卡宾(NHC)配体和铱(III)中心的基础上,将苯基吡啶配体替换为氧代异阿朴啡生物碱(La),以增强π共轭效应和生物活性,以此设计并合成了一种新型铱(III)配合物2a。体外细胞毒性实验发现2a对多种TNBC细胞系均表现出显著抑制作用。接着,作者检测了ICD关键分子标志物(CRT暴露、ATP和HMGB1释放),证实2a在TNBC细胞中具有显著的ICD诱导能力,且其活性优于1a及对照化合物(图1)。
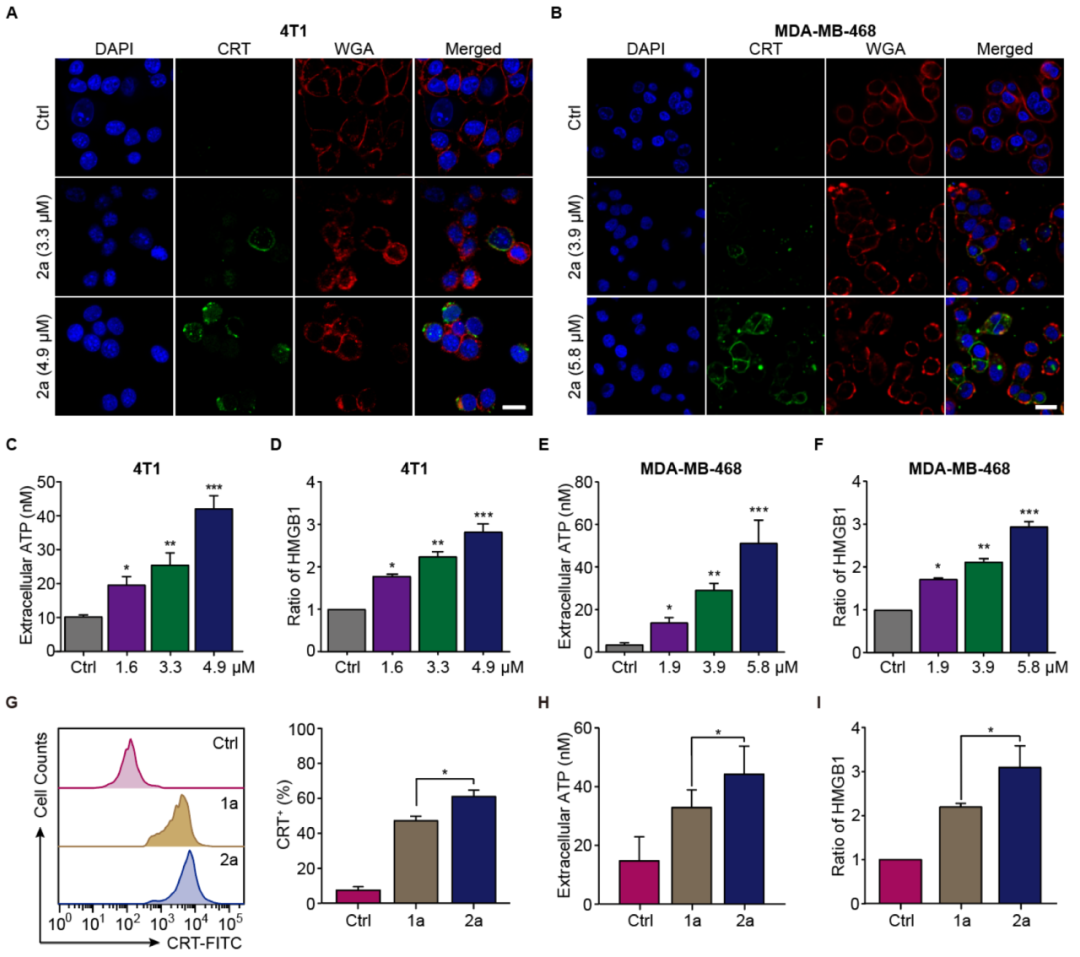
图1:TNBC细胞中2a诱导ICD相关DAMPs
二、体内实验表明2a诱导ICD触发抗肿瘤免疫反应
研究人员在免疫健全的BALB/c小鼠中进行的体内疫苗接种实验评估2a诱导ICD介导的抗肿瘤免疫效果。结果显示,2a处理的癌细胞能够显著延迟肿瘤的再次生长,与顺铂(OXA)相比,2a组中有更高比例的小鼠保持无肿瘤状态,并且在实验结束时,2a组小鼠的肿瘤体积明显小于对照组和OXA组(图2)。此外,所有小鼠在整个实验过程中体重保持稳定,表明2a在有效抑制肿瘤的同时,对小鼠的整体健康状况没有显著负面影响。
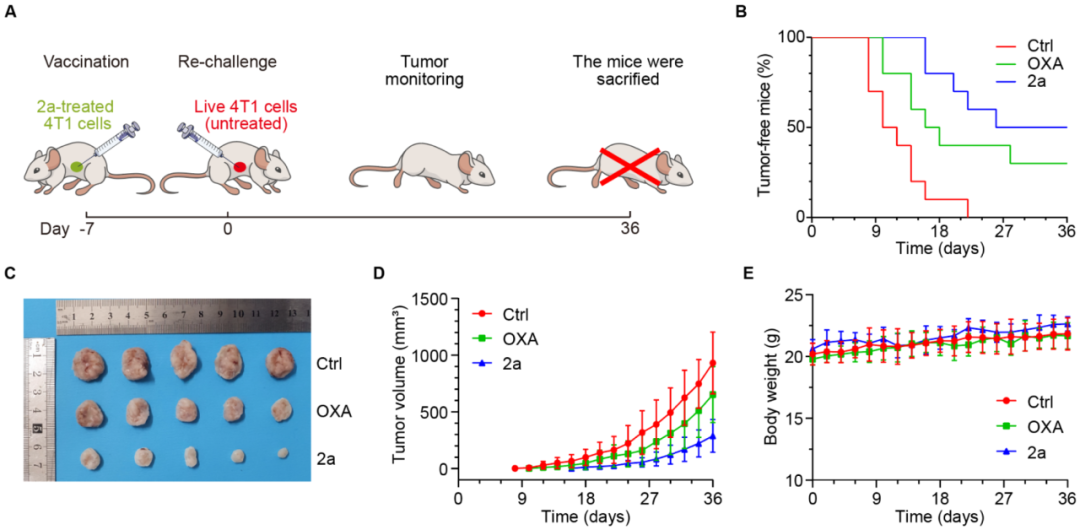
图2:体内实验揭示2a抗肿瘤免疫
为了深入了解体内免疫反应与肿瘤进展之间的关系,研究人员使用质谱流式细胞术分析了不同处理组小鼠体内多种免疫细胞的分布差异。结果显示,2a处理组的小鼠在肿瘤组织、脾脏、淋巴结和外周血液中均显示出更高的CD8+ T细胞激活水平以及更强的细胞毒性,促进了组织驻留记忆T细胞形成、同时显著抑制调节性T细胞(Treg)浸润。总而言之,2a通过诱导ICD重塑肿瘤免疫微环境,触发了强大的抗肿瘤免疫反应,其效果优于传统的ICD诱导剂OXA。
三、2a与抗PD1联合治疗协同抗肿瘤
研究人员进一步评估了2a在携带4T1肿瘤的BALB/c小鼠模型中的治疗效果。小鼠分别接受OXA、抗PD-1、2a或2a与抗PD-1联合治疗。结果显示,2a表现出显著的抗肿瘤活性,其中2a与抗PD-1联合使用显著增强了抗肿瘤效果,其肿瘤生长抑制率(IRT)高于任何单药治疗组(图3C),表明两者之间存在协同作用。联合治疗组的肿瘤体积最小(图3D),进一步证实了2a与抗PD-1的协同抗肿瘤作用。
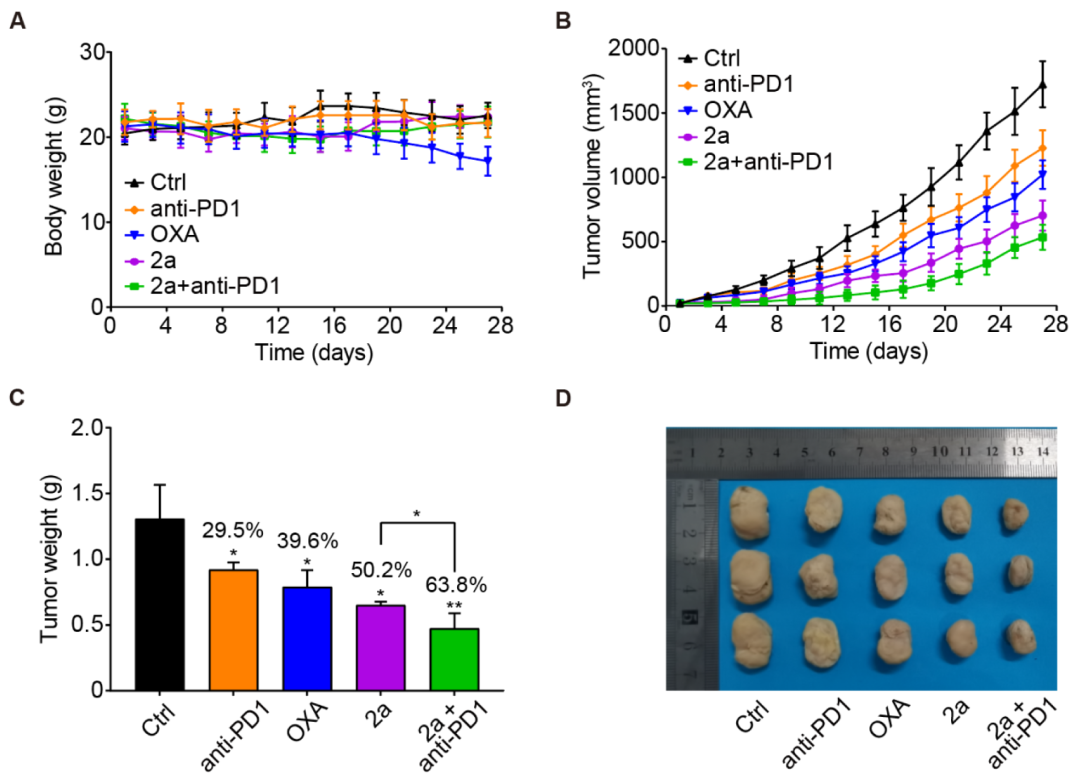
图3:2a与抗PD1联合治疗协同抗肿瘤
四、热蛋白质组分析2a的主要靶蛋白
为了深入解析2a诱导ICD的分子机制,作者采用热蛋白质组分析(TPP)方法,将4T1细胞裂解液与2a孵育,并进行温度梯度处理结合质谱分析确定其热稳定性增加或降低的潜在靶蛋白,包括Cat D、PRDX1、MCM5和COPG1(图4C)。通过细胞热转移实验(CETSA)和等温剂量-反应分析(ITDR)验证了Cat D为潜在的靶蛋白(图4E-F)。2a与Cat D分子对接结果(图4K-L)进一步证明2a能够与Cat D的活性口袋中的关键氨基酸残基相互作用,引起蛋白构象变化。
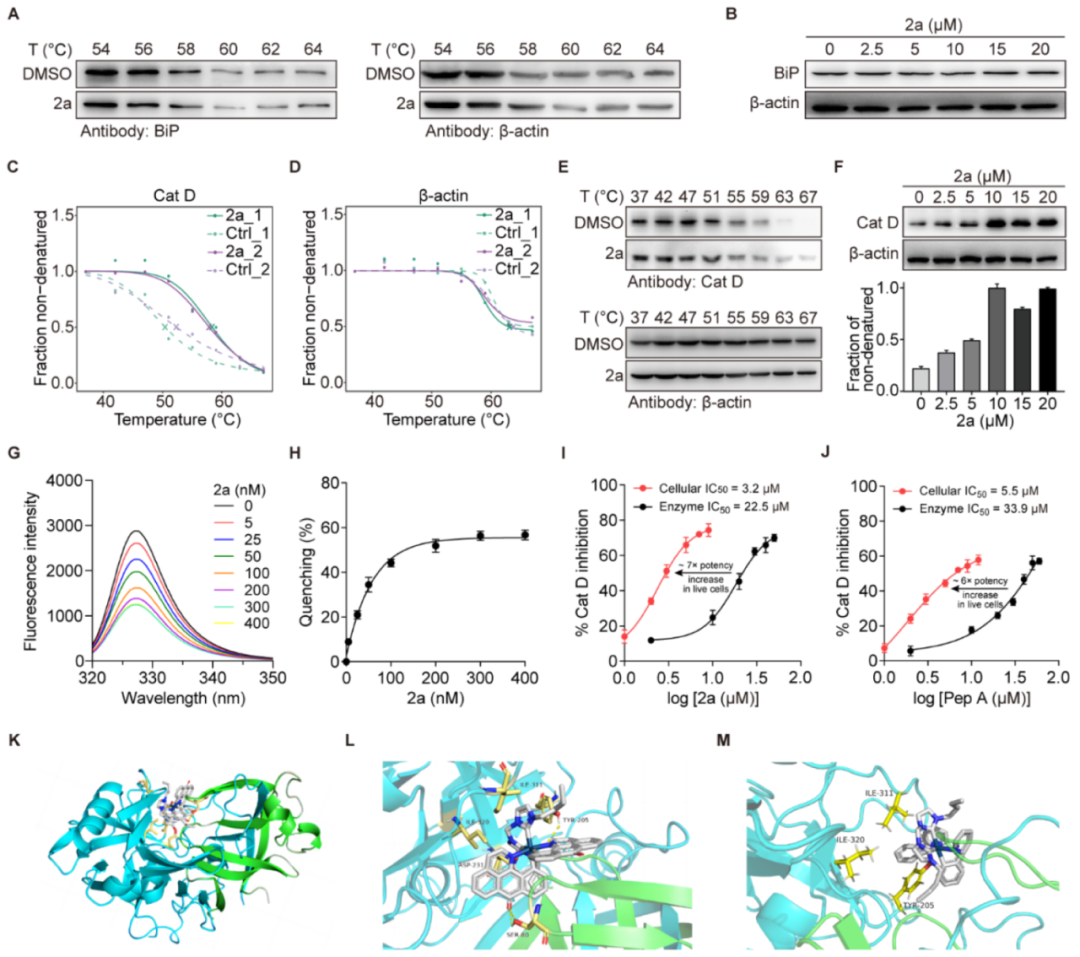
图4:2a与Cat D的相互作用研究
五、2a通过抑制Cat D诱导自噬
研究人员随后证实了2a能够诱导自噬。2a处理的细胞显示出明显的自噬小体增加(图5A),同时,用自噬抑制剂3-MA(3-甲基腺嘌呤)处理细胞后,2a 处理细胞的存活率呈剂量依赖性增加(图5C)。正如预期,2a通过下调p-mTOR和p-ULK1(S757)并上调p-AMPK触发自噬,自噬标志蛋白LC3-II水平也以时间依赖的方式增加(图5D)。而Cat D抑制剂pepstatin A和myricitrin也呈现类似效应,这些结果表明2a具有独特的CatD-自噬通路激活机制。总之,2a通过抑制Cat D激活LKB1-AMPK-ULK1信号轴,进而诱导自噬依赖性细胞死亡。
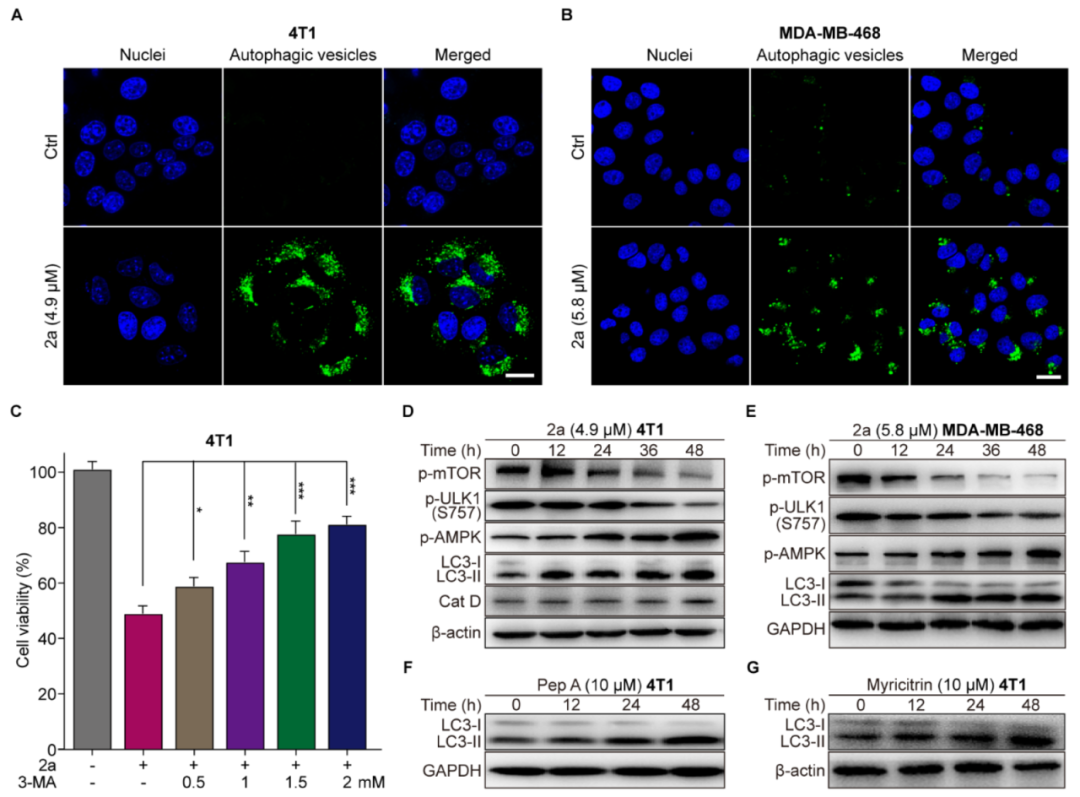
图5:2a诱导的自噬效应
研究结论
综上所述,研究人员设计了一种新型的铱(III)配合物2a,通过热蛋白质组学技术发现2a的靶蛋白CatD,其作用机制通过抑制CatD激活LKB1-AMPK-ULK1信号通路,进而诱导自噬依赖性ICD,并证实了Cat D抑制在自噬依赖性ICD诱导中的普遍性,为开发新型ICD诱导剂提供了新的思路。
青莲百奥与TPP的渊源起于2019年
国内首家提供TPP药物靶点服务[1]
国内首家与客户合作发表研究成果实现转化[1]
5年发展积累近百个项目经验
青莲百奥不断创新,推出升级服务,致力于将先进技术转化为具有实际价值的成果。青莲百奥始终与客户携手前行,共同探索和发展药靶研究技术。

参考文献
[1] HU C, ZHANG J, CUI R, et al. The enhancement effect of small molecule Lyb24 reveals AzoR as a novel target of polymyxin B [J]. Biomedicine & Pharmacotherapy, 2023.