食管鳞状细胞癌(ESCC)是全球常见的上消化道恶性肿瘤,其进展从食管炎(ESO)开始,经过轻度、中度、重度不典型增生(MID、MOD、SED)和原位癌(CIS)阶段,最终发展为浸润癌。当前临床策略中,低级别上皮内瘤变(LGIN,含MID和MOD)患者通常不采取手术治疗,而高级别上皮内肿瘤(HGIN,含SED和CIS)患者则需内镜黏膜切除治疗。但该策略被认为对LGIN处理不足,对HGIN处理过度,因此需要更科学的分层系统,为临床诊疗提供新的建议。
近日,上海交通大学公共卫生学院王慧/李晓光/李辰团队合作在国际知名综合性期刊Advanced Science(IF 14.1)上发表了题为“Spatio-Temporal Proteomic Landscape Reveals Early Warning Signals of Esophageal Squamous Cell Carcinoma Progression”的研究论文。研究通过基于激光捕获显微切割(LCM)技术的空间分辨蛋白质组学方法构建了ESCC进展的全面时空图谱,揭示了ESCC早期发生进展过程中的关键蛋白质变化,并发现MOD阶段可作为临床关键节点,同时提出了靶向PARP1-TP63-GBP6轴的早期干预新策略,为ESCC的早期诊断、随访监测及早期干预提供了重要科学依据。
研究结果
ESCC进展的时空蛋白质组学研究设计
研究收集了ESCC进展5个关键阶段ESO、MID、MOD、SED、ESCC的临床样本进行了时空蛋白质组学分析。通过LCM技术,从54名患者的71个活检样本中精确采集了上皮病变组织(L组)和相邻非病变组织(N组),进行空间蛋白质组学分析,以揭示ESCC进展的分子机制和早期预警生物标志物。
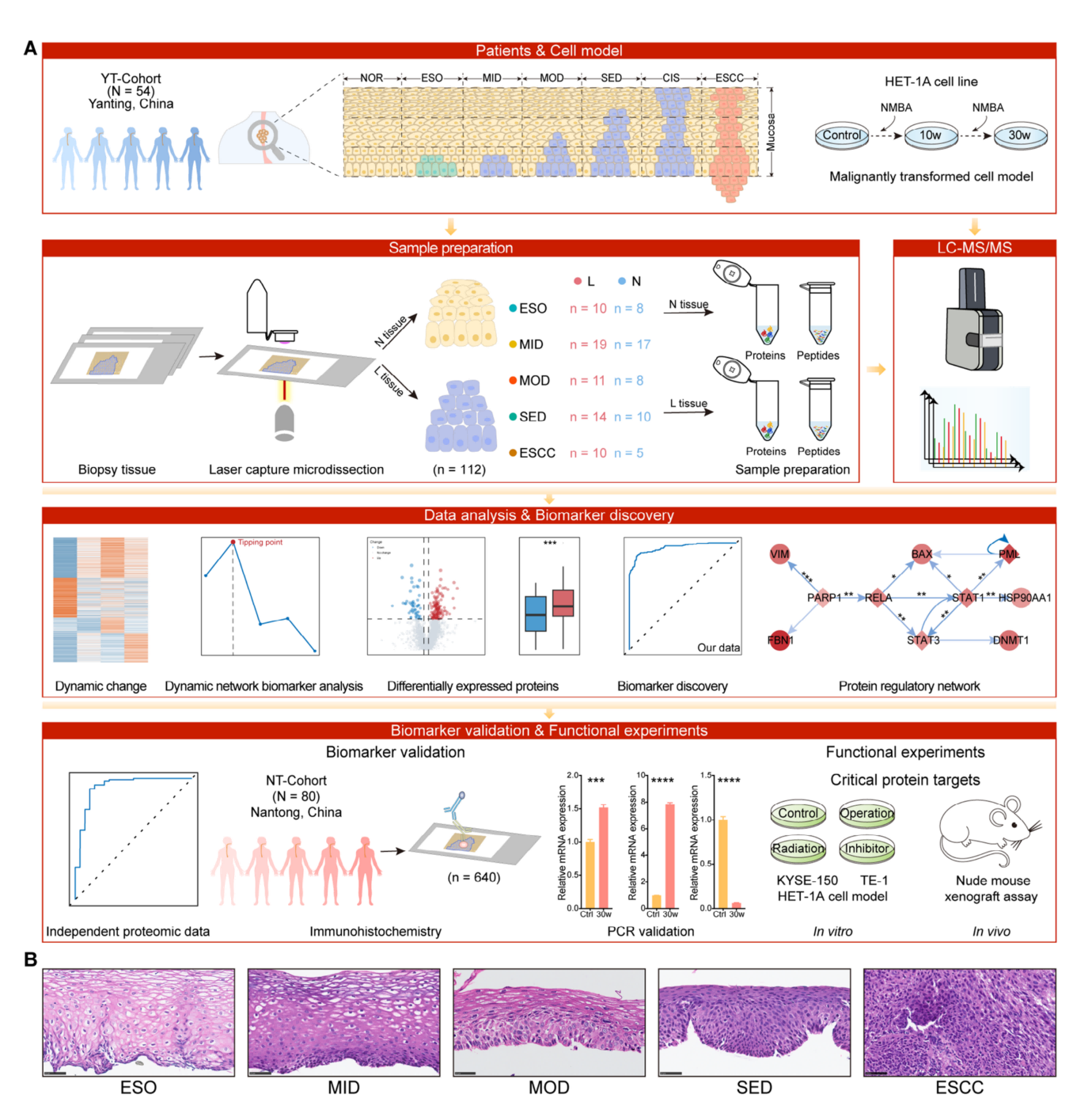
图1. ESCC进展的时空蛋白质组学研究设计
空间蛋白质组学解析ESCC进展中的差异图谱
空间蛋白质组数据显示,L组和N组中分别鉴定出151和155个食管特异性蛋白,L组中正常食管功能相关分子显著下调。功能分析发现,随着ESCC的进展,致癌相关通路在L组中被激活,如RNA代谢、细胞周期及上皮-间质转化等;而参与食管主要功能的蛋白质则缺失。研究通过空间蛋白质组描绘ESCC各个阶段的蛋白质谱,发现了L组和N组之间的显著差异。
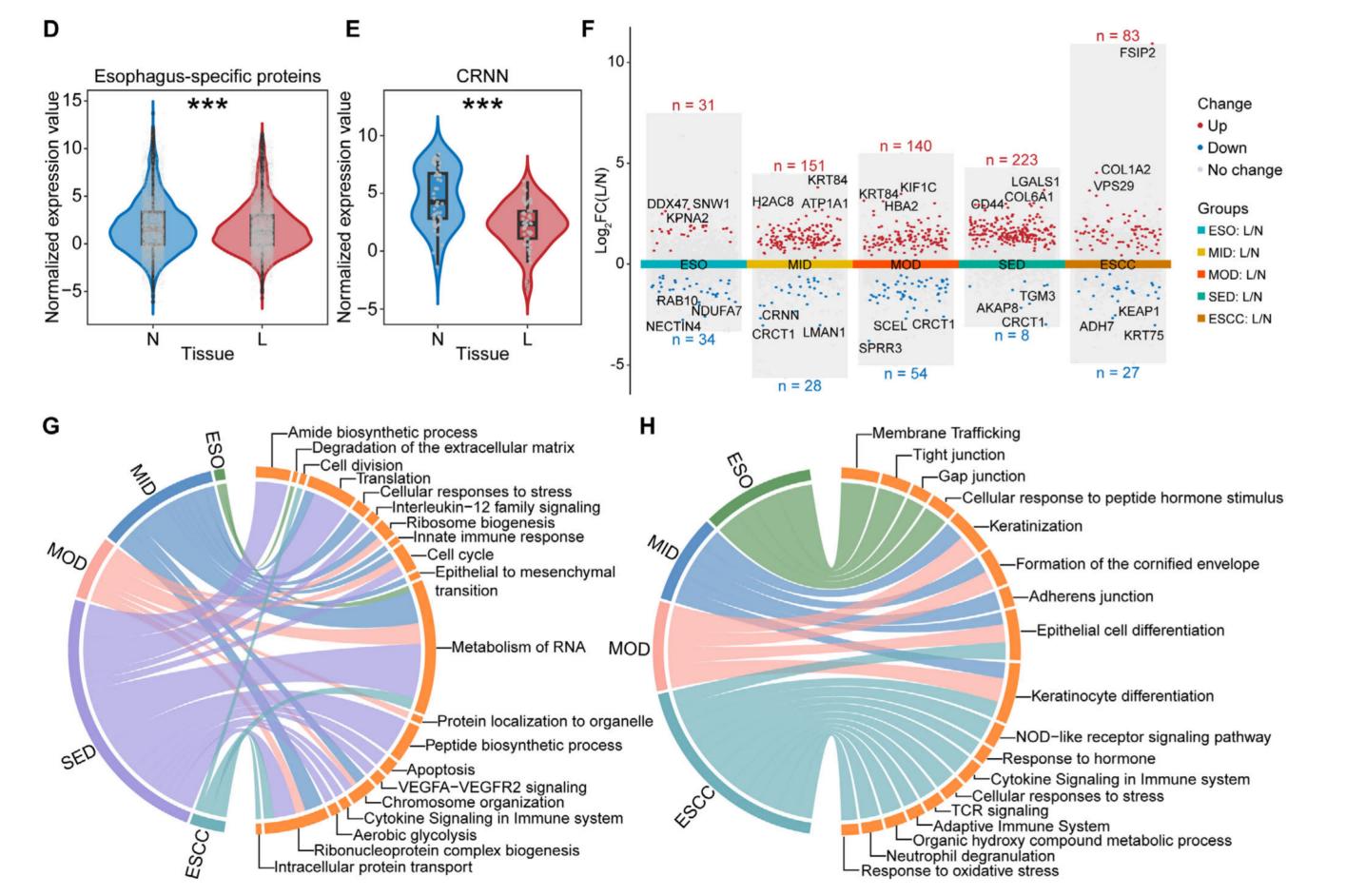
图2. ESCC进展过程中L组和N组间的蛋白质组学差异
时空组学分析ESCC进展过程中的蛋白质动态变化与关键节点
文章通过Mfuzz聚类分析了L组和N组中ESCC各阶段的蛋白表达趋势。L组中,参与肿瘤发生、代谢及免疫的通路整体呈上升趋势,于MOD阶段达峰值,而食管正常功能相关通路则逐渐下调。N组趋势与L组基本相反,其翻译和免疫相关通路也在MOD阶段达到峰值。
随后,作者采用DNB分析ESCC进展的蛋白动态变化及蛋白互作,并通过iTALK分析配体-受体介导的细胞间信号。结果显示,MOD组拥有最多的阶段特异性蛋白,是ESCC从相对良性状态向恶性状态过渡的关键节点,其中上皮-间质转化(EMT)通路发挥关键作用。
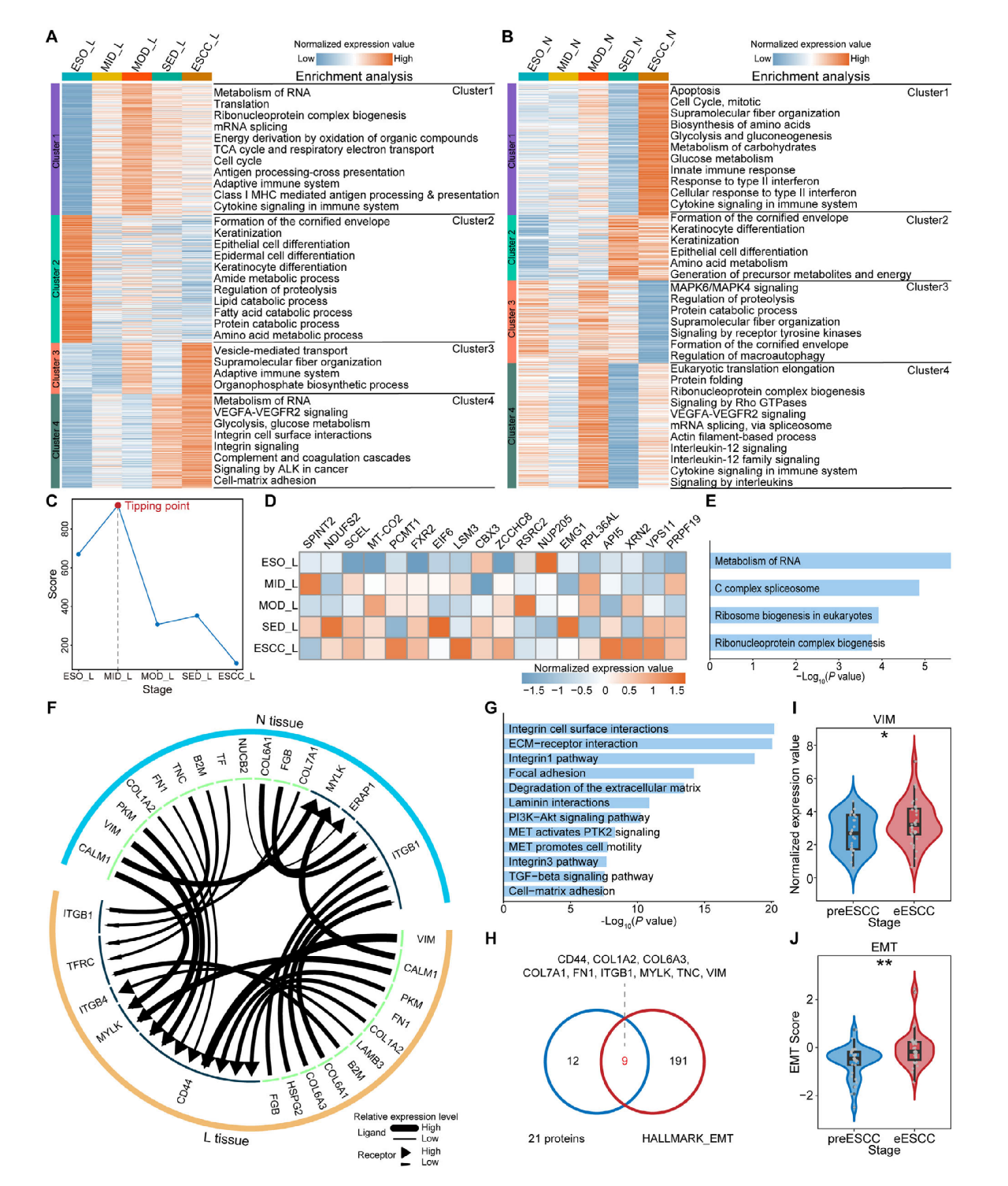
图3. ESCC进展过程中的蛋白质动态变化与关键节点
preESCC阶段与eESCC阶段的蛋白质组差异
文章将ESO与MID合并为preESCC(癌前阶段),MOD、SED与ESCC合并为eESCC(癌早期阶段)。差异分析发现,eESCC中上调的蛋白质富集于RNA代谢及核糖核蛋白复合物合成,下调的蛋白质则参与氨基酸代谢和适应性免疫系统。此外,TGF‐β信号和免疫相关通路促进ESCC进展,而高表达的PARP1位于网络上游,调控下游靶点。因此,PARP1与DNA修复及EMT密切相关,是早期干预的潜在靶点。
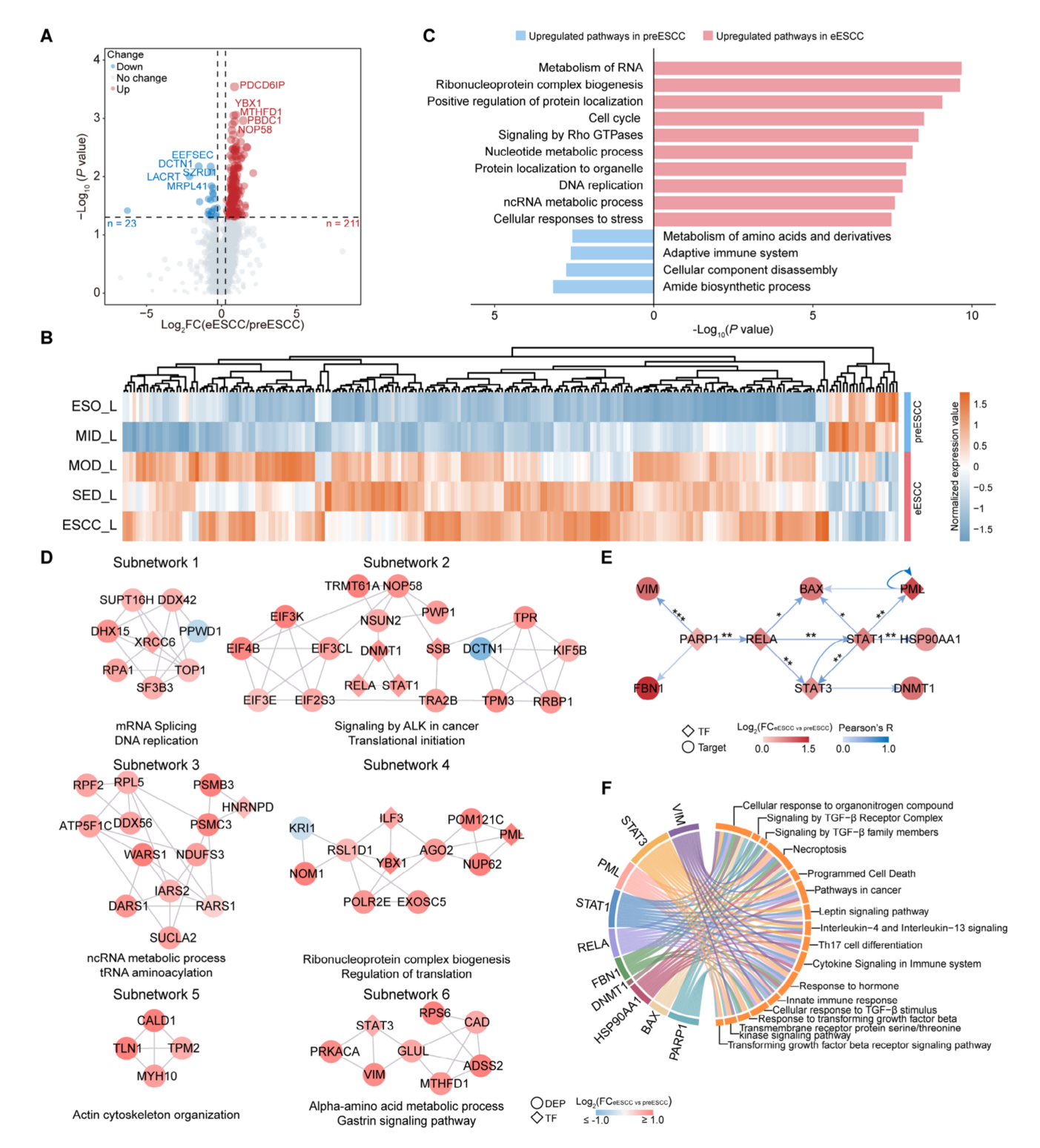
图4. preESCC阶段与eESCC阶段的蛋白质组差异
ESCC进展的早期预警生物标志物
文章开发了机器学习模型,以识别ESCC的早期生物标志物。最终确定了七个分子特征的SVM模型,在区分eESCC与preESCC方面,以及两个独立队列中的正常和ESCC患者,都取得了良好表现(AUC = 0.956、0.930、0.903)。通过功能分析文章构建了一个包含富含细胞迁移和运动性、EMT和PI3K-Akt-mTOR信号的蛋白质的PPI网络,强调了其中EMT的关键作用。
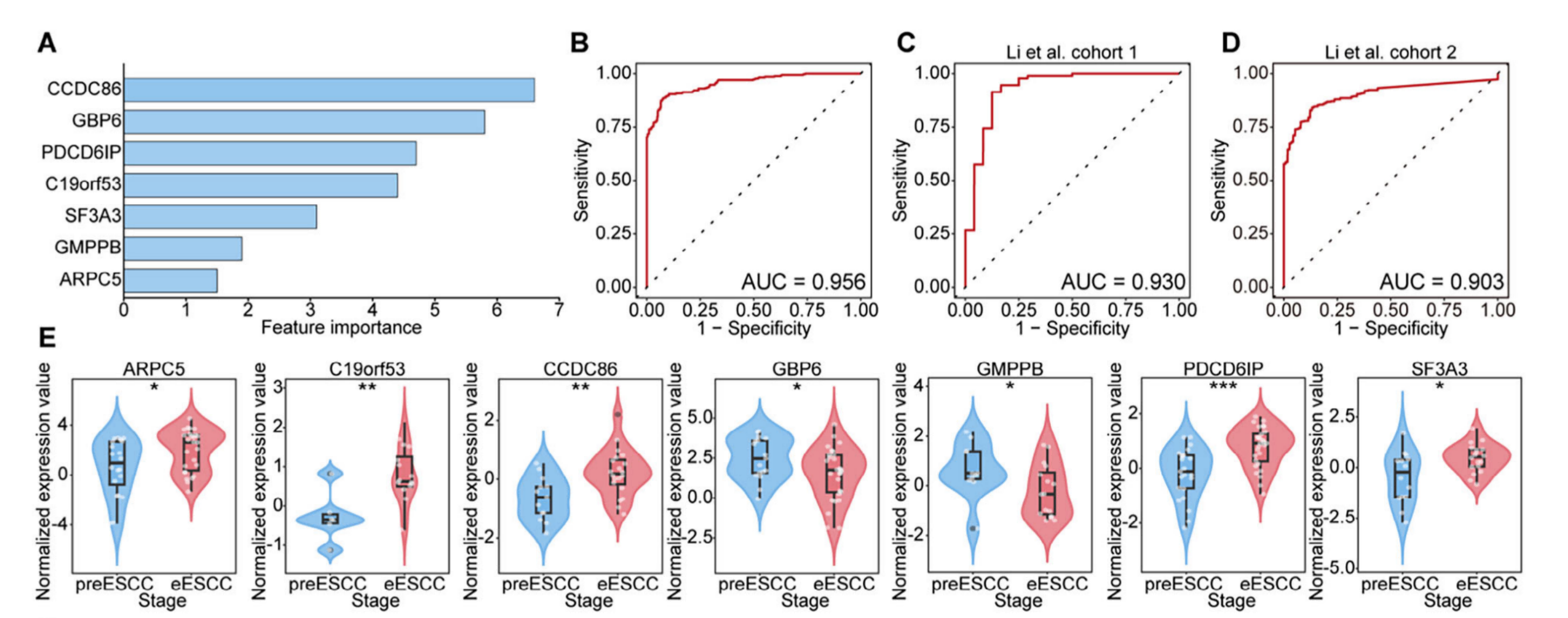
图5. 机器学习识别ESCC的早期预警生物标志物
GBP6的作用机制以及作为早期干预靶点的潜力
接下来,文章基于特征重要性排名及HPA中食管特异性蛋白,从预警生物标志物中筛选出ESCC早期干预靶点,并锁定GBP6作为目标。细胞模型显示,GBP6过表达显著抑制食管上皮细胞恶性转化及ESCC细胞的增殖、迁移与侵袭,而敲低GBP6则促进这些过程。功能分析表明,GBP6的逐渐缺失可能通过加速细胞周期和诱导EMT促进ESCC进展。
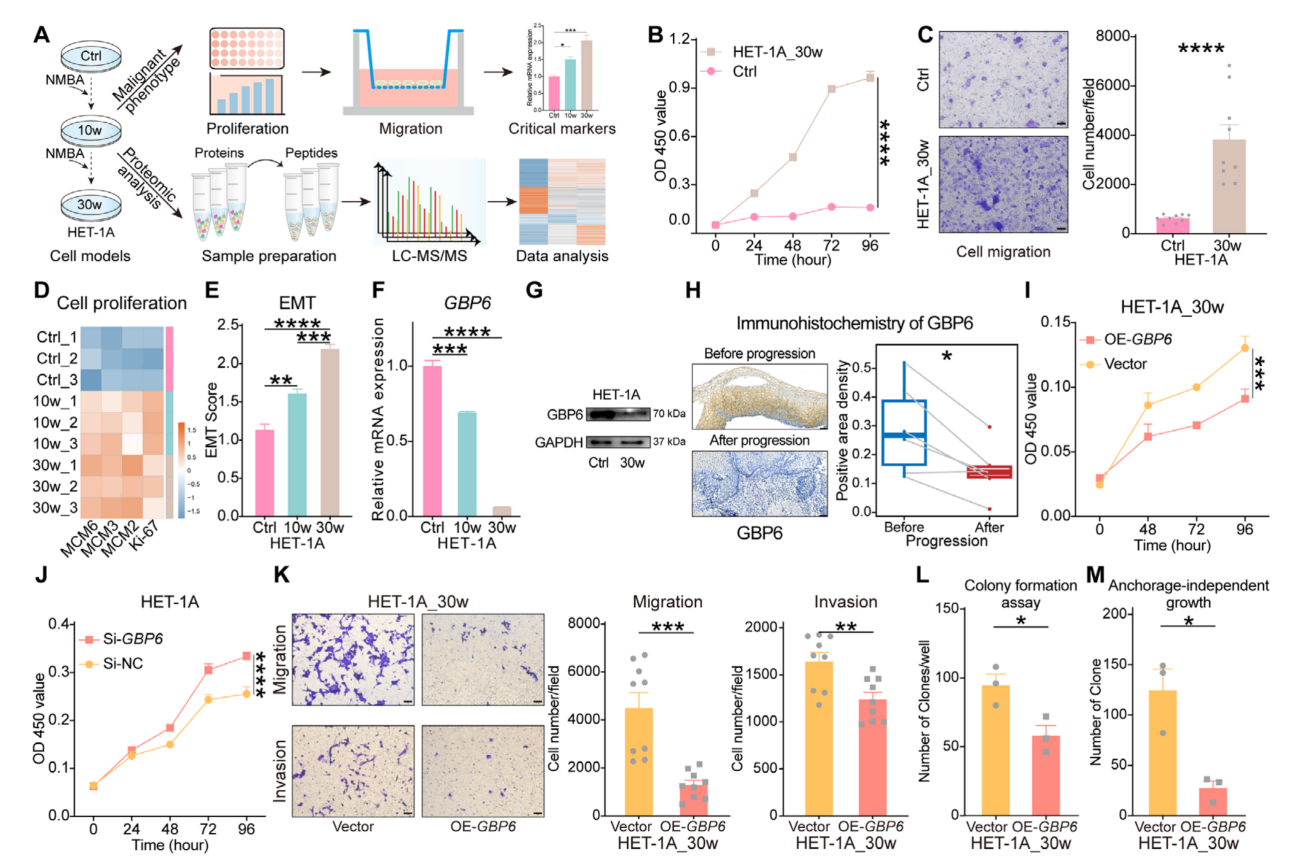
图6. GBP6的逐渐缺失通过加速细胞周期和诱导EMT来驱动ESCC的发育
随后文章探讨了ESCC进展中GBP6逐渐缺失的原因。研究发现,PARP1在ESCC进展过程中逐渐上调,在肿瘤组织中尤为显著。体外与体内实验证实,抑制PARP1可有效逆转DNA损伤引起的GBP6缺失,从而抑制ESCC进展。而转录因子TP63是GBP6的潜在抑制因子,并参与DNA损伤相关PARP1通路的下游信号传导。综上,文章提出一条新的机制轴:抑制PARP1可下调GBP6的TP63,从而挽救GBP6表达缺失,抑制ESCC肿瘤进展。
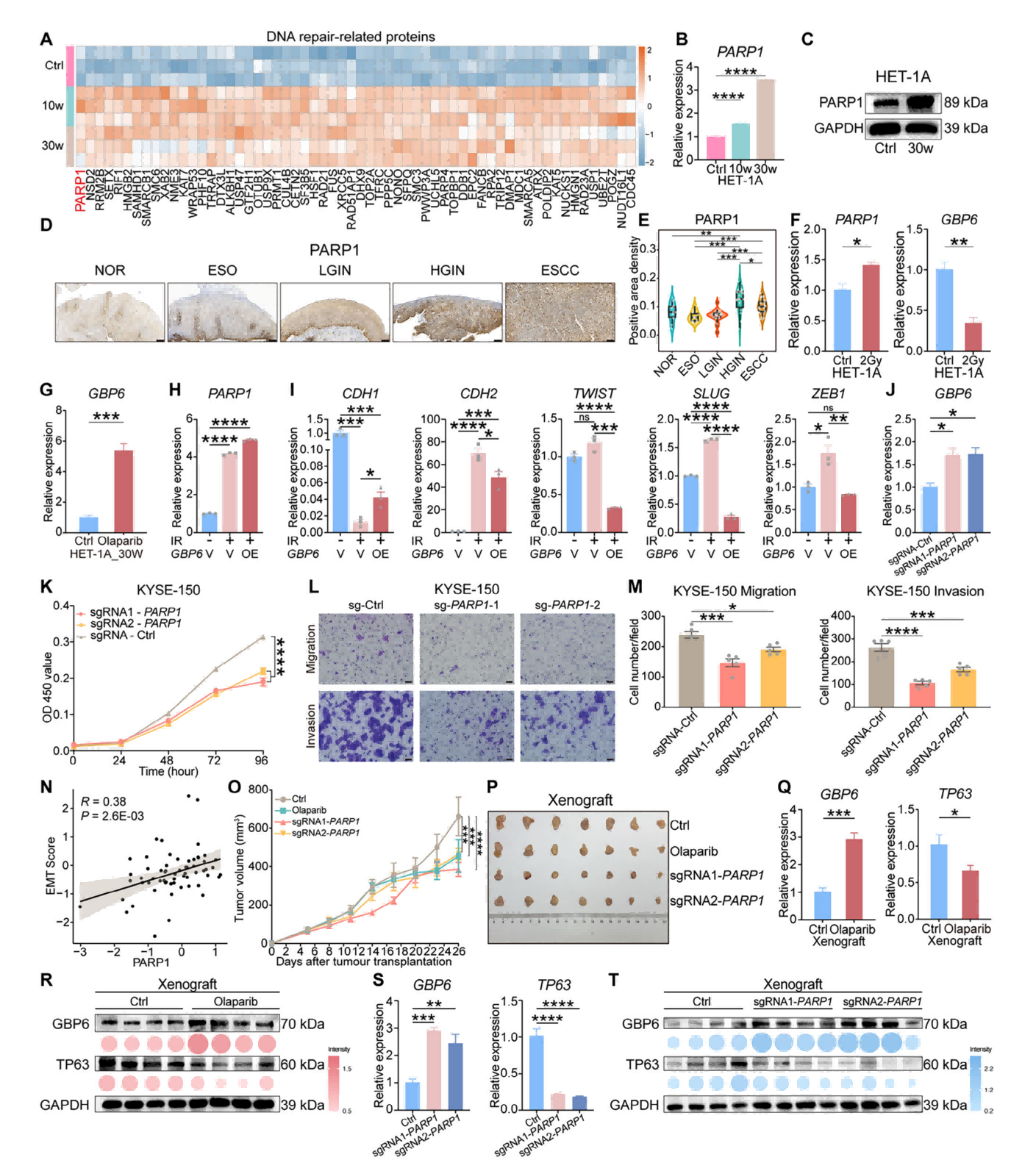
图7. 抑制PARP1可挽救由DNA损伤引起的GBP6缺失
文章结论
本文构建了一个精确且无偏的空间蛋白质组学图谱,涵盖ESCC从ESO、MID、MOD和SED到ESCC的整个进程。首次系统性地界定了ESCC各阶段进展相关的动态蛋白质表达,揭示了食管上皮功能显著丧失及致癌通路激活。文章初步建立了ESCC进展的新分层系统和有前景的早期蛋白质预警模型,发现GBP6缺失通过调控细胞周期和激活促进ESCC进展,PARP1抑制可能通过抑制TP63挽救GBP6的渐进性缺失。文构建的图谱弥补了癌前病变进展蛋白质组学研究缺乏的关键空白,并为ESCC研究提供了宝贵的蛋白质数据。
青莲百奥解决方案
青莲百奥提供一站式区域空间蛋白质组学和全息空间蛋白质组学服务,从组织切片选择感兴趣的区域(ROI),再到LCM与质谱检测分析,满足您空间蛋白质组研究的多重需求,为空间蛋白质组学领域提供了更多选择。
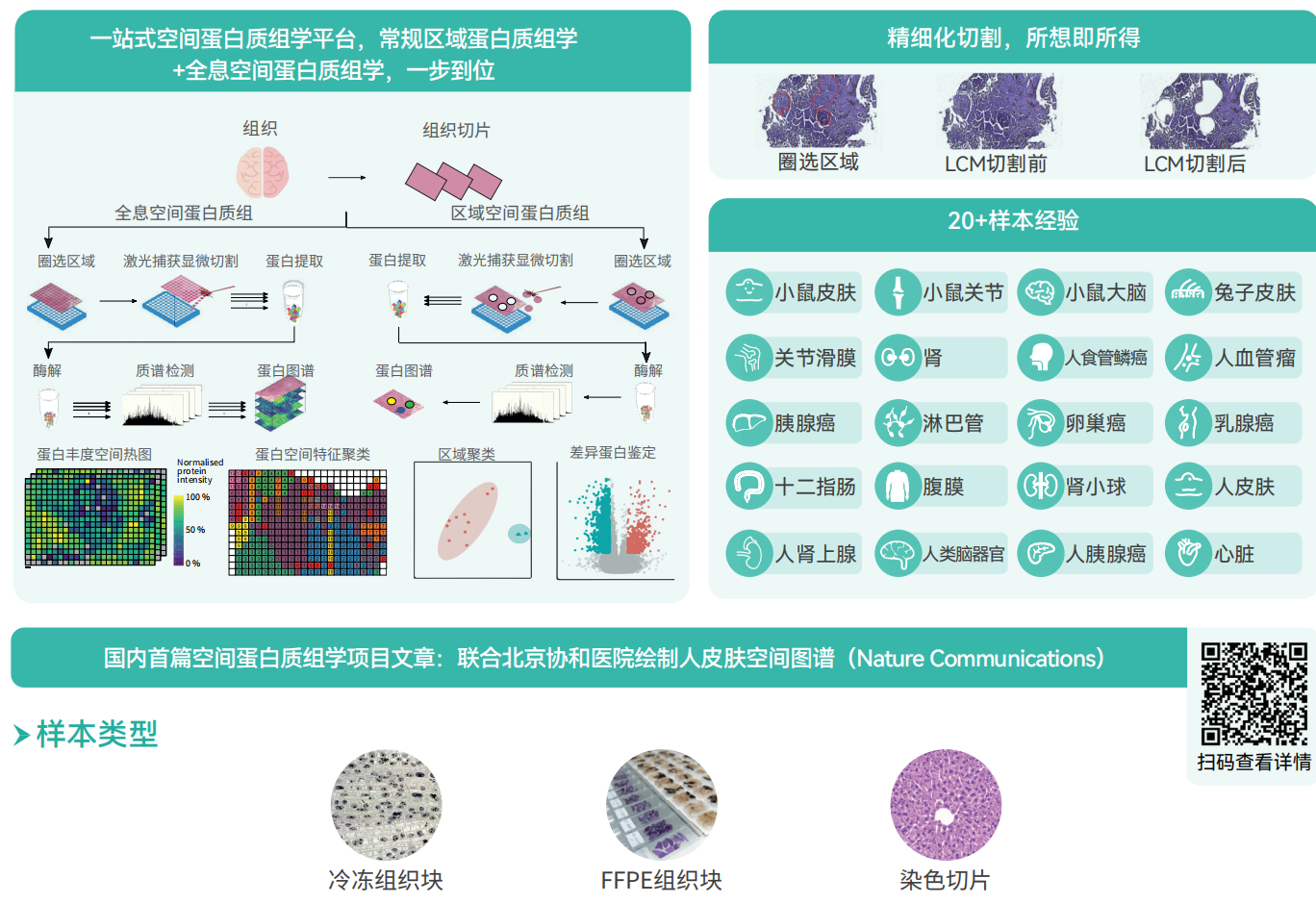
参考文献
Li X, Yuan J, Gao M, Liu J, Wang Q, Zhang Y, Cao M, Hu X, Yang H, Li J, Li C, Li X, Wang H. Spatio-Temporal Proteomic Landscape Reveals Early Warning Signals of Esophageal Squamous Cell Carcinoma Progression. Adv Sci (Weinh). 2026 Mar;13(16):e14343.