椎间盘退变(IVDD)是导致腰痛和残疾的主要原因,全球患者超4亿。现有临床治疗(保守或手术)只能缓解症状,无法阻止疾病进展。椎间盘作为人体最大无血管组织,髓核(NP)处于缺氧低营养微环境,退变时乳酸大量堆积(浓度超血浆 10 倍)是核心特征。乳酸可介导蛋白质赖氨酸乳酸化(新型翻译后修饰),调控肿瘤、纤维化、炎症等病理过程,但乳酸化在 IVDD 中的全景图谱、关键靶点及作用机制完全未知。
2026年2月28日,陆军军医大学李长青教授团队在子刊《Nat Commun》(IF:15.7)发表文章“ SOD1 lactylation impair its enzymatic activity by conformational change to aggravate intervertebral disc degeneration”。该研究依托乳酸化蛋白质组、代谢组与单细胞测序多组学技术,系统描绘了IVDD中的乳酸化修饰图谱,筛选并锁定椎间盘退变中关键的 SOD1 K123 位点乳酸化修饰,验证了SOD1 K123 乳酸化通过构象改变损害酶活,激活 p53 通路诱发髓核细胞衰老与退变的机制。在此基础上,通过虚拟筛选获得靶向小分子ZL-01,并构建了髓核细胞靶向递送系统,最终形成覆盖乳酸化修饰→关键靶点→分子机制→药物干预→递送策略的完整研究链条的完整研究链条。

研究亮点
1.首次揭示IVDD中乳酸化修饰的全景图:系统描绘了退变髓核组织中蛋白乳酸化谱,并发现其与氧化应激密切相关。
2.发现并验证SOD1 K123la这一关键致病修饰:阐明了SOD1 K123la-p53轴在IVDD中的新机制:连接了乳酸代谢、氧化还原稳态和细胞衰老/凋亡通路。
3.开发有转化潜力的治疗策略:通过虚拟筛选获得首个靶向SOD1 K123la的小分子抑制剂ZL-01,并利用II型胶原靶向肽修饰的EVs实现了药物在髓核的滞留和递送,有效缓解IVDD。
研究结果
1. IVDD中乳酸积累驱动蛋白乳酸化,且与髓核细胞氧化损伤高度关联
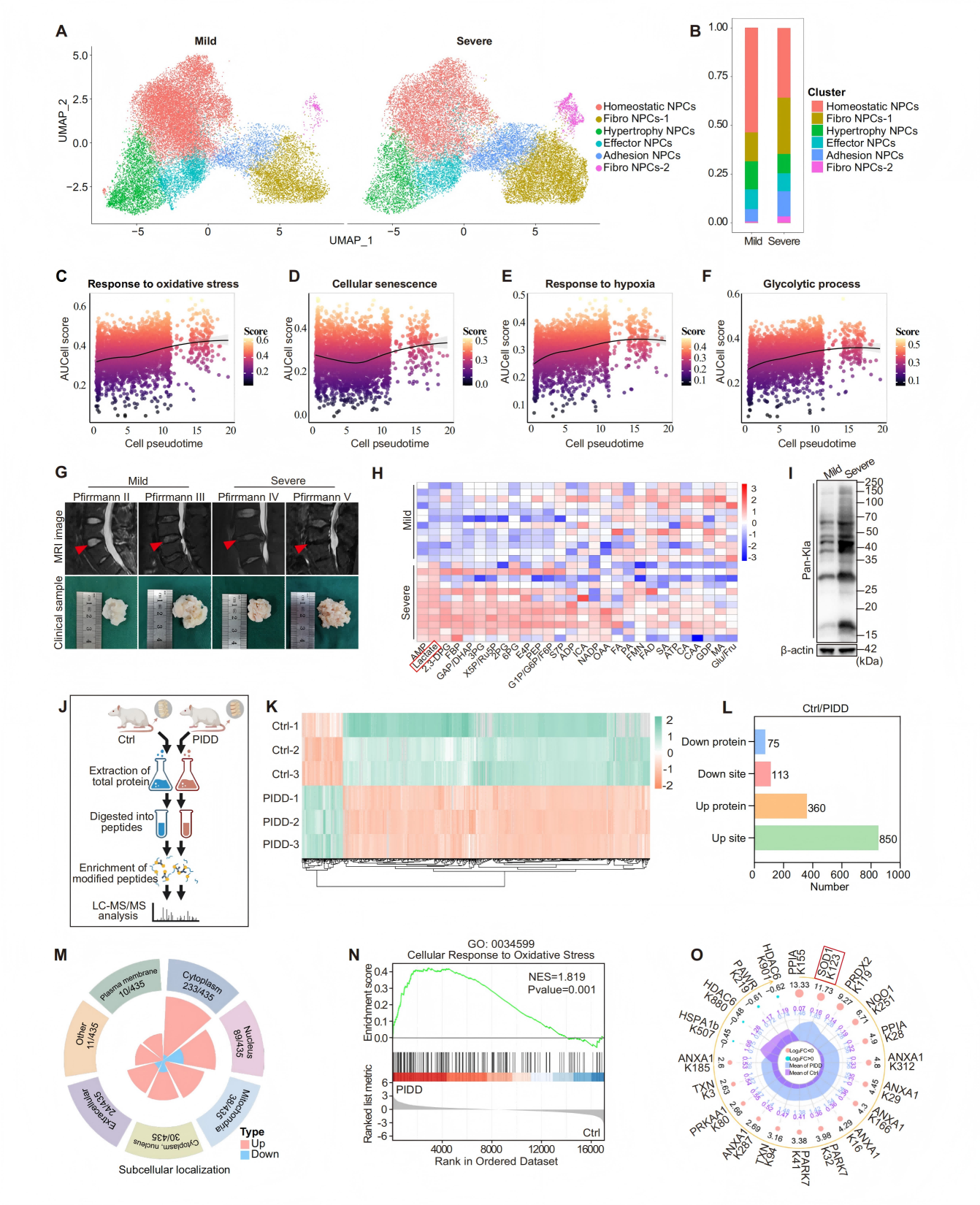
研究者首先分析了人退变髓核组织的单细胞测序数据,发现重度退变患者中纤维化髓核细胞亚群增多。临床样本进一步证实,重度退变髓核中活性氧水平、DNA损伤及细胞衰老标志物均显著升高,且与乳酸含量呈正相关。在大鼠穿刺和自然衰老诱导的椎间盘退变模型中,同样观察到乳酸积累和整体蛋白乳酸化水平升高,而乙酰化、琥珀酰化水平无明显变化。最后,通过乳酸化蛋白质组学分析,系统描绘了退变髓核中的乳酸化修饰图谱,发现差异乳酸化蛋白主要定位于细胞质,并高度富集于“细胞对氧化应激的反应”通路。
2.SOD1 K123la通过激活p53通路加剧髓核细胞氧化损伤
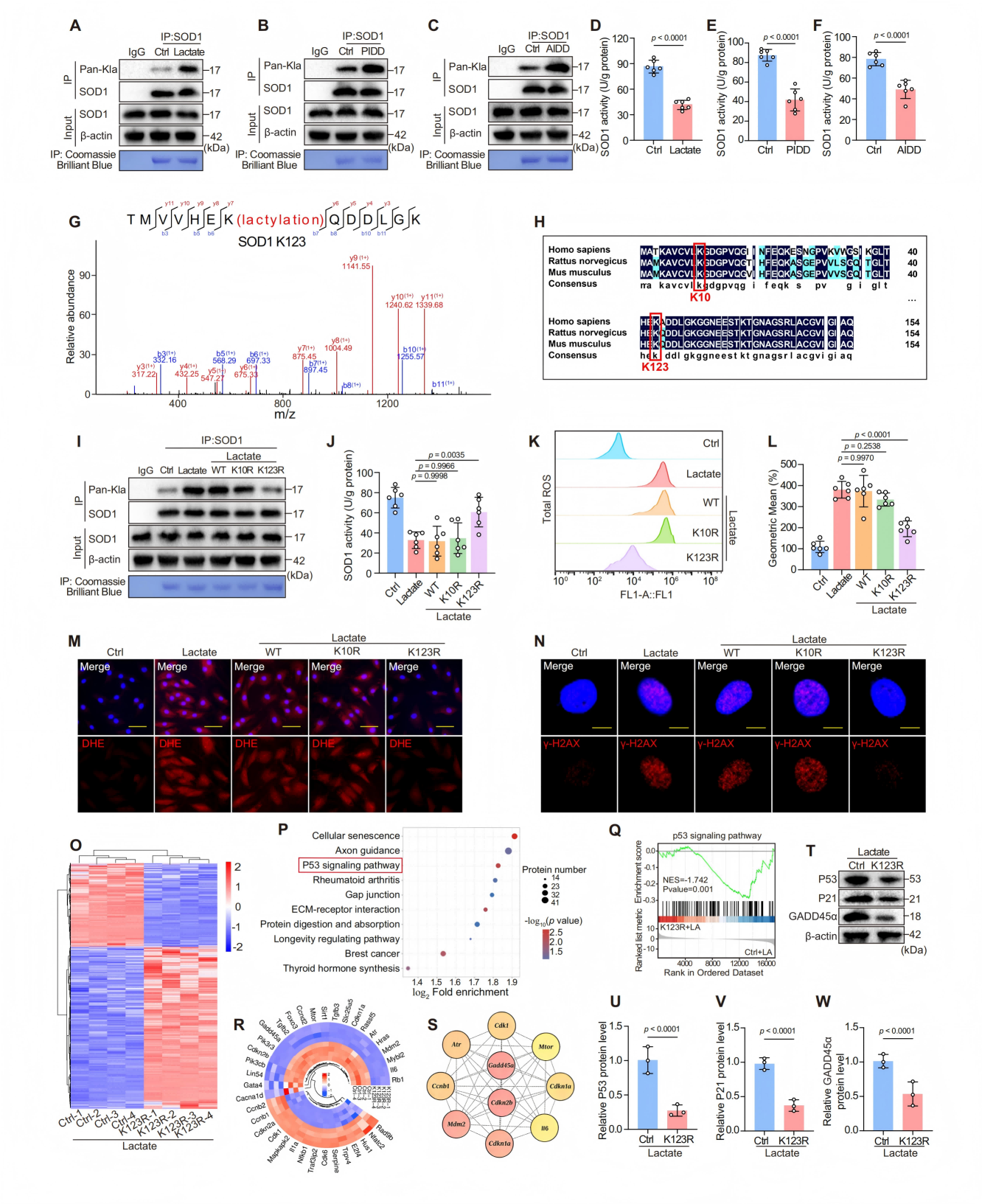
在多组学筛选出的氧化应激相关乳酸化蛋白中,关键抗氧化酶SOD1的乳酸化水平尤为突出。通过构建模拟去乳酸化的K123R点突变发现该突变能有效恢复SOD1酶活性、增加总抗氧化能力,并显著减轻DNA损伤和细胞衰老。转录组测序和WB结果表明,SOD1 K123la主要通过激活p53及其下游靶基因P21和GADD45a来发挥有害作用。进一步通过敲低乳酸转运体,证实胞内乳酸是导致上述效应的关键。
3.SOD1 K123a通过改变构象抑制酶活性并在体内加剧椎间盘退变
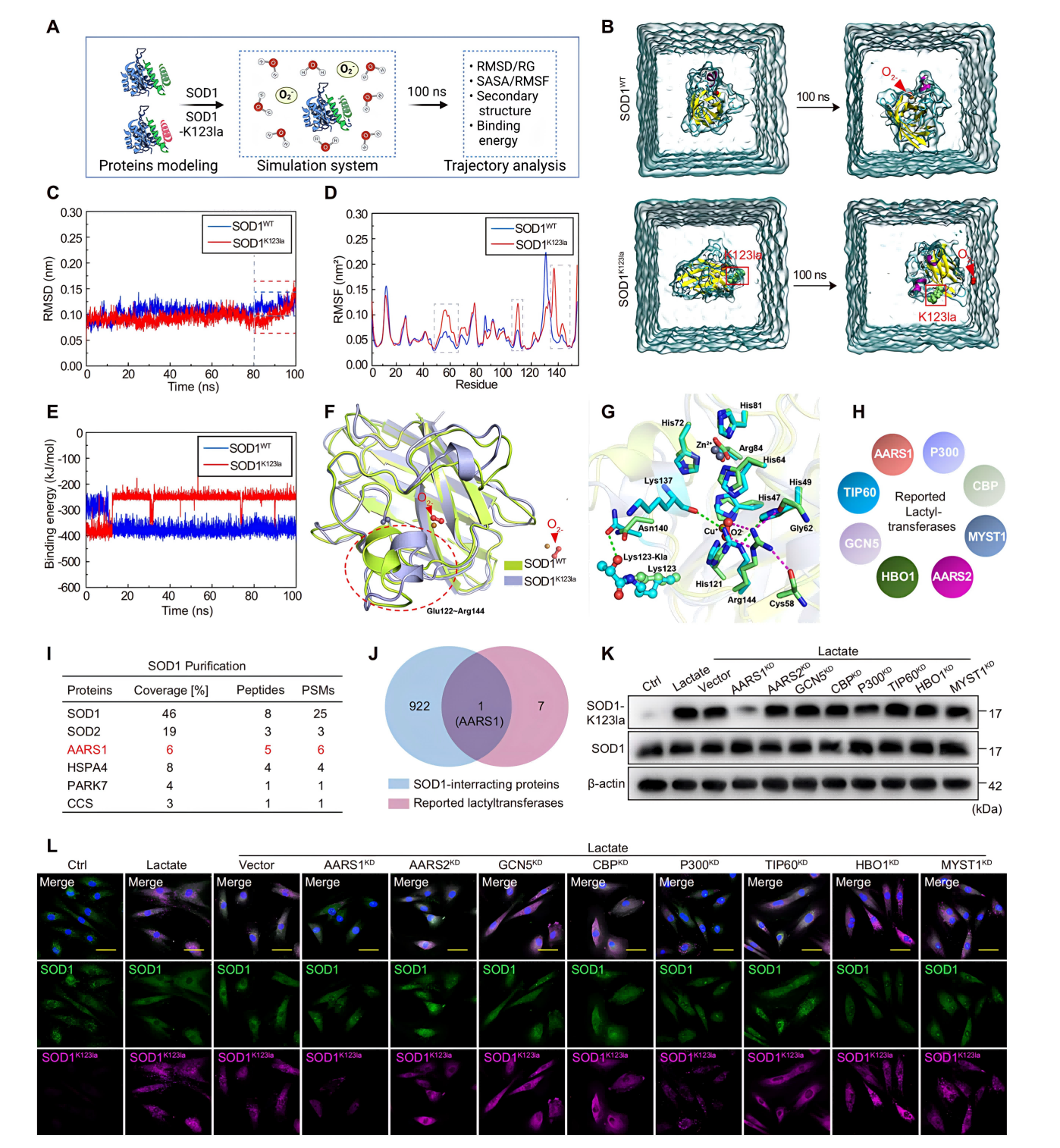
研究者构建了SOD1 K123R敲入大鼠模型,其椎间盘退变程度(磁共振和组织学评分)显著减轻,p53通路活性以及细胞衰老标志均明显降低,而SOD1酶活性和总抗氧化能力则得以恢复。分子动力学模拟揭示了其机制:K123位点发生乳酸化后,破坏了SOD1活性中心附近的Arg144与底物超氧阴离子及关键氨基酸之间的氢键网络,导致蛋白构象稳定性下降、与底物结合能力显著减弱。并通过免疫沉淀-质谱联用技术,鉴定出AARS1和P300是催化SOD1发生K123位点乳酸化的主要乳酰转移酶。
 4.发现并鉴定靶向SOD1 K123a乳酸化的特异性小分子抑制剂ZL-01
4.发现并鉴定靶向SOD1 K123a乳酸化的特异性小分子抑制剂ZL-01
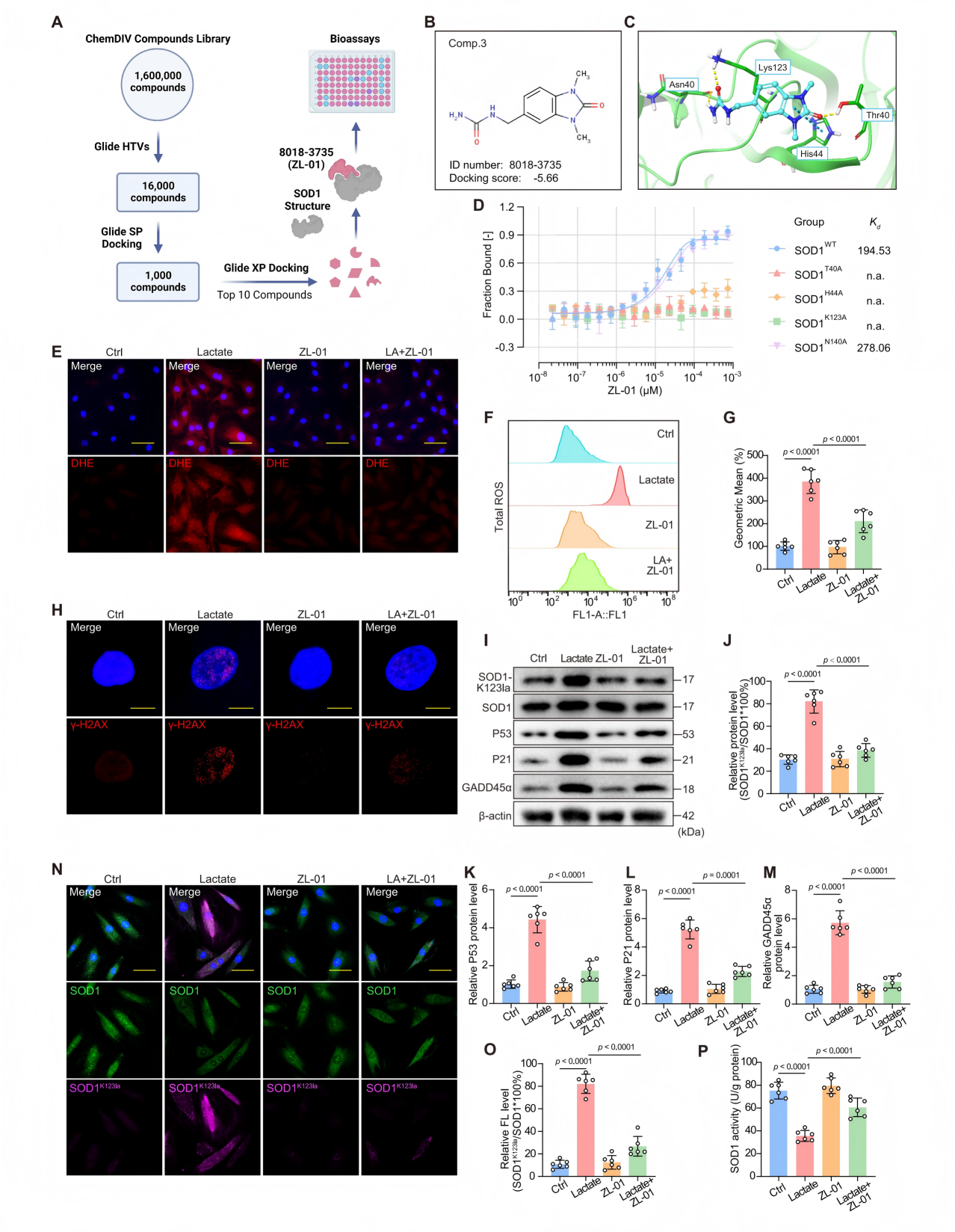
随后,以SOD1蛋白的K123位点为靶点,对包含160万个小分子的化合物库进行了高通量虚拟筛选,成功获得候选化合物3,并将其命名为ZL-01。体外实验验证,ZL-01通过与SOD1蛋白的Thr40、His44、Lys123等残基特异性结合,能够有效降低乳酸处理后髓核细胞中SOD1 K123a的水平,恢复SOD1酶活性,减少活性氧产生、DNA损伤和细胞衰老,且对SOD1的乙酰化和琥珀酰化修饰无明显影响,显示较好的特异性。
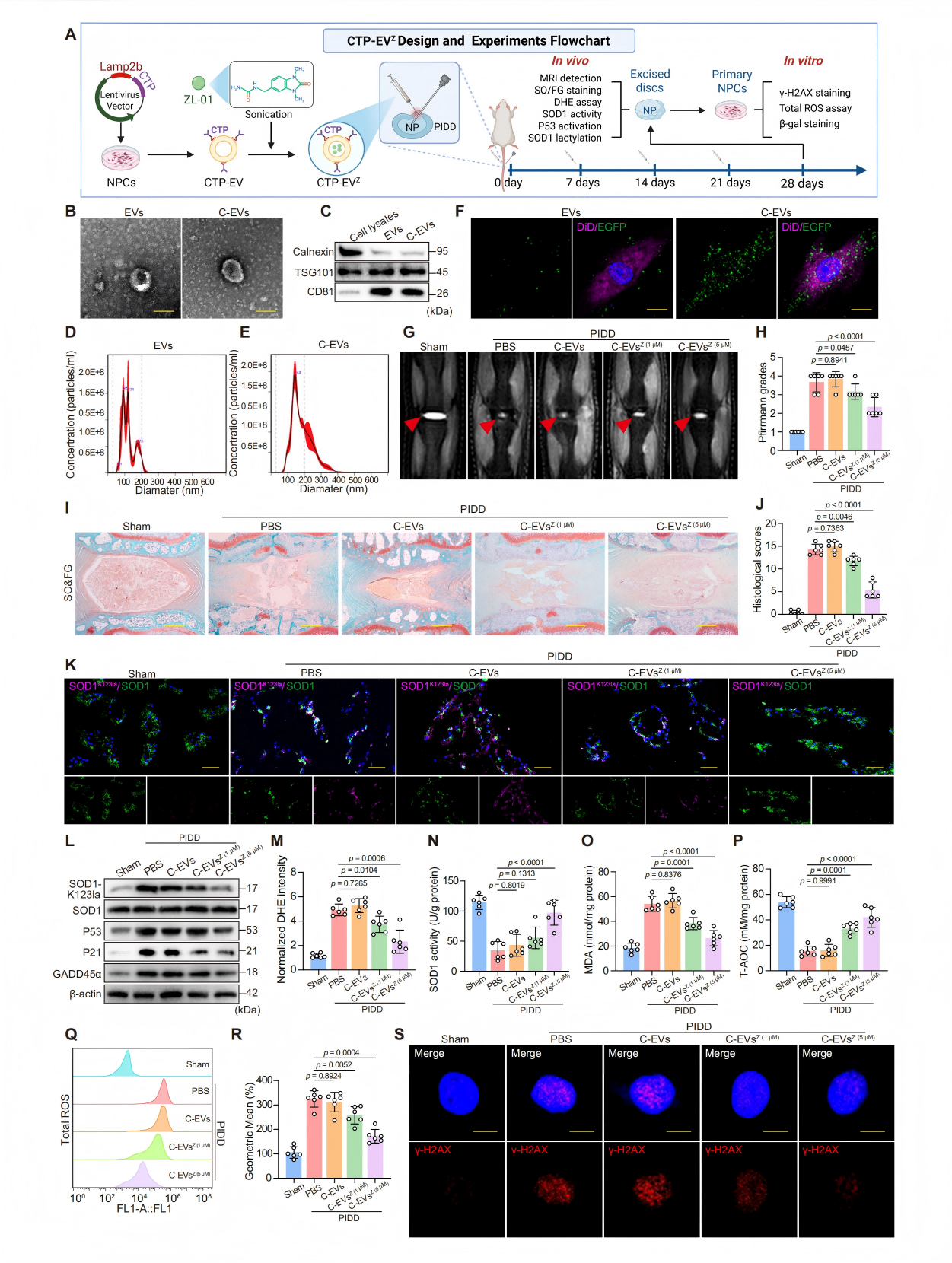
5.靶向递送ZL-01有效缓解大鼠椎间盘退变
研究者开发了一种工程化细胞外囊泡递送系统:在囊泡表面表达II型胶原靶向肽,使其能主动靶向髓核组织,并将ZL-01装载其中(C-EVsZ)。在椎间盘退变大鼠模型中,局部注射C-EVsZ不仅显著改善了磁共振和组织学退变评分,而且有效降低了髓核组织中SOD1 K123a水平,恢复了SOD1酶活性,抑制了p53通路,并减少了氧化损伤和细胞衰老,且未观察到明显的全身毒性。
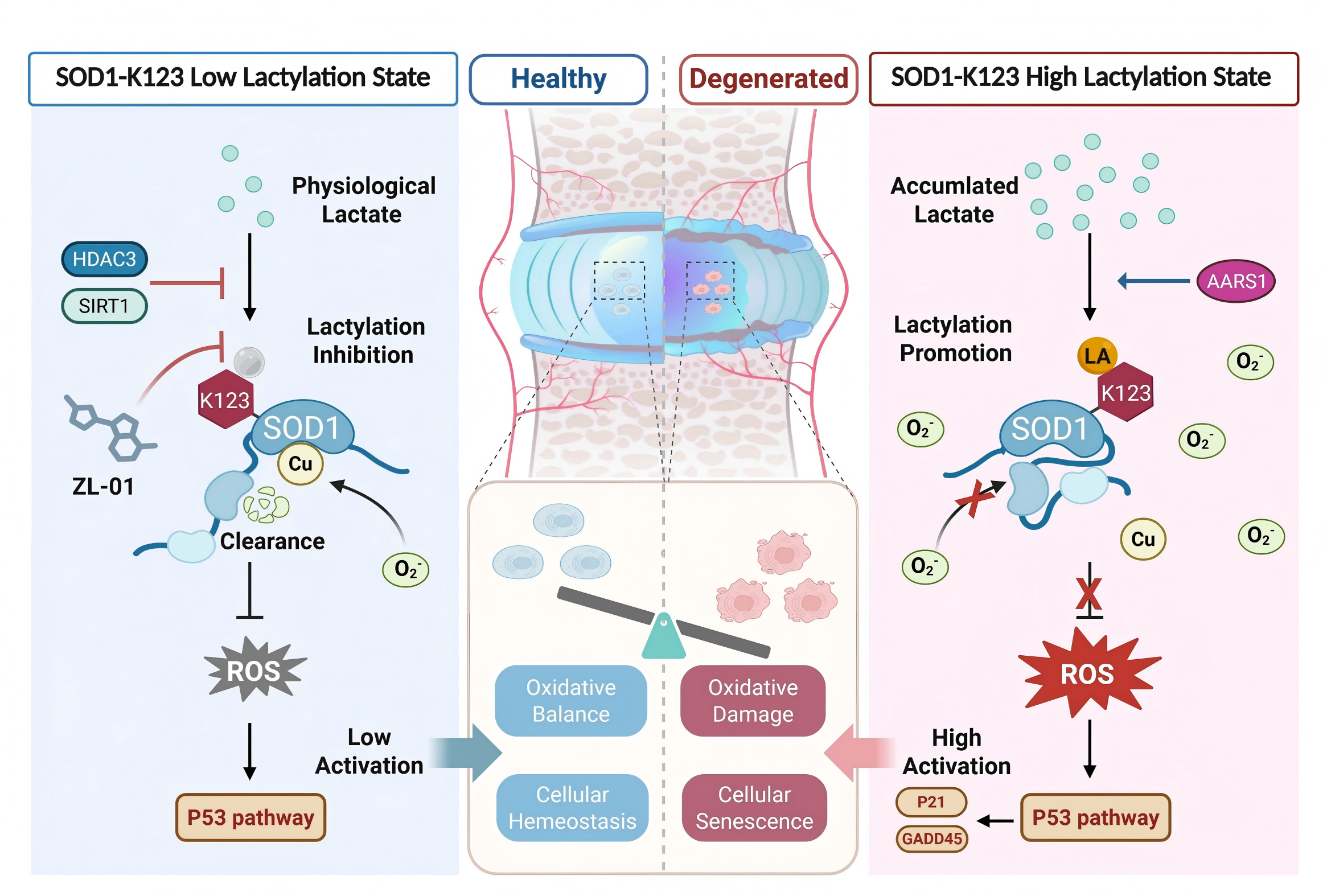
研究结论与意义
该研究系统揭示了椎间盘退变中乳酸化修饰的关键致病作用,阐明了SOD1在K123位点的乳酸化通过改变蛋白构象、抑制其酶活性并激活p53通路,从而加剧髓核细胞氧化损伤和椎间盘退变的核心机制。同时,所开发的特异性小分子抑制剂ZL-01及其靶向递送系统,为椎间盘退变的疾病修饰治疗提供了极具临床转化潜力的新策略。
青莲百奥修饰组学解决方案
青莲百奥修饰蛋白组学产品线升级,不仅精心打磨了经典修饰产品线(如磷酸化、糖基化、泛素化等),同时开拓了一系列新型修饰产品线(如乳酸化、棕榈酰化、琥珀酰化、氧化还原等)。现凭借先进的高分辨率、高灵敏度质谱技术,积累了丰富的修饰组学研究经验,提供深入的生物信息学分析报告,为科研工作的深入探索和成果的有效转化提供强有力的支持。
