
新型冠状病毒Omicron变异株自2021年末出现以来,已逐步取代早期毒株成为全球主要流行株。新型冠状病毒Omicron变异株虽致病力较原始株显著减弱,但部分轻症或无症状感染者仍可出现肺部炎症渗出及CT影像异常。这种"轻症-肺损伤"分离现象提示,Omicron可能通过特定分子机制选择性损伤肺血管-肺泡屏障(血气屏障),但其具体路径尚未阐明。同时也提示Omicron的致病机制与原始株不同,不能仅靠常规炎症指标判断损伤程度。
2025年4月23日,广州医科大学附属第一医院、呼吸疾病国家重点实验室孙宝清团队在《Nature Communications》上发表了题为“VCL/ICAM-1 pathway is associated with lung inflammatory damage in SARS-CoV-2 Omicron infection”的研究论文,整合血液蛋白组学、N-糖基化组和代谢组学等多个组学技术,阐明了Omicron BA.2.76感染导致肺部炎症性损伤的核心机制——VCL/ICAM-1通路的异常激活,并证实靶向该通路可有效减轻肺泡水肿、修复血气屏障完整性,为开发针对新冠病毒血管并发症的新型疗法提供了极具潜力的靶点。

研究方法与材料
发现队列:包括20名无症状Omicron感染者、20名有症状Omicron感染者、20名原始株感染者及20名健康对照。所有Omicron感染者均无疫苗接种史。
验证队列:20名有症状Omicron感染者和15名健康对照,用于验证在发现队列中识别的关键生物标志物。
关键技术:血浆蛋白质组学、N-糖基化组学、非靶向代谢组学、大鼠急性肺损伤模型等。
研究结果
1. 血液蛋白组学发现Omicron感染的特征:凝血与细胞骨架重塑
作者首先对参与者的临床特征和实验室生物标志物进行比较,相比原始毒株,Omicron感染引发了独特的免疫应答模式和炎症状态。
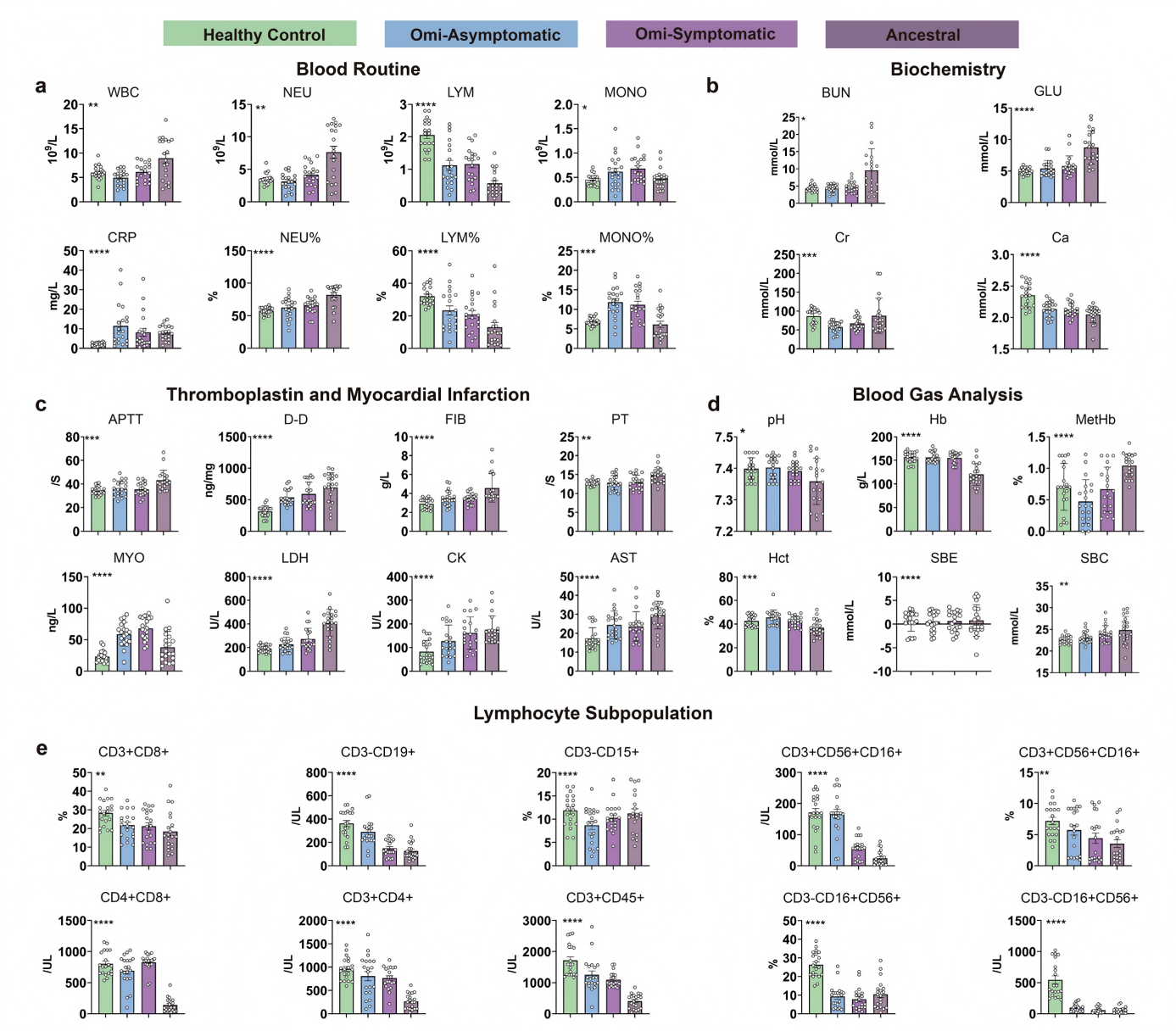
图1.临床特征对比
使用Orbitrap Exploris™ 480对血浆样本进行体液蛋白质组学分析(未去除高丰度蛋白),鉴定到了726种蛋白质。与健康对照组相比,无症状和有症状Omicron感染者分别有51和62个差异表达蛋白。通路富集分析显示,即使是无症状感染者,其血小板功能、凝血和血管反应也发生了显著变化。有症状感染者的变化则更突出,涉及糖酵解/糖异生、黏着斑等通路,表明存在显著的代谢重编程和细胞粘附机制改变。
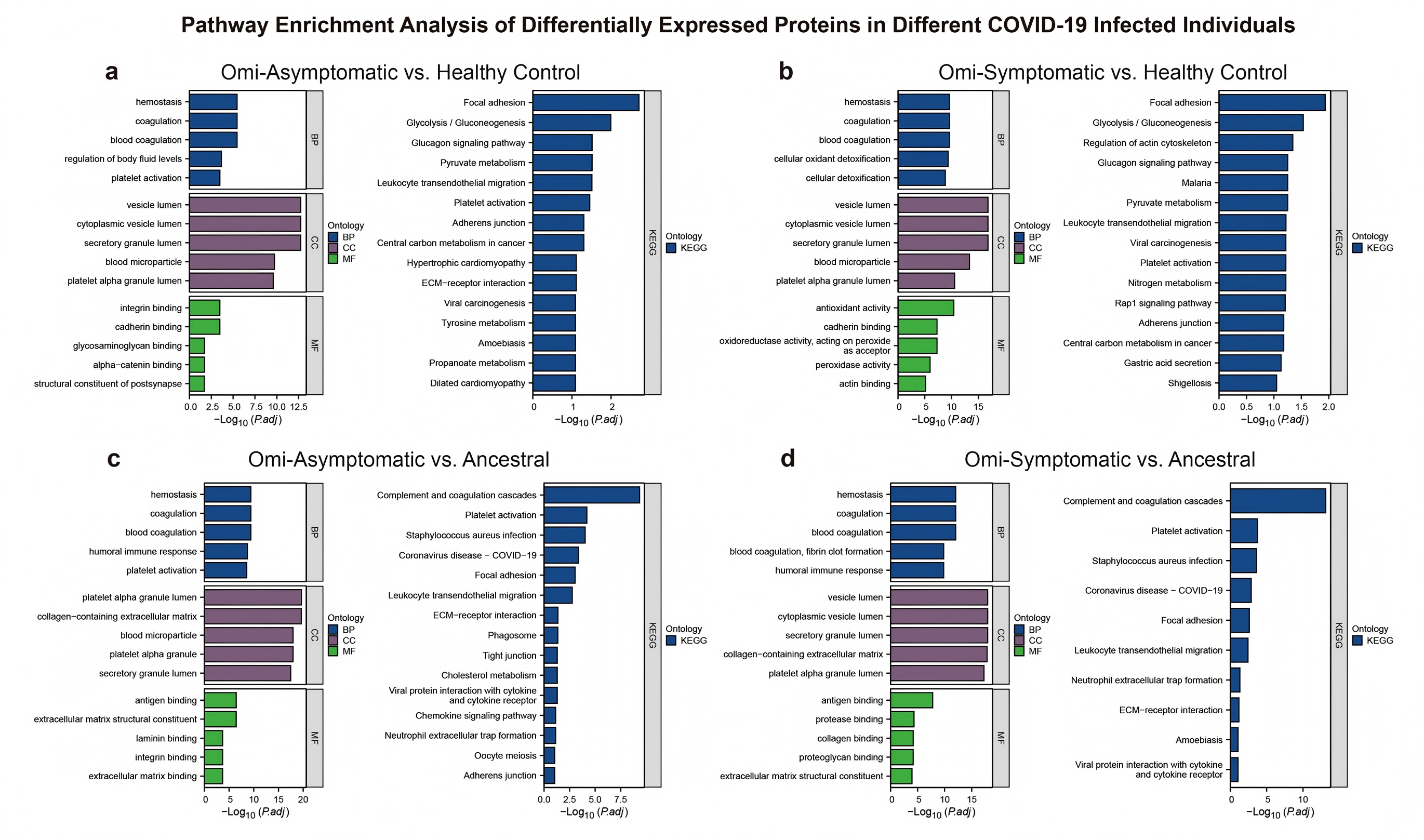
图2. Omicron感染者差异表达蛋白质的通路富集分析
蛋白互作网络筛选出纽蛋白(VCL)和细胞间黏附分子-1(ICAM-1) 在Omicron感染者(尤其是有症状者)中位于核心位置。功能富集分析指出,这些枢纽蛋白与肌动蛋白细胞骨架组织、凝血、血小板活化等通路密切相关。VCL和ICAM-1在Omicron和原始株感染者中表达均上调,提示它们在炎症粘附和渗出过程中扮演关键角色。
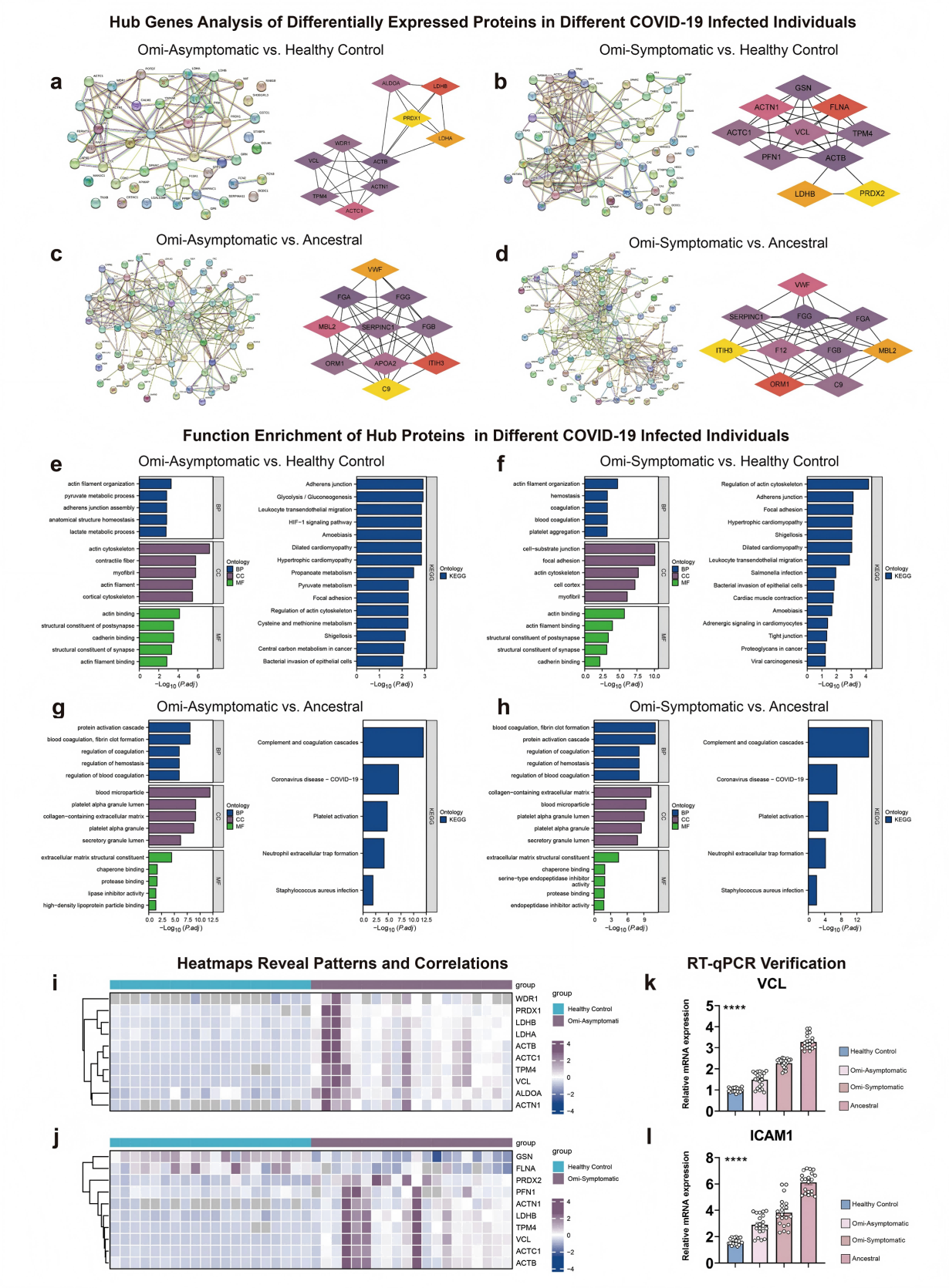
图3. Omicron感染核心枢纽蛋白的筛选及其功能富集分析
2. 代谢组学揭示能量代谢失衡与炎症微环境
随后的代谢组学分析进一步描绘了Omicron感染的代谢图谱。研究发现,Omicron感染(无论有无症状)均引起了显著的代谢重编程,涉及嘌呤代谢、药物代谢、鞘脂代谢和类固醇激素生物合成等通路。对三羧酸循环(TCA)和糖酵解代谢物的分析揭示了不同毒株的差异:原始株感染同时激活了TCA循环和无氧糖酵解(乳酸水平升高),而Omicron感染则表现为TCA循环活性增强,但维持相对正常的无氧糖酵解。这表明Omicron感染引发了不同的能量代谢应激状态。
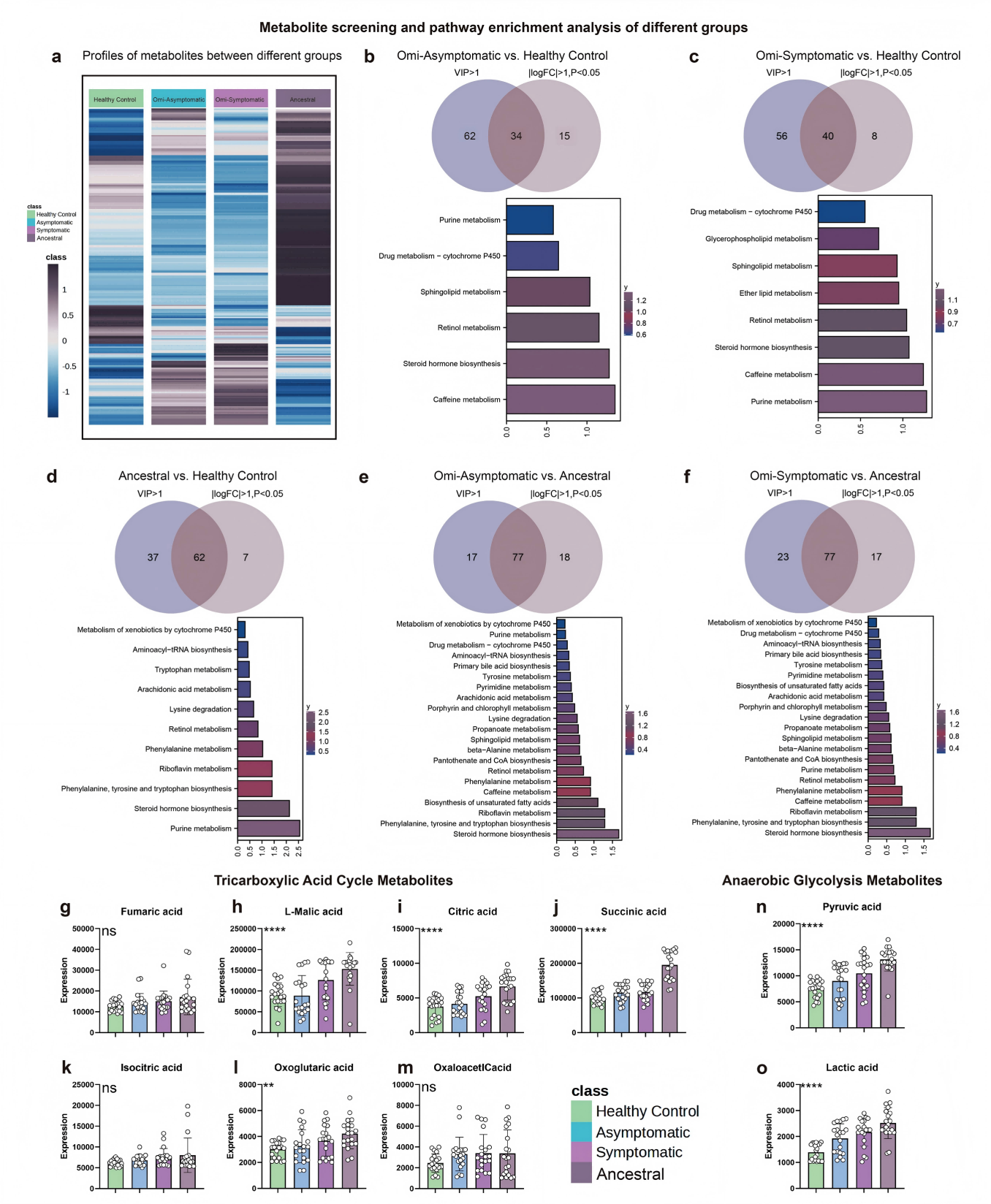
图4. 不同感染组的全面代谢物谱与通路富集分析
3. 整合组学锁定VCL通路,并与临床指标强相关
将体液蛋白质组与代谢组数据整合分析后发现,VCL、ICAM-1与全反式维甲酸等代谢物处于互作网络的核心,富集于Rap1信号通路、黏着斑、凝血调节等通路。相关性分析提供了更直接的临床证据。研究发现,血浆中VCL水平与关键临床炎症标志物CRP、PCT、血清淀粉样蛋白A(SAA) 以及影像学上的CT评分(直接评估肺部渗出程度)均呈显著正相关,说明VCL不仅是分子标志物更能够反映疾病的炎症状态和肺部渗出损伤的严重程度。
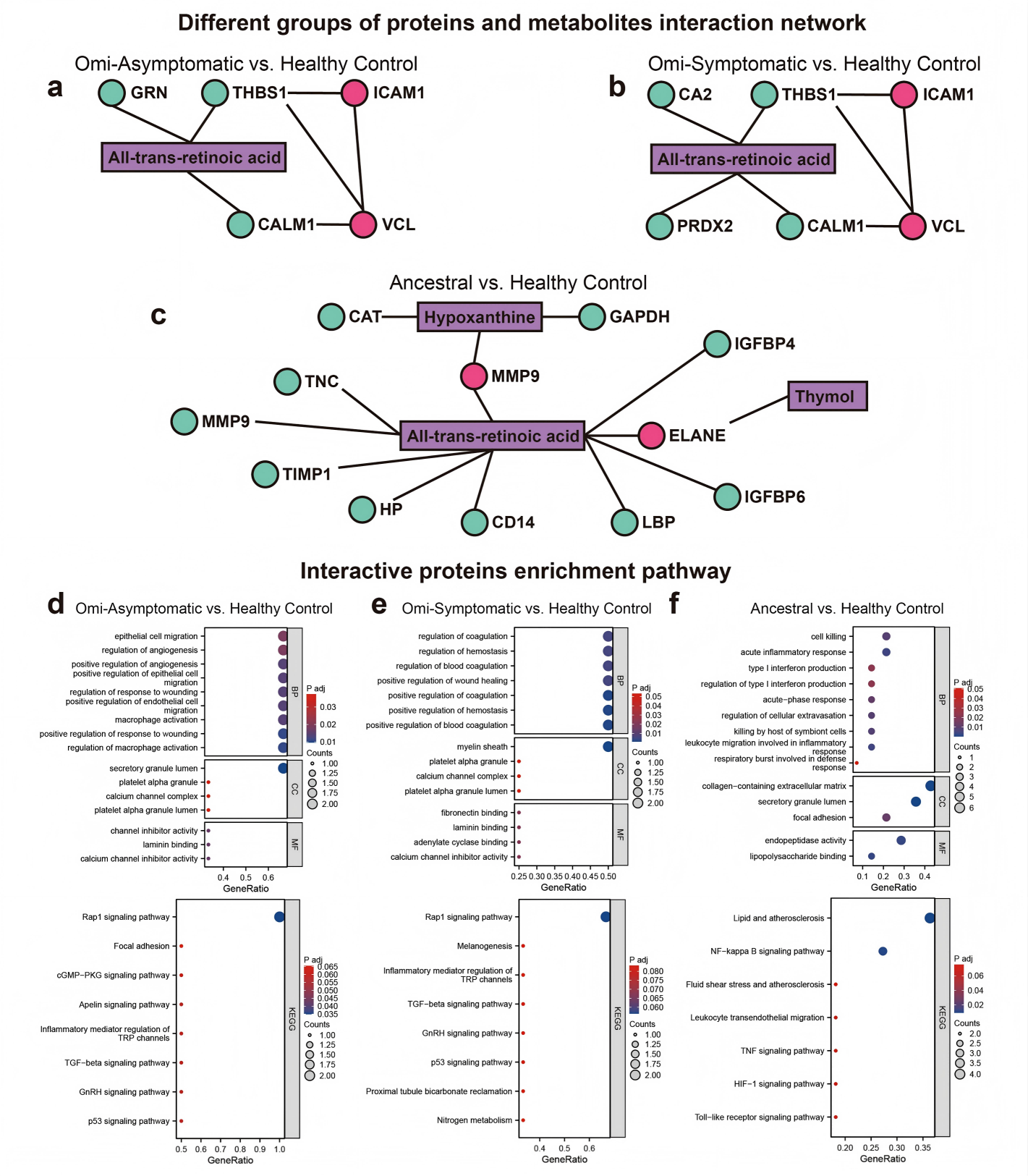
图5. 蛋白质与代谢物的相互作用网络及其通路富集
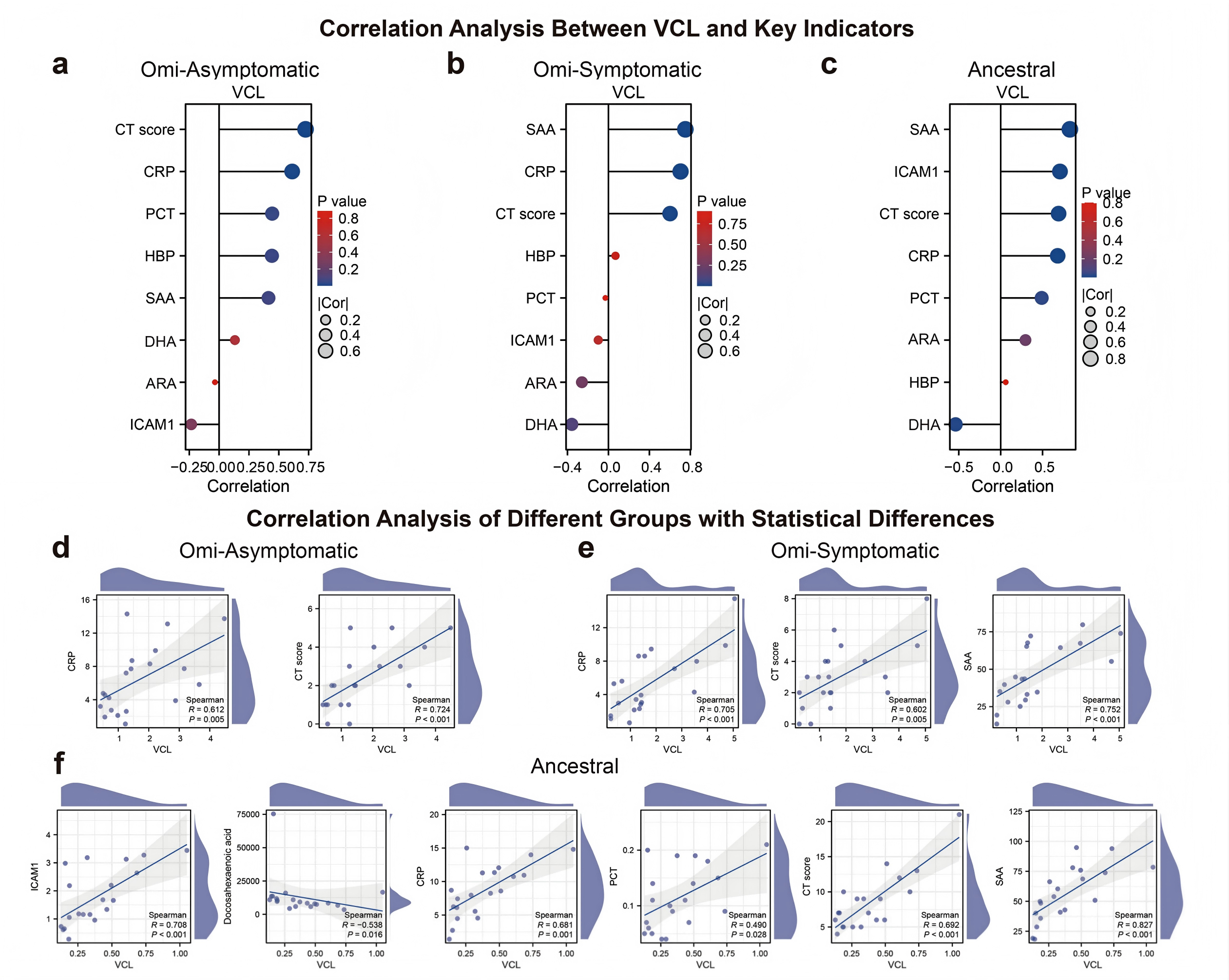
图6a-f. VCL-ICAM1通路与临床指标的相关性
4. N-糖基化修饰为VCL的“活跃”提供证据
蛋白质的N-糖基化修饰对其功能至关重要。本研究有一个关键发现:随着疾病严重程度从无症状Omicron、有症状Omicron到原始株感染递增,VCL的N-糖基化修饰水平呈现逐步升高的宏观趋势。相反,ICAM-1的N-糖基化水平则线性下降。VCL糖基化的增加可能会增强其介导细胞外渗和粘附的能力,从而加剧炎症和血管变化。
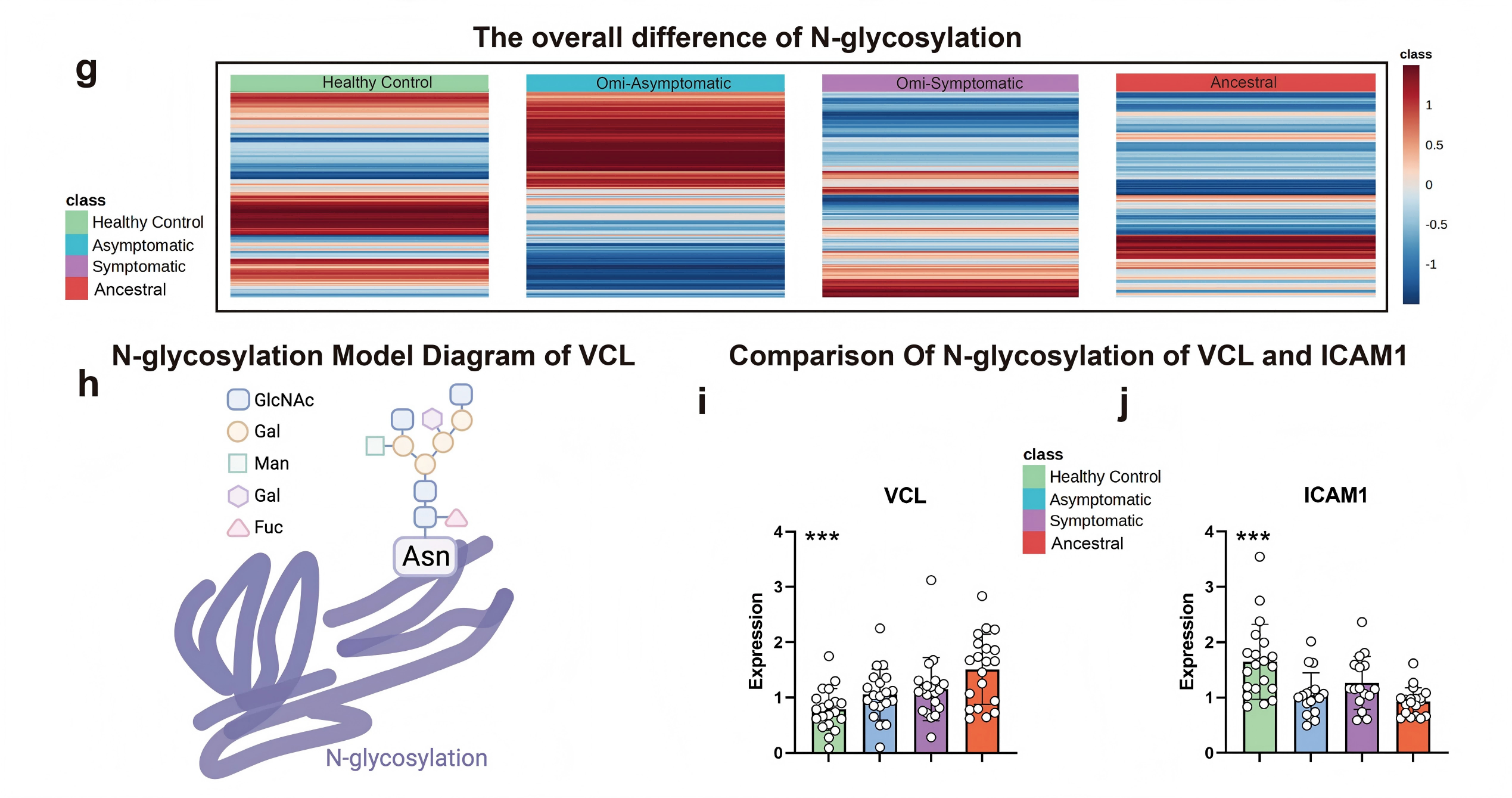
图6g-j. VCL-ICAM1通路N-糖基化水平分析
5. 动物模型验证:抗VCL干预有效保护血气屏障
为验证VCL-ICAM1通路对Omicron感染的影响,作者构建了大鼠肺损伤模型。血浆指标检测发现,肺损伤模型大鼠血浆中的VCL、ICAM-1、肝素结合蛋白(HBP)和CRP水平显著升高,而抗VCL干预能显著降低这些指标。HE染色显示,肺损伤大鼠肺泡结构塌陷、间质增厚、炎性细胞浸润、肺泡水肿。抗VCL干预后,肺泡水肿明显减轻。透射电镜进一步观察到,干预后受损的肺泡毛细血管屏障(血气屏障)结构基本恢复正常。免疫荧光显示,肺损伤组织中VCL表达显著增加,清晰地勾勒出肺泡结构,表明其在炎症环境中细胞骨架活性增强。最后作者由此提出抗VCL干预是Omicron感染的潜在治疗方法。
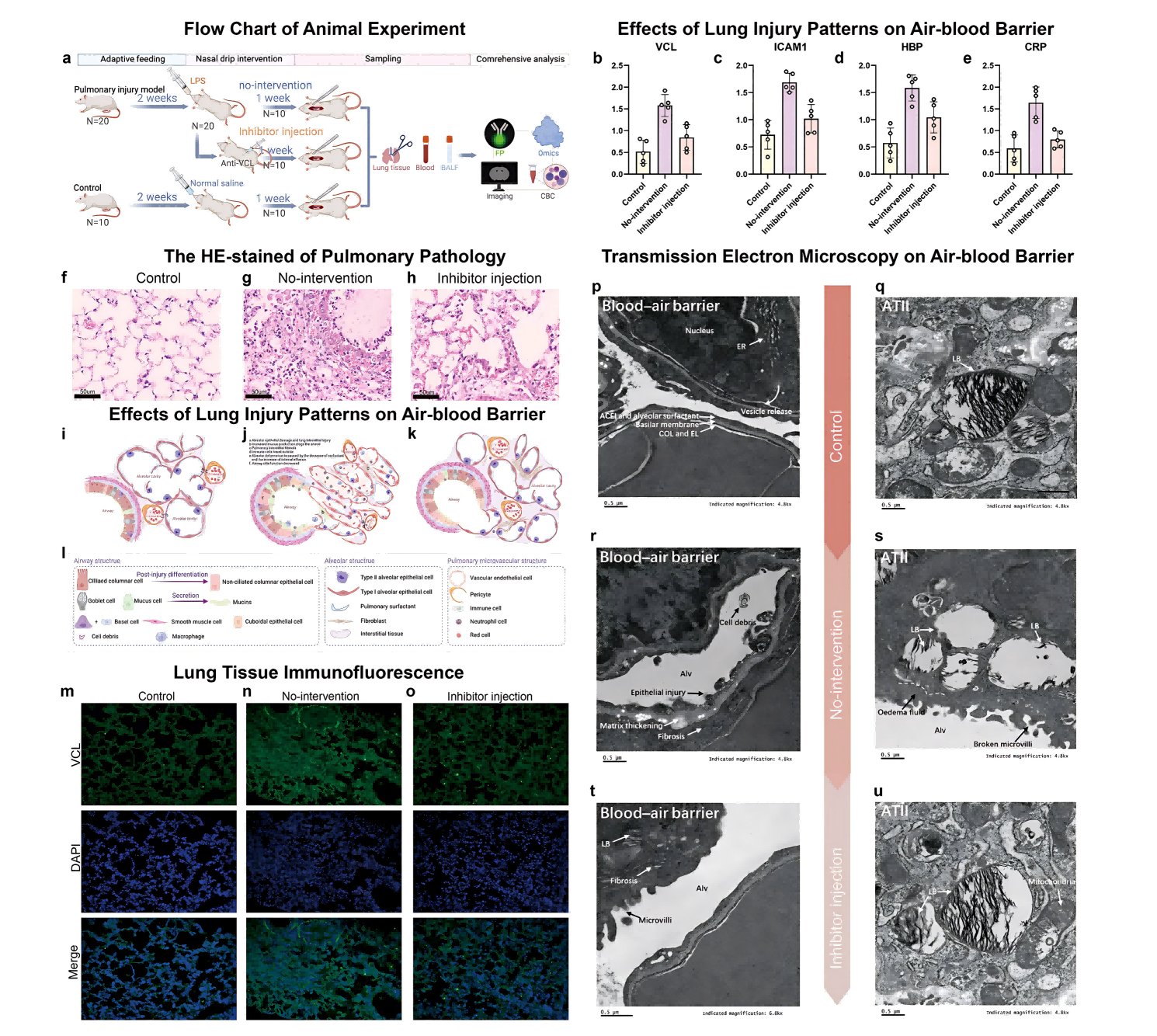
文章总结
研究通过血液蛋白组、N-糖基化修饰组学和代谢组等多组学整合,明确了Omicron的独特致病路径,Omicron通过特异性激活VCL/ICAM-1通路,导致肺部局部的细胞骨架重塑、内皮细胞功能障碍和血管通透性增加,最终引发肺部炎症渗出和血气屏障损伤。VCL不仅是Omicron感染相关的生物标志物,其表达水平和糖基化修饰程度与疾病严重度相关,而且靶向VCL的干预在动物模型中显示出明确的治疗效果。
本研究首次将差异化糖基化修饰与病毒感染所致的血管渗漏、炎症微环境重塑直接关联,为开发针对新冠病毒血管并发症的精准医疗策略提供了全新线索。
即使Omicron感染者症状轻微,也应关注肺部微血管损伤;靶向VCL/ICAM-1通路及N-糖基化修饰,有望成为未来抗病毒血管损伤治疗的新方向。
