下腰痛(lower back pain, LBP)是肌肉骨骼系统常见症状,也是导致残疾的主要原因之一。研究已明确椎间盘退变(intervertebral disc degeneration, IVDD)是LBP的主要病因,椎间盘椎间盘是由髓核(nucleus pulposus, NP)、纤维环(annulus Fibrosus, AF)和软骨终板(cartilaginous endplates, CE)组成的复杂结构关节。位于椎间盘中央的髓核为凝胶状物质,内含髓核细胞(nucleus pulposus cells, NPCs)和细胞外基质。NPCs的功能状态对维持椎间盘稳态至关重要。然而,由于对其潜在分子机制的认识尚不充分,椎间盘退变的有效治疗仍面临重大挑战。
线粒体功能障碍与IVDD密切相关。近年来,线粒体双链RNA(mitochondrial double-stranded RNA,mtdsRNA)作为一种新型损伤相关分子模式受到广泛关注,研究已证实mtdsRNA的胞质积累在骨关节炎、亨廷顿病、干燥综合征及非酒精性脂肪肝等疾病中发挥重要作用,但其在IVDD中的功能仍待深入探索。
今年10月9日,武汉协和医院曹阳、廖志伟团队于Cell Commun Signal(IF=8.9)杂志上发表了题为“Taurine can restrict MtdsRNA mediated pyroptosis by enhancing mitophagy in nucleus pulposus cells”的研究论文,该研究通过整合临床测序数据与细胞模型功能实验,发现了mtdsRNA在IVDD中发挥的重要作用:氧化应激下的髓核细胞通过释放mtdsRNA激活RIG-I/MDA5-MAVS-NLRP3轴诱发焦亡;退变过程中牛磺酸稳态失衡会加剧mtdsRNA释放,而外源性补充牛磺酸可通过增强线粒体自噬抑制mtdsRNA泄漏、维持线粒体健康。这些发现将牛磺酸代谢、线粒体核酸和细胞焦亡联系起来,并表明mtdsRNA是椎间盘退变的重要致病分子和潜在治疗靶点。
北京青莲百奥生物科技有限公司为文章提供了转录组学服务。

研究结果
一、退行性髓核组织中mtdsRNA升高
研究整合了先前临床组织研究的测序数据,发现在退行性NP组织样本中,dsRNA相关基因如IFIT5、MX1、RIG-I和IFIH1等呈现高表达,1型干扰素相关通路和病毒感染相关的RLR通路也显著上调。在椎间盘组织样本中的qRT-PCR分析也证实了退行性NP组织mtdsRNA高表达。WB分析显示,在退行性NP组织中,PNPT1表达显著降低,RIG-I和MDA5显著升高,而MAVS水平虽然没有变化,但寡聚化明显增加,说明RLR-MAVS通路可能在退行性NP组织中被激活。因此研究判断,在退行性NP组织中,mtdsRNA显著升高,并通过激活RLR信号通路引发组织炎症。
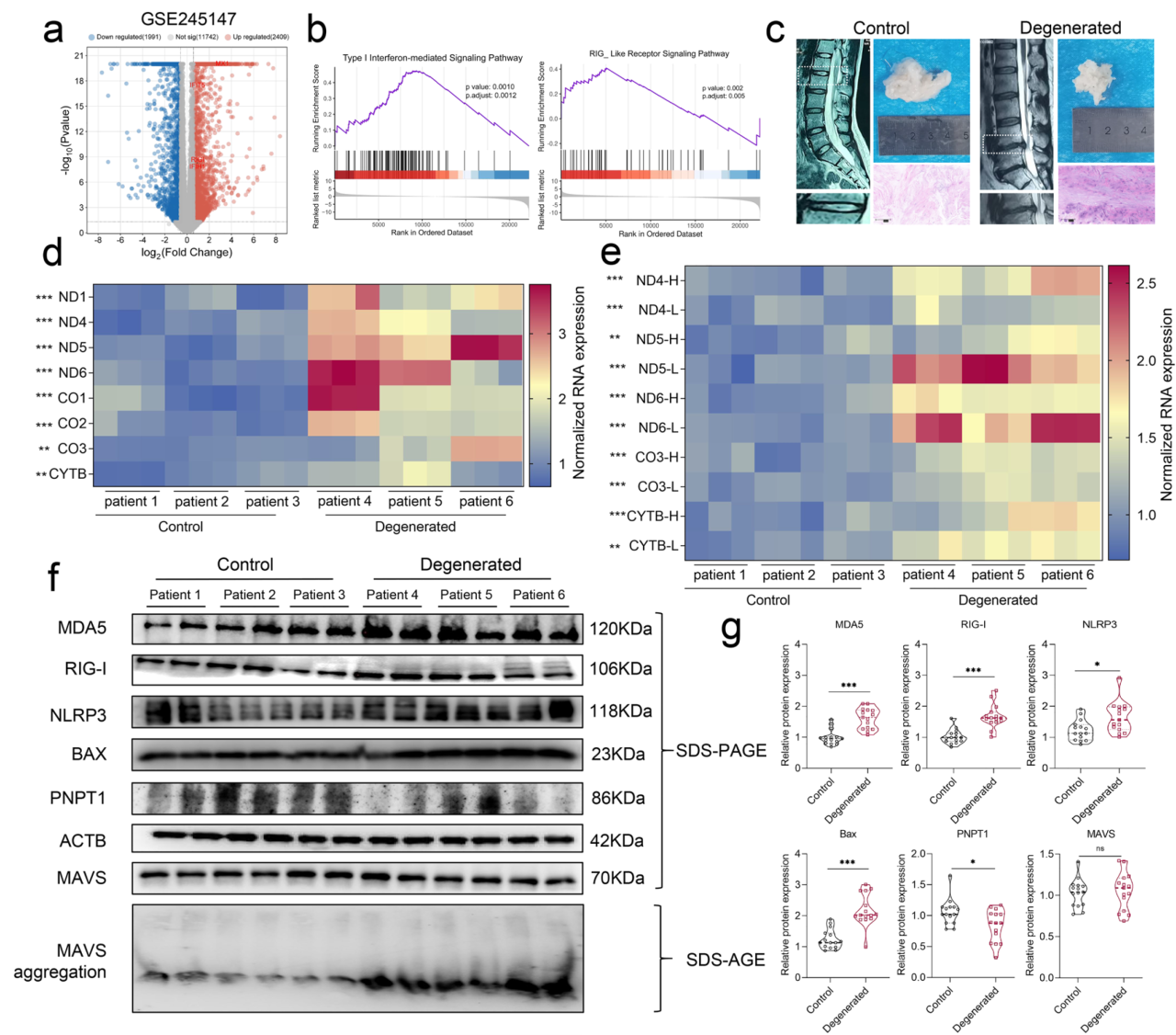
图1. NP组织中的mtdsRNA
二、mtdsRNA与细胞焦亡
mtdsRNA已被证明可以诱导细胞炎症,NLRP3为细胞焦亡的关键介质。通过LPS诱导NPCs构建细胞焦亡模型,分析发现RIG-I和MDA5均呈现出和退行性NP组织中一致的升高趋势,MAVS也出现寡聚化。其中RIG-I和MDA5都与mtdsRNA结合,说明dsRNA具有诱导RLR-MAVS激活并促进细胞焦亡进展的潜力。在LPS刺激下,MAVS和NLRP3之间增强的相互作用也佐证了这一观点。
为了进一步揭示RLR-MAVS在细胞焦亡进展中的作用,研究团队进行了基因敲除实验,发现敲低RLR和MAVS都导致焦亡指标的表达降低,敲低MAVS比敲低RIG-I或MDA5更有效地缓解细胞焦亡的进展,可能归因于MAVS位于RLR的下游,对于细胞焦亡的重要性更高。上述结果表明,LPS刺激释放的mtdsRNA,通过激活RLR-MAVS通路促进细胞焦亡的进展。
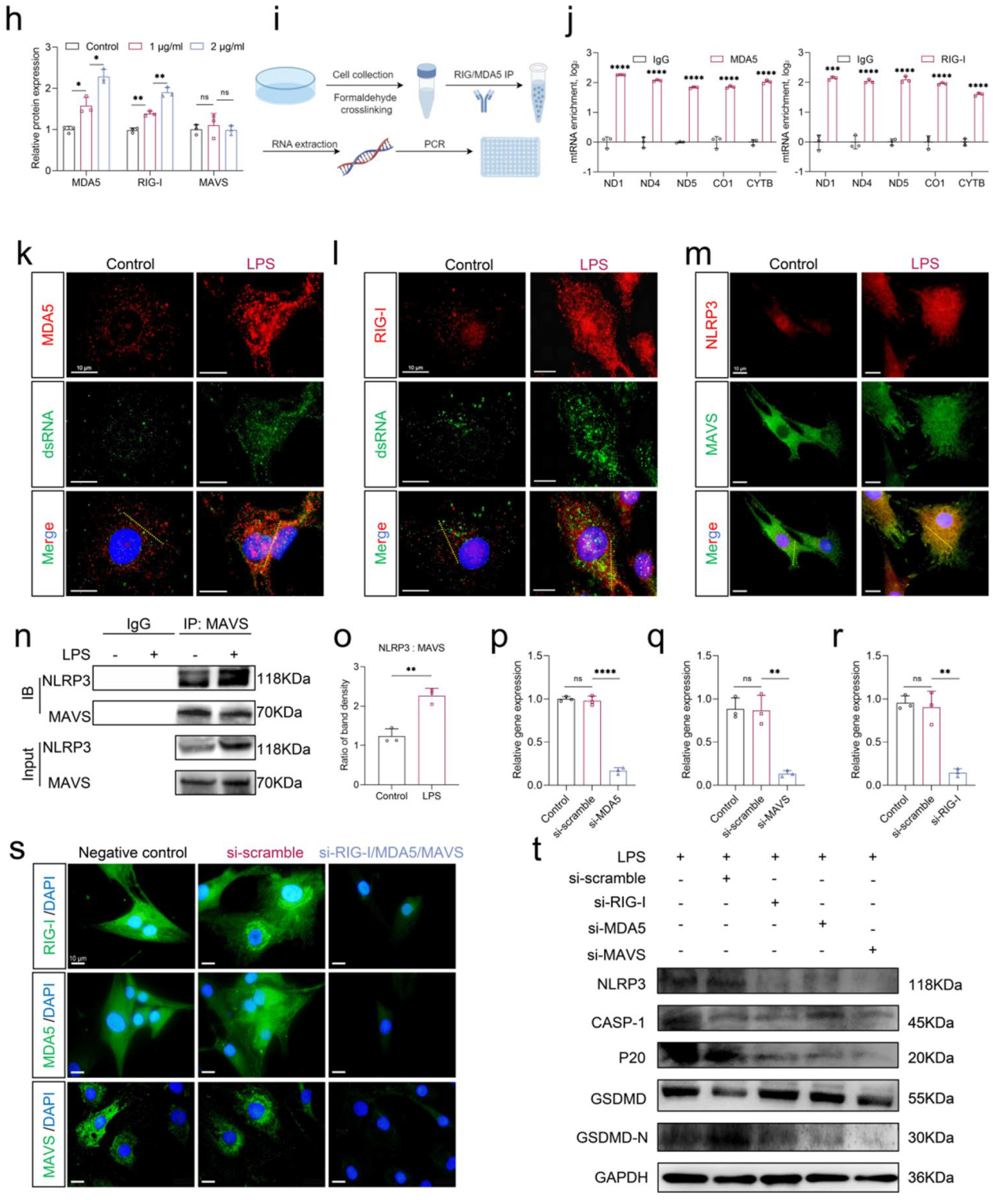
图2. mtdsRNA触发RLR-MAVS-NLRP3轴并促进细胞焦亡
三、抑制mtdsRNA的渗漏可缓解细胞焦亡
为探究mtdsRNA与细胞焦亡的关联,研究通过三种方式(敲低BAX、过表达PNPT1及IMT1处理)干预后观察焦亡程度。结果显示这三种干预均降低mtdsRNA与线粒体的共定位及荧光强度,证实其能够有效抑制mtdsRNA渗漏,同时qRT‒PCR实验也证实NPCs胞质中mtdsRNA含量降低。进一步检测了RLR-MAVS-NLRP3信号轴的激活状态,IMT1处理、BAX敲低和PNPT1过表达均有效减弱了MAVS与NLRP3的共定位,且NLRP3荧光强度明显降低,说明抑制了该信号轴的活化。CASP-1活性检测与ELISA分析则显示,抑制mtdsRNA泄漏能够显著降低NPCs的炎症反应。综上所述,抑制mtdsRNA能通过阻断RLR-MAVS-NLRP3信号轴有效缓解NPCs的焦亡过程。
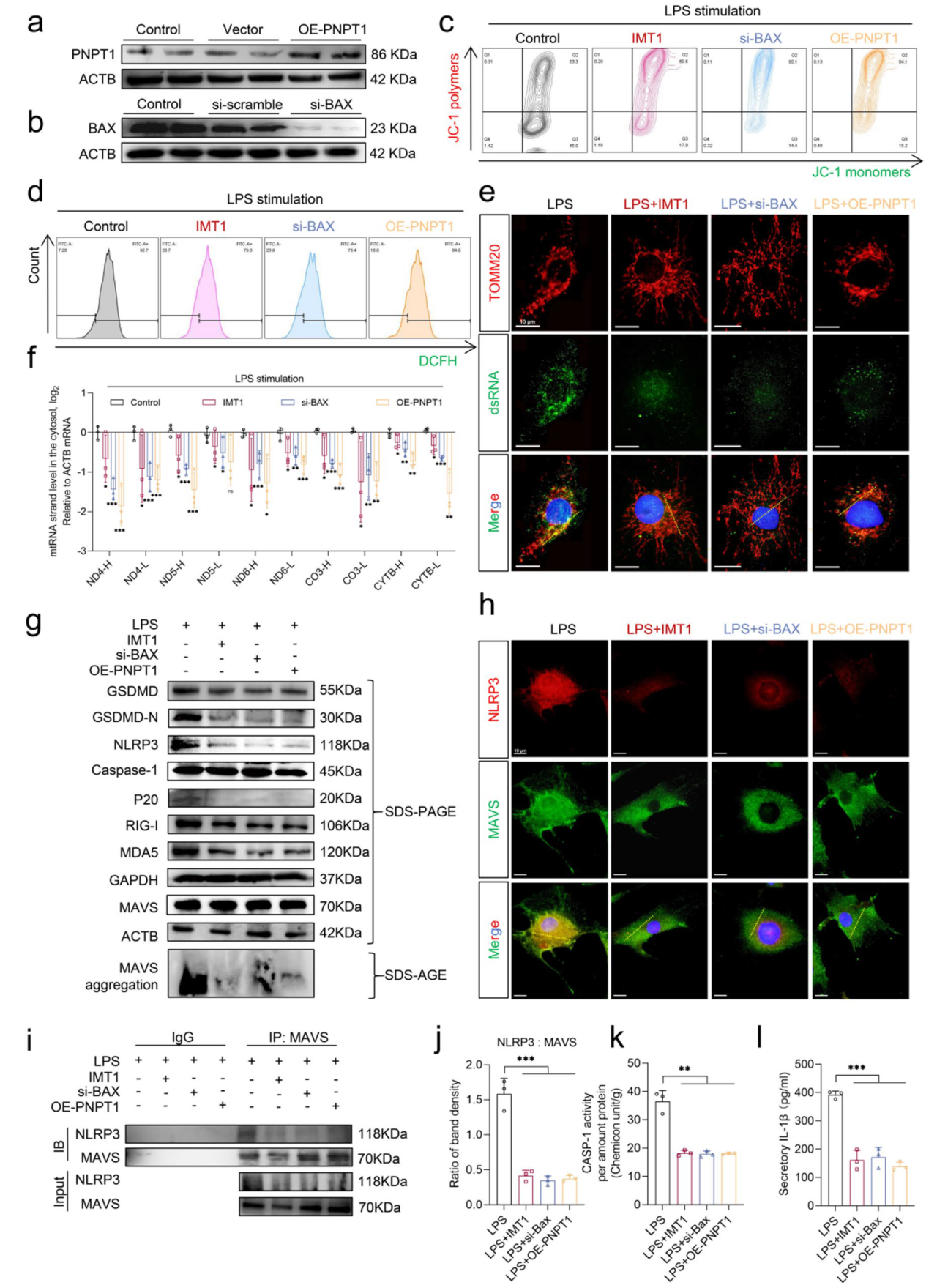
图3. 抑制mtdsRNA的渗漏可以缓解NPCs细胞焦亡
四、牛磺酸对于维持线粒体功能至关重要
为了进一步挖掘mtdsRNA的上游调控机制,研究采用非靶向代谢组学分析由LPS刺激引起的代谢物变化,发现牛磺酸与亚牛磺酸代谢通路受影响最为显著,验证实验也显示LPS处理可降低NPC中的牛磺酸含量。随后的研究发现,牛磺酸能减轻氧化应激、促进细胞增殖、维持线粒体健康,并通过抑制RLR-MAVS-NLRP3轴活化从而降低细胞焦亡程度,Co-IP进一步显示牛磺酸减少了NLRP3与MAVS的相互作用。总之,牛磺酸缺乏会诱发mtdsRNA泄漏,而外源性牛磺酸可通过维持线粒体功能完整并抑制焦亡通路。
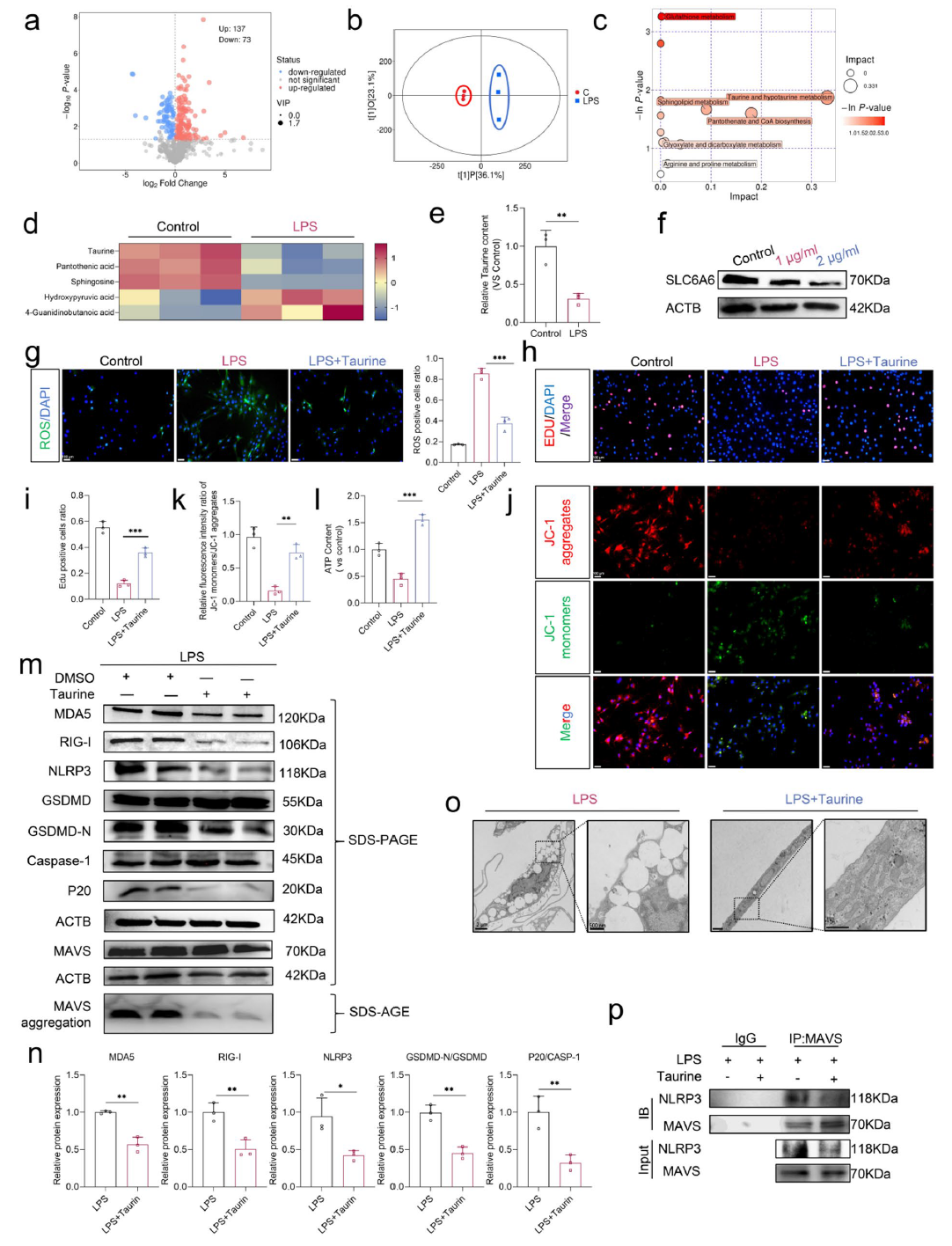
图4. 牛磺酸对于维持NPC线粒体功能的重要性
五、牛磺酸可以抑制mtdsRNA的渗漏
免疫荧光和qRT‒PCR分析发现,牛磺酸可有效抑制mtdsRNA的泄漏,为深入解析这一机制,研究构建了mtdsRNA渗漏模型,并通过转录组学比较模型组与牛磺酸处理组的差异基因表达。结果显示,牛磺酸降低干扰素刺激基因、炎症相关基因及氧化应激基因的表达,并恢复ROS解毒相关基因功能。功能富集也显示,牛磺酸抑制I型干扰素信号通路与炎症反应,同时增强细胞抗氧化损伤能力,上调线粒体自噬相关基因表达。因此,牛磺酸通过抑制mtdsRNA泄漏、调控自噬及相关信号通路,有效缓解氧化应激与炎症反应,发挥细胞保护作用。
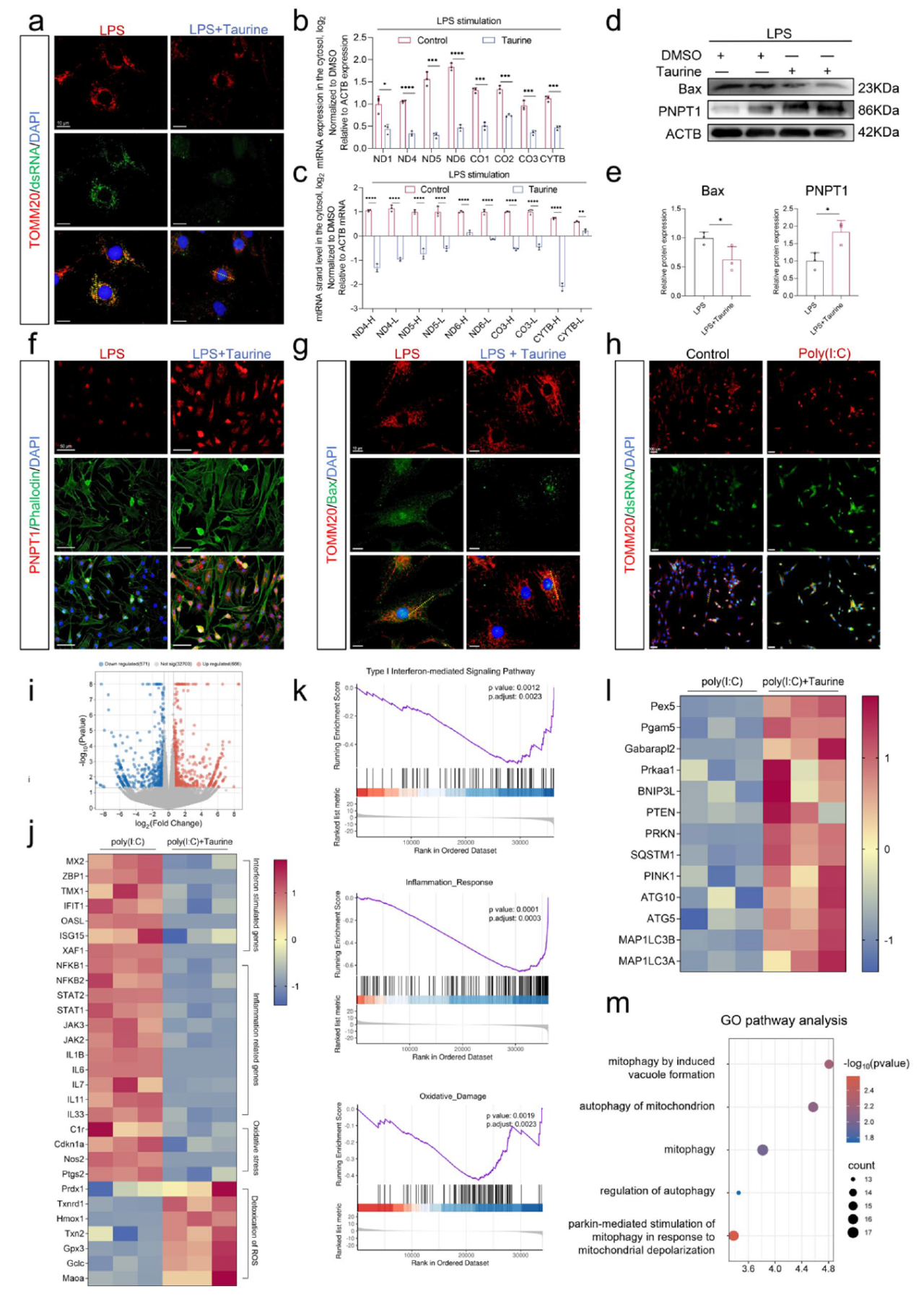
图5. 牛磺酸可以抑制mtdsRNA的渗漏
六、牛磺酸可以通过增强线粒体自噬来抑制mtdsRNA-MAVS-NLRP3轴
为进一步探究牛磺酸调控线粒体自噬的机制,研究采用了自噬抑制剂3-MA进行干预,发现3-MA处理可升高细胞内ROS水平,并削弱牛磺酸的保护作用,且逆转了牛磺酸在氧化应激下对线粒体膜电位的保护效应。WB与免疫荧光的结果显示,牛磺酸激活PINK1-Parkin通路以清除受损线粒体,而3-MA逆转该作用并抑制线粒体自噬水平。
对qRT‒PCR分析发现,3-MA引起胞质mtdsRNA积累。表明牛磺酸通过诱导线粒体自噬促进mtdsRNA清除,进而抑制RLR-MAVS-NLRP3信号轴活化,而3-MA处理可拮抗牛磺酸的保护效应。后续通过动物实验也证实,牛磺酸可以有效抑制dsRNA-MAVS-NLRP3的活化,在大鼠椎间盘退行性模型中具有明确的保护作用。
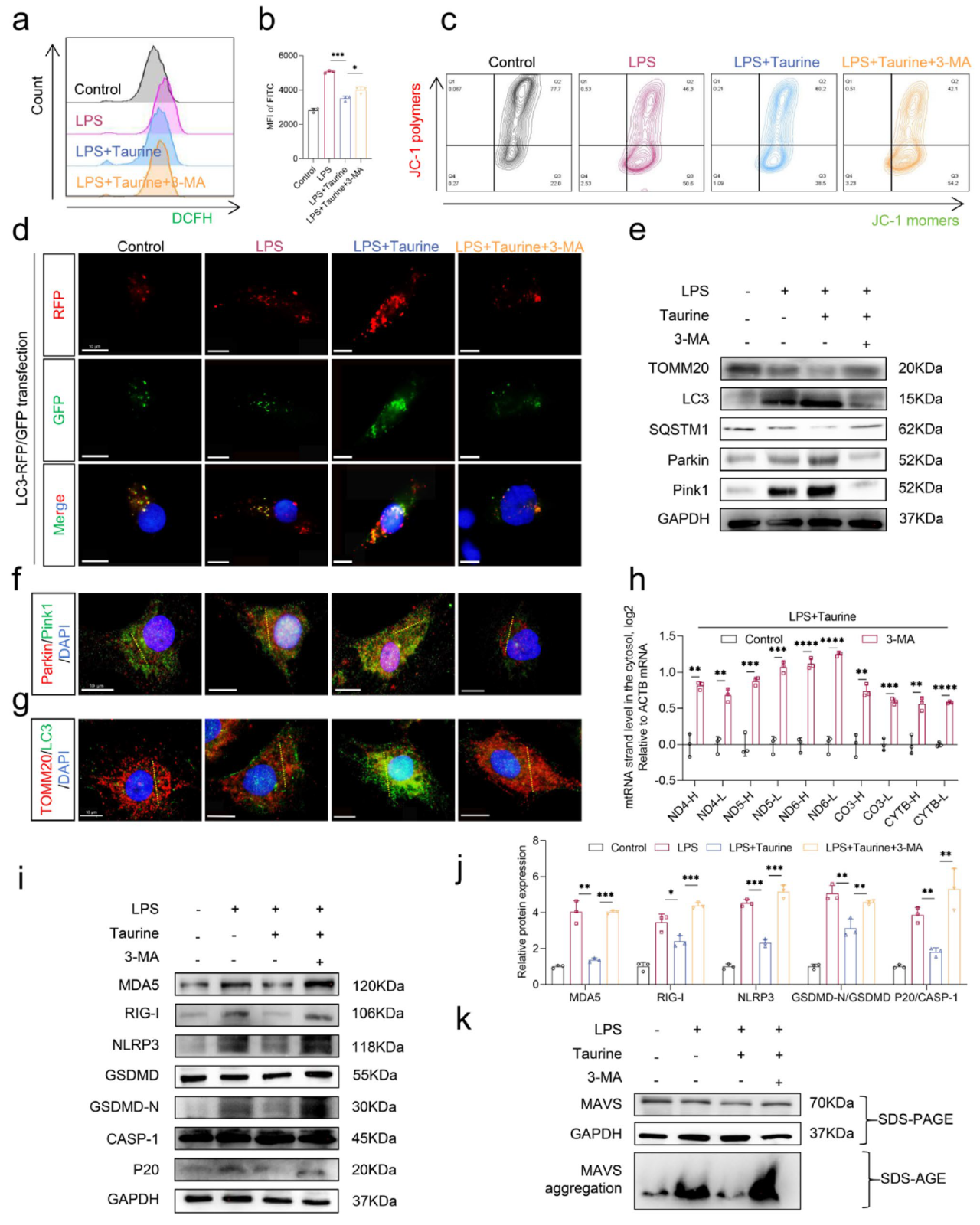
图6. 牛磺酸可以通过增强线粒体自噬来抑制mtdsRNA-MAVS-NLRP3轴
研究结论
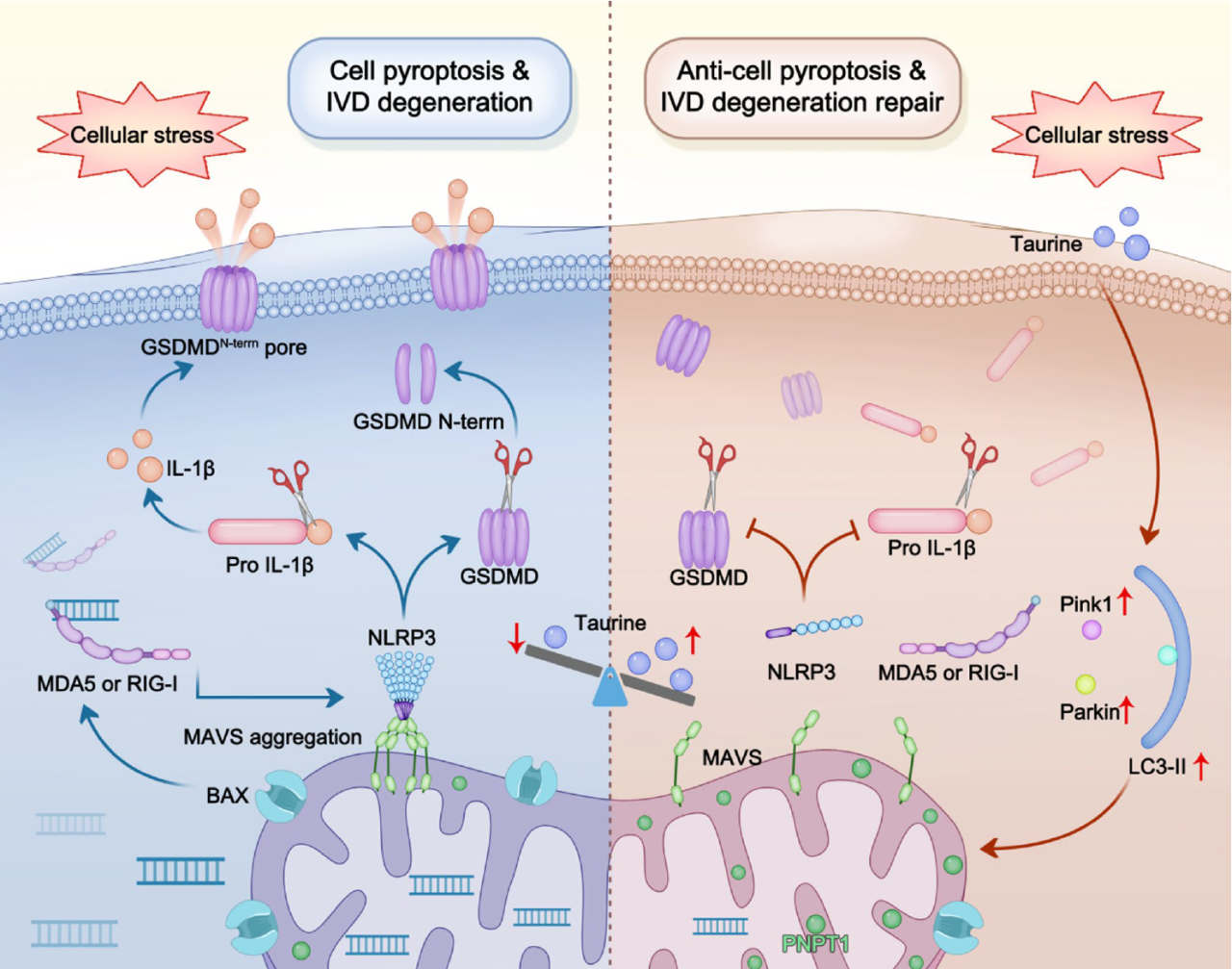
本研究系统阐明了mtdsRNA在椎间盘退变中的致病作用。研究发现,线粒体功能紊乱的髓核细胞会将过量mtdsRNA释放至胞质,激活RIG-I/MDA5受体并诱导MAVS发生寡聚化,进而招募NLRP3炎症小体,最终引发退变椎间盘组织中的细胞焦亡与炎症反应。退变过程中,髓核细胞中存在显著的牛磺酸缺乏,该代谢紊乱会通过破坏线粒体稳态加剧mtdsRNA的积累。而外源性补充牛磺酸可通过增强线粒体自噬抑制mtdsRNA释放,从而有效缓解NLRP3介导的细胞焦亡。这些结果确立了mtdsRNA作为IVDD进展的关键致病因子和治疗靶点,同时揭示通过牛磺酸进行代谢干预的治疗潜力。
参考文献
Ou Z, Wei J, Tong B, Lei J, Liang H, Zhu D, Wang H, Zhou X, Wu D, Xu H, Du Z, Du Y, Peng S, Zhang X, Yin H, Wang K, Yang C, Liao Z. Taurine can restrict MtdsRNA mediated pyroptosis by enhancing mitophagy in nucleus pulposus cells. Cell Commun Signal. 2025 Oct 9;23(1):423.
青莲百奥合作文章
青莲百奥深度参与众多前沿研究,与中国医学科学院、中国科学院、军事医学研究院、国家蛋白质科学中心、四川大学华西医院等顶尖科研机构通力合作,累计发表SCI论文近200篇,累计影响因子(IF)超1500。多项重磅研究成果发表于《Nature》《Science Translational Medicine》《Nature Communications》等国际顶级期刊。
