抗生素耐药性日益严重,耐甲氧西林金黄色葡萄球菌(MRSA)已经成了临床的噩梦 。今天分享的这篇青莲百奥项目文章是一篇典型类似老药新用思路的作品,讲的是如何用TPP技术解释抗癌药候选者SC-43把超级细菌MRSA给饿死的机制。接下来我们一起看看他们都做了什么吧。

标题:SHP-1 agonist SC-43 limits methicillin-resistant Staphylococcus aureus infection through inhibition of heme biosynthesis(SHP-1激动剂SC-43通过抑制血红素生物合成限制耐甲氧西林金黄色葡萄球菌感染)
作者:深圳市人民医院检验科黄维团队、陆军军医大学邹全明/李海波团队、中山大学·深圳李锡涛团队
发表期刊:EMBO Molecular Medicine(IF=8.3)
发表日期:2026年4月10日
北京青莲百奥生物科技有限公司为文章提供了TPP技术
研究背景
本研究的主角是SC-43和MRSA。
1. SC-43是一个正在进行临床试验的SHP-1激动剂,而SHP-1是个抑癌基因,所以SC-43原本主要在抗肿瘤和抗纤维化领域应用。
2. MRSA广谱耐药,普通的抗生素如β-内酰胺类和头孢之类的已经对它没啥作用。目前临床上唯一的守门员是万古霉素,属于是最后一道防线,所以急需一个新的药物对付MRSA。
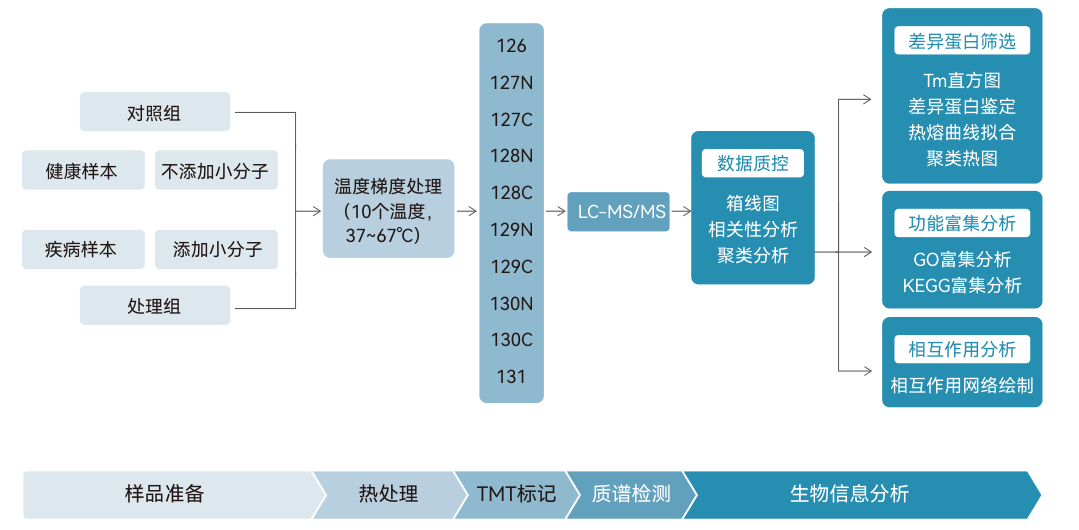
3. TPP (Thermal Proteome Profiling)中文名叫热蛋白质组学,利用蛋白受热容易变性析出的原理,筛选与药物结合的靶蛋白。TPP也是一种钓靶技术,做药物研究的老师可能比较熟悉(同类型的技术还有LiP-MS等,青莲百奥可提供)。
研究思路
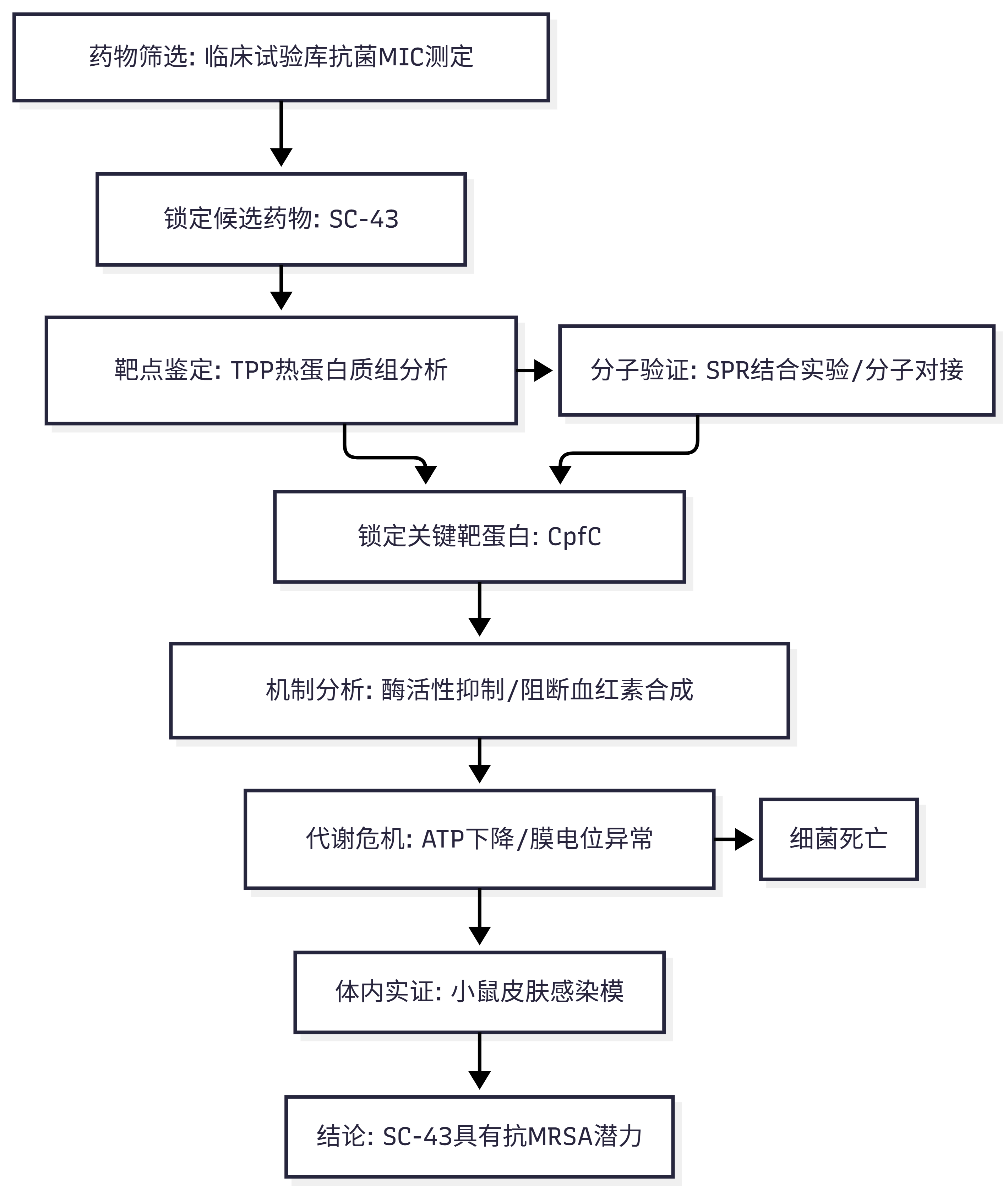
研究结果
1.标准开场:化合物库挖掘
文章以老药新用(Drug Repurposing)开头,也就是归纳法穆勒五法中的求同求异法,从一堆还在临床试验中的化合物里找能杀菌的。结果发现在930个化合物中,原本用来抗癌/抗纤维化的化合物SC-43居然对MRSA有奇效,MIC(最低抑菌浓度)<0.625 µg/mL。作为对比,美国CLSI认为万古霉素对临床分离的MRSA菌株MIC>2µg/mL时应采用替代药物治疗。

表S1(节选):I-III期临床试验药物对MRSA的MIC筛选
随后杀菌实验验证了一下,发现SC-43专杀革兰阳性菌(比如MRSA、屎肠球菌),对大肠杆菌等革兰阴性菌无效,说明SC-43的靶点可能是阳性菌特有的或必需的。
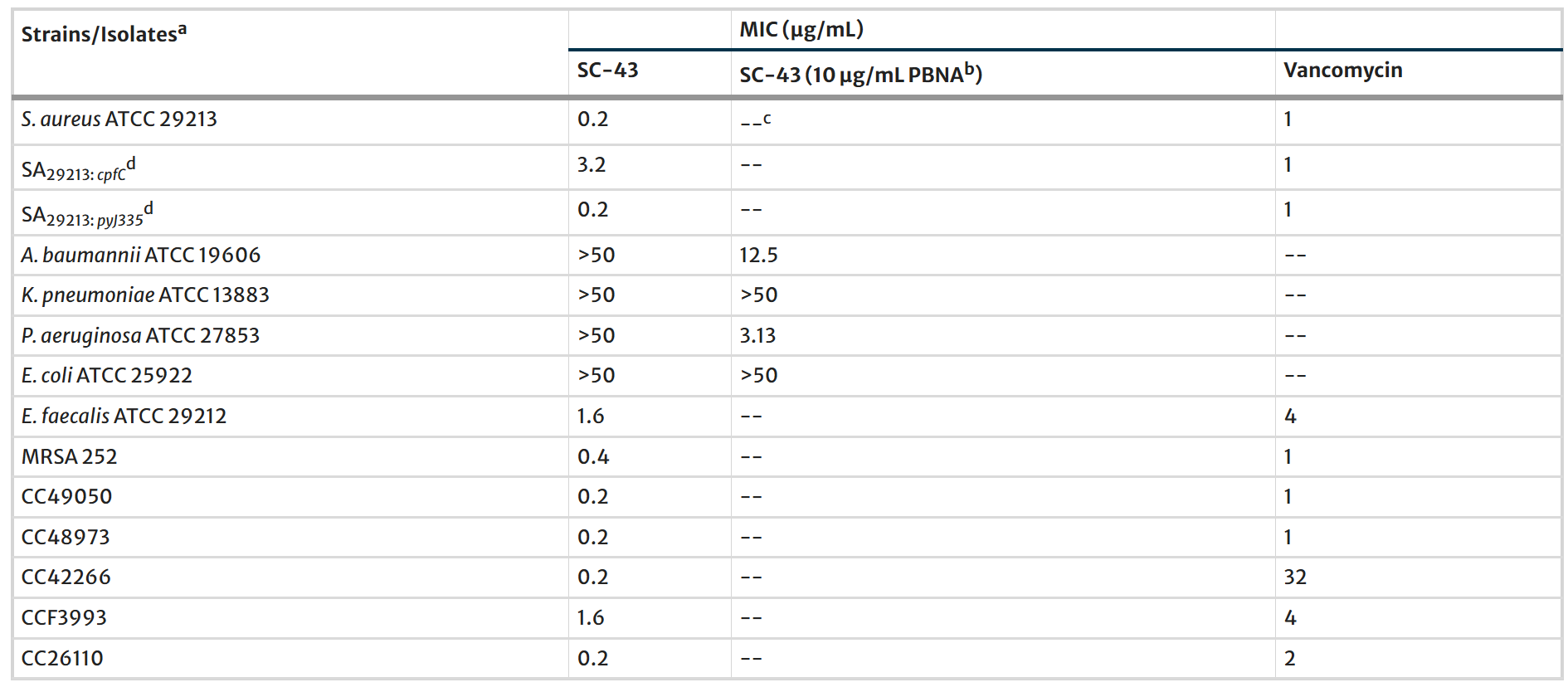
表1:SC-43对革兰阳性菌与阴性菌的抗菌活性评价
2.TPP筛选SC-43的特异性靶蛋白
为了找靶蛋白,作者用了热蛋白质组学(TPP)。简单说,就是给细菌加热,看哪个蛋白在药物处理后耐热程度变化了。结果显示9个蛋白热稳定性上升(图1B),经过一系列筛选过程(无非就是看看阳性菌必需而阴性菌不必需的蛋白),发现CpfC蛋白的热变性温度(Tm值)升高了(图1C),说明CpfC是SC-43的潜在结合靶蛋白。为此他们做了个重组蛋白SACpfC,通过表面等离子共振(SPR)验证了这一点(图1D)。CpfC蛋白是细菌粪卟啉依赖性途径(CPD)中的关键酶,而CPD的作用是合成血红素(图1A),维持细菌能量代谢和氧化还原平衡,是MRSA在缺氧环境下生存的重要法器。
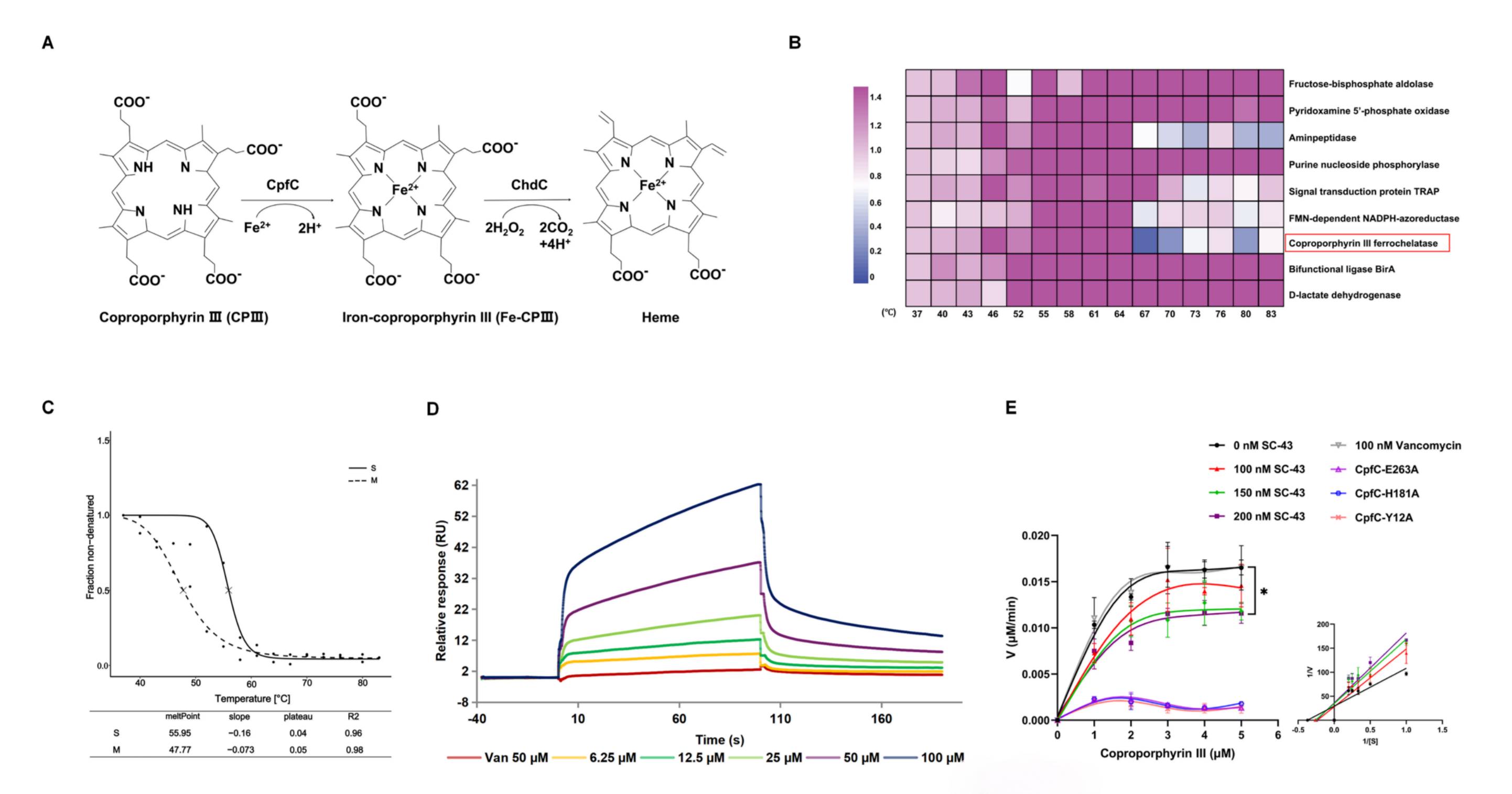
图1:SC-43对CpfC的抑制作用
3.机制探索:SC-43结合CpfC后细菌发生了什么?
既然是酶,作者首先是测了下CpfC酶活性在SC-43处理后有无变化。亚铁螯合酶活性测定结果发现,SC-43以剂量依赖方式抑制了CpfC的酶活(图1E)。由于CpfC的作用是促进合成血红素,而血红素是细菌呼吸链中的重要成员,他们又测了一下细菌里的血红素和ATP水平,SC-43处理后果然都下降了(图2A-B),甚至出现了膜电位超极化(图2D)。到这里已经可以画一个初步的故事线:SC-43抑制CpfC活性→血红素合成受阻→呼吸链崩溃→细菌能量失调死亡。当然,如果这时候加一个拯救实验就更好了。好在作者也想到了,在培养基添加外源血红素(heme),SC-43的杀菌效果被逆转(图2C),更进一步证实SC-43调控血红素合成来杀菌。
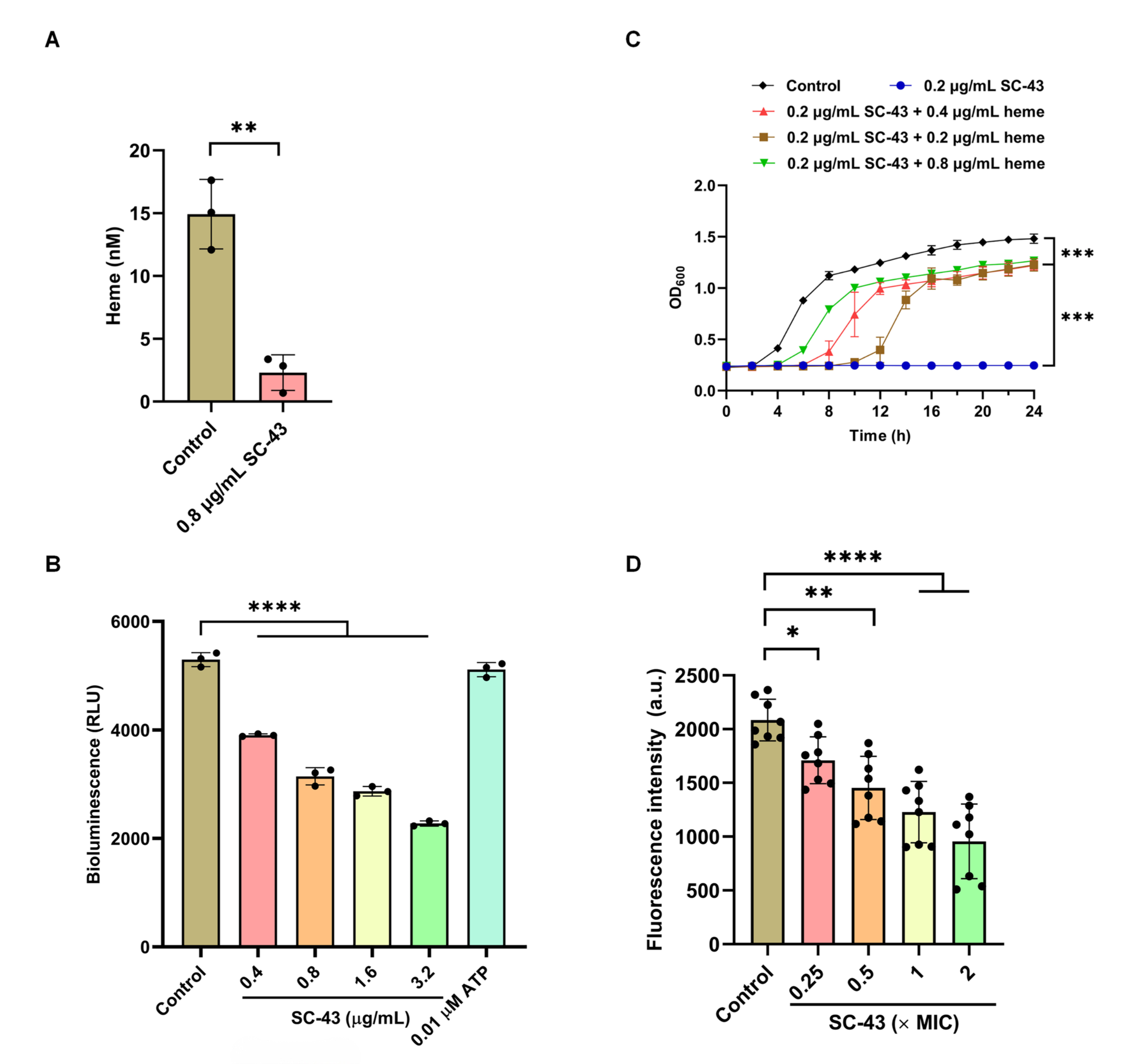
图2:SC-43对血红素生物合成及相关功能的影响
4.结构生物学看SC-43和CpfC的结合位点
光知道SC-43和SACpfC有结合还不够,还得知道他们在什么位置结合(可能为了证明特异性,也可能为方便设计更特异的药)。因此他们解析了SACpfC的晶体结构(分辨率还挺高,2.19 Å),序列和结构比对发现CpfC在革兰阳性菌中保守(图没放,在原文图4),并且做了分子对接(Docking)和分子动力学模拟(MD),发现SC-43完美地卡在了CpfC的活性口袋里,和Tyr12、His181和Glu263形成了氢键等互作(图5)。三个位点突变成Ala后,SPR和分子对接的亲和力大幅下降(图S2, 表2),同时CpfC铁螯合催化能力消失(图1E),证实SC-43通过与活性位点竞争性结合来抑制CpfC的功能。
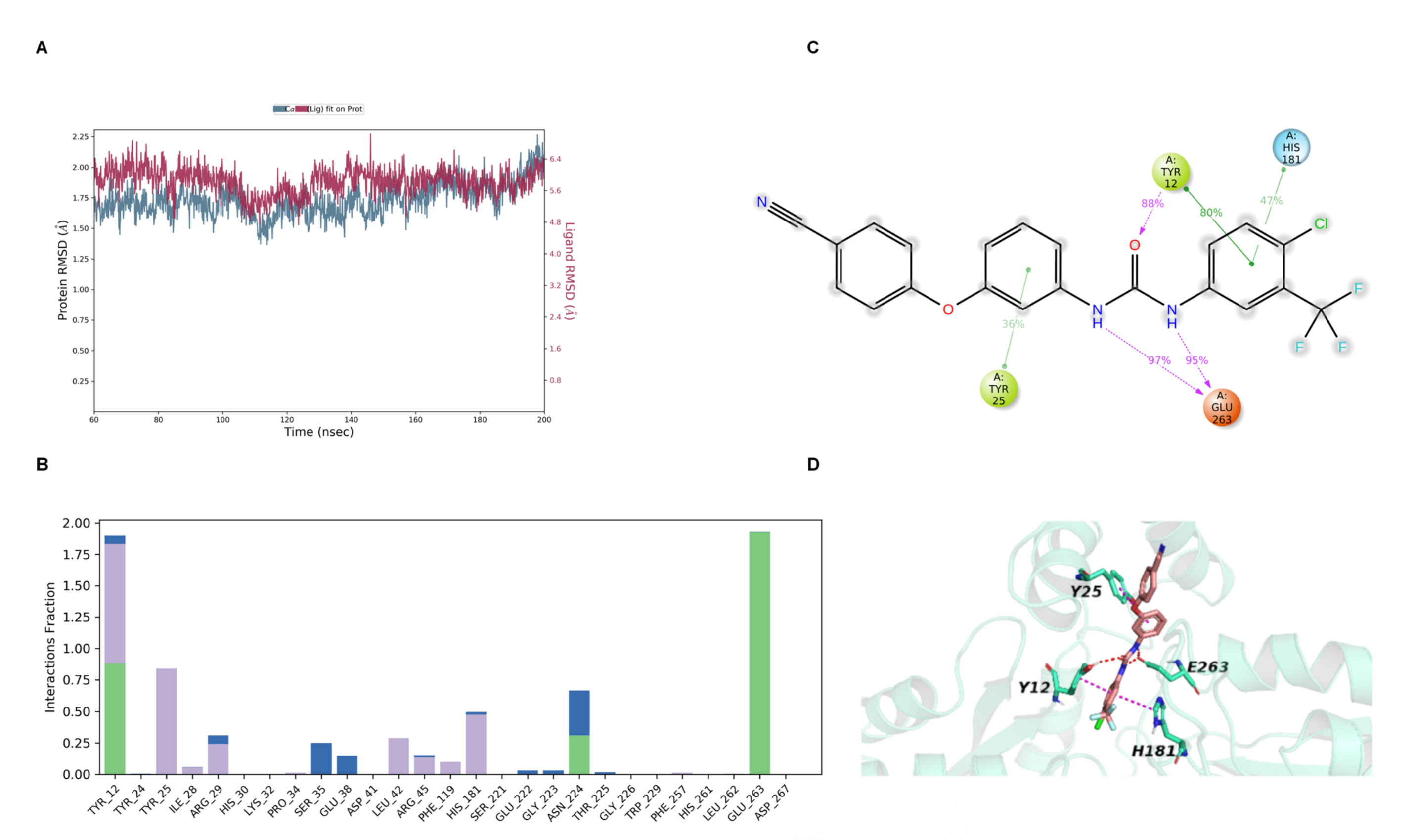
图5:SC-43和SACpfC分子对接和分子动力学模拟
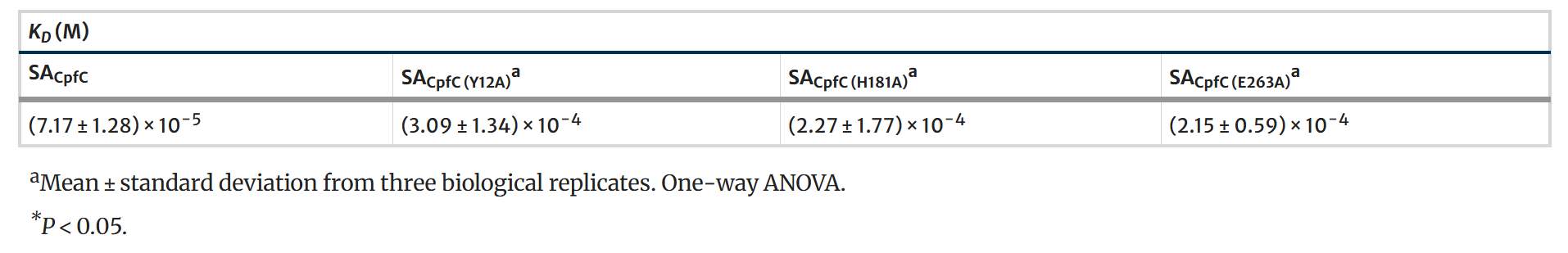
表2:SACpfC野生型和突变体的SPR分析
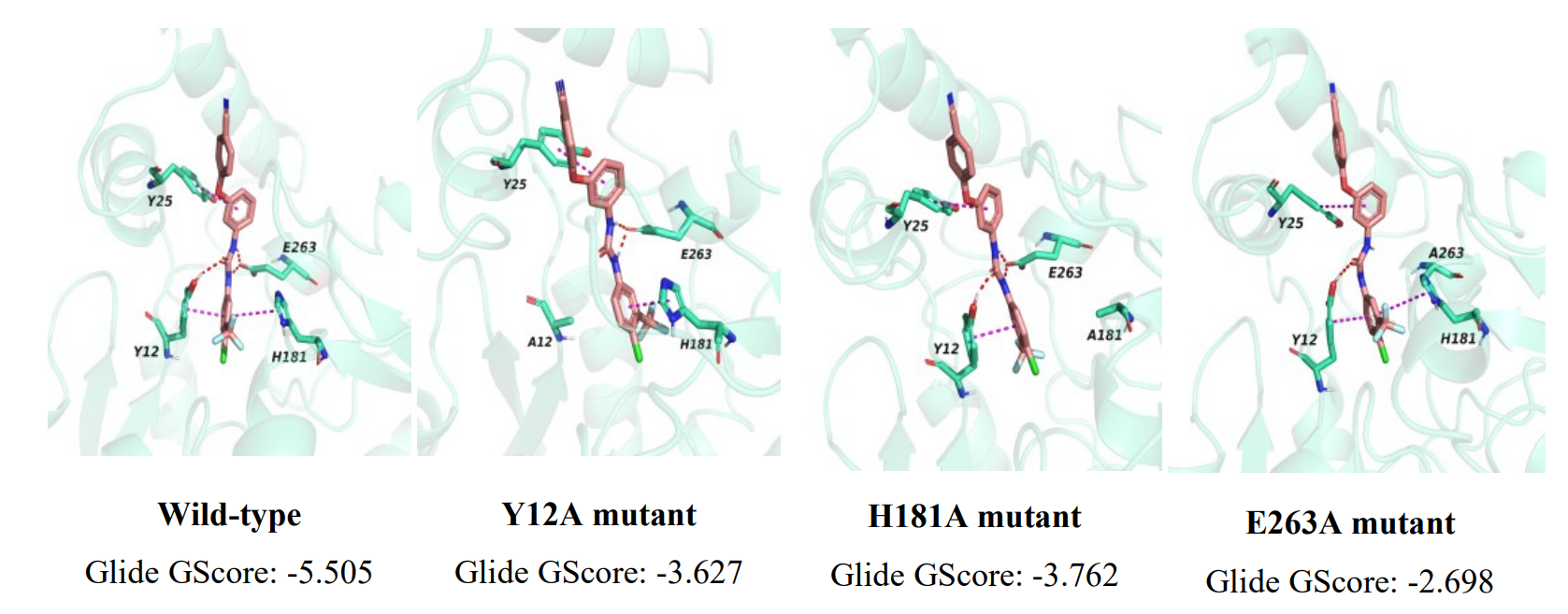
图S2:SACpfC野生型和突变体的分子对接
5.SC-43在小鼠感染模型中的疗效
机制解释得差不多,是时候证明药物能用了。作者在MRSA皮肤伤口感染小鼠模型上做了实验,SC-43确实能促进伤口愈合、大幅降低伤口的载菌量,效果与临床常用药莫匹罗星(Mupirocin)相当甚至更好,初步说明能用,有待临床转化。
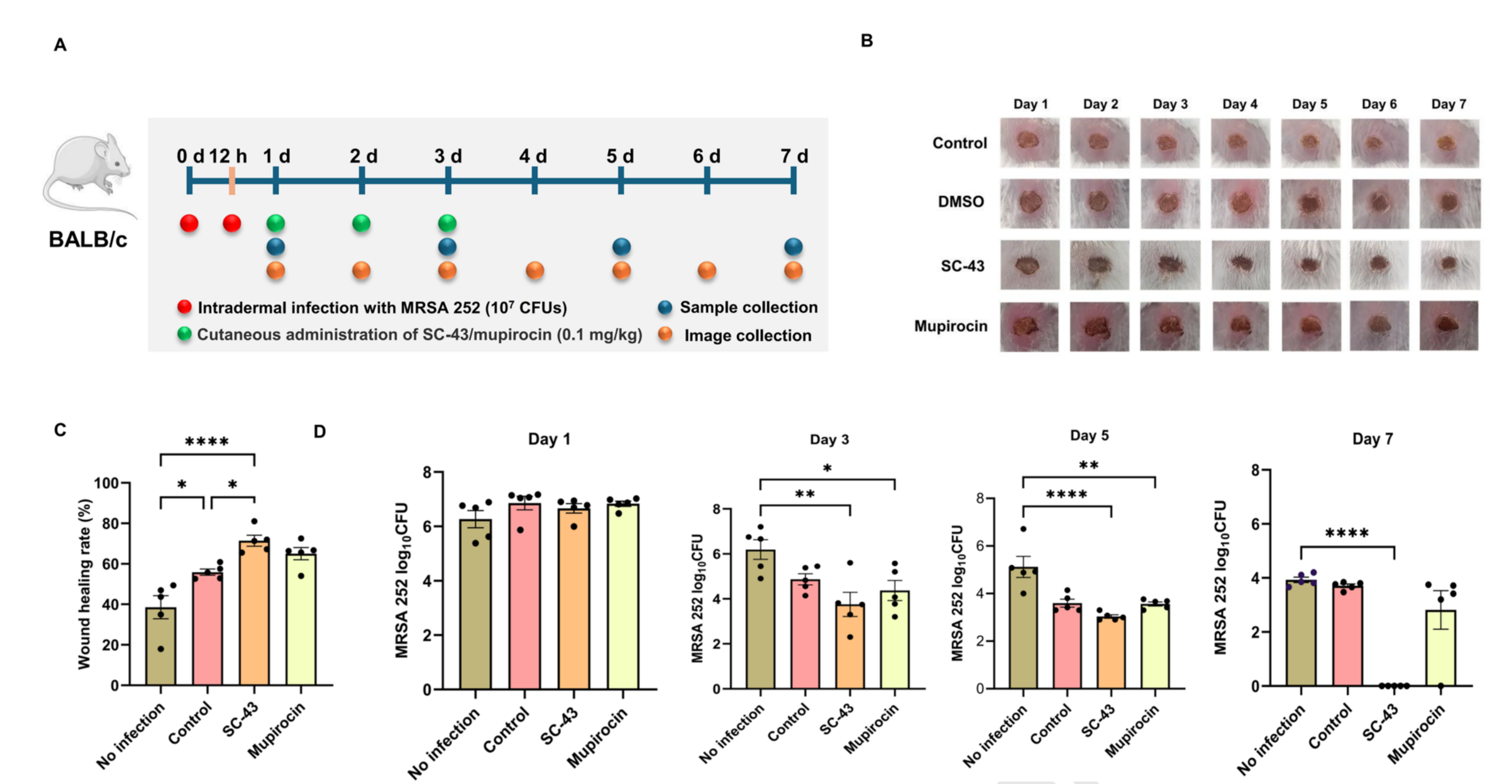
图6:小鼠模型验证SC-43对MRSA的疗效
总结
这篇文章的核心思路,可以概括为:一筛、二找、三验证。第一步筛出来有效的化合物SC-43,用的是正在临床试验中的化合物库,安全性得到保障。第二步找化合物对应的靶蛋白,用到TPP技术像吸铁石一样将靶蛋白CpfC找出来,非标记技术不用在化合物上加探针,准确性很高。第三步验证SC-43和CpfC结合,以及作为细菌合成血红素的关键酶,CpfC的功能被SC-43抑制,最后在小鼠模型上确证,形成完整的故事:SC-43靶向革兰阳性菌CpfC蛋白→抑制血红素合成→破坏能量代谢→导致细菌死亡。
原文链接:点击直达>>>项目文章 | 热蛋白质组学(TPP)锁定老药“饿死”超级细菌金葡的新靶点
一站式药物筛选平台
黄维教授团队与青莲团队联手打造一站式创新型高通量抗菌药物筛选平台,为解决临床问题,开展先导化合物药物筛选及优化、创新药物临床前开发、确证药物靶点等核心技术,共同提供强有力的支撑。
青莲百奥解决方案
青莲百奥与TPP的渊源起于2019年
国内首家提供TPP药物靶点服务
国内首家与客户合作发表研究成果实现转化
5年发展积累近百个项目经验
青莲百奥不断创新,推出升级服务,致力于将先进技术转化为具有实际价值的成果。青莲百奥始终与客户携手前行,共同探索和发展药靶研究技术。