植物中的效应子触发免疫(ETI)是由细胞内核苷酸结合富亮氨酸重复序列受体(NLRs)介导的,这些受体通过钙离子(Ca2+)信号通路发挥作用。然而,NLR诱导的Ca2+信号如何启动下游免疫反应,如增强活性氧(ROS)信号传导,目前仍不清楚。
今年9月3日,浙江大学生物技术研究所梁岩/林福呈团队于Molecular Plant (IF=24.1)杂志上发表了题为“CPK12 decodes effector-triggered calcium signaling and phosphorylates PIP2;1 to facilitate apoplastic ROS transport into the cytoplasm in Arabidopsis”的研究论文。该研究基于拟南芥植株样本进行全方位的分析和探索,发现当植物遭受非致病性细菌感染时,CPK12会以Ca2+依赖的方式被激活,并通过对PIP2;1的磷酸化修饰,使得细胞外ROS进入细胞质,在NLR介导的Ca2+信号传导与植物免疫中ROS反应的空间调控之间建立了关键分子桥梁。揭示了CPK家族成员在调控免疫信号区室化过程中的功能特异性。
北京青莲百奥生物科技有限公司为该研究提供了蛋白质组学检测服务。
研究结果
一、Ca2+依赖的CPK12有助于调节ETI-ROS信号
研究团队首先系统分析了CPK所有的突变体,确定其中CPK12是调控ETI-ROS信号通路的关键激酶。为了验证cpk12表型确实由CPK12基因突变引起,研究构建了FLAG标签融合CPK12的互补植株,并筛选出两个独立株系进行后续分析。转基因植株的ETI-ROS水平与野生型相当,但cpk12突变株比野生型更易感病,而CPK12-FLAG转基因植株则完全恢复了抗性。GFP标签融合的CPK12也成功互补了cpk12突变体表型。说明CPK12在ETI-ROS信号传导及植物抗病性中发挥重要作用。
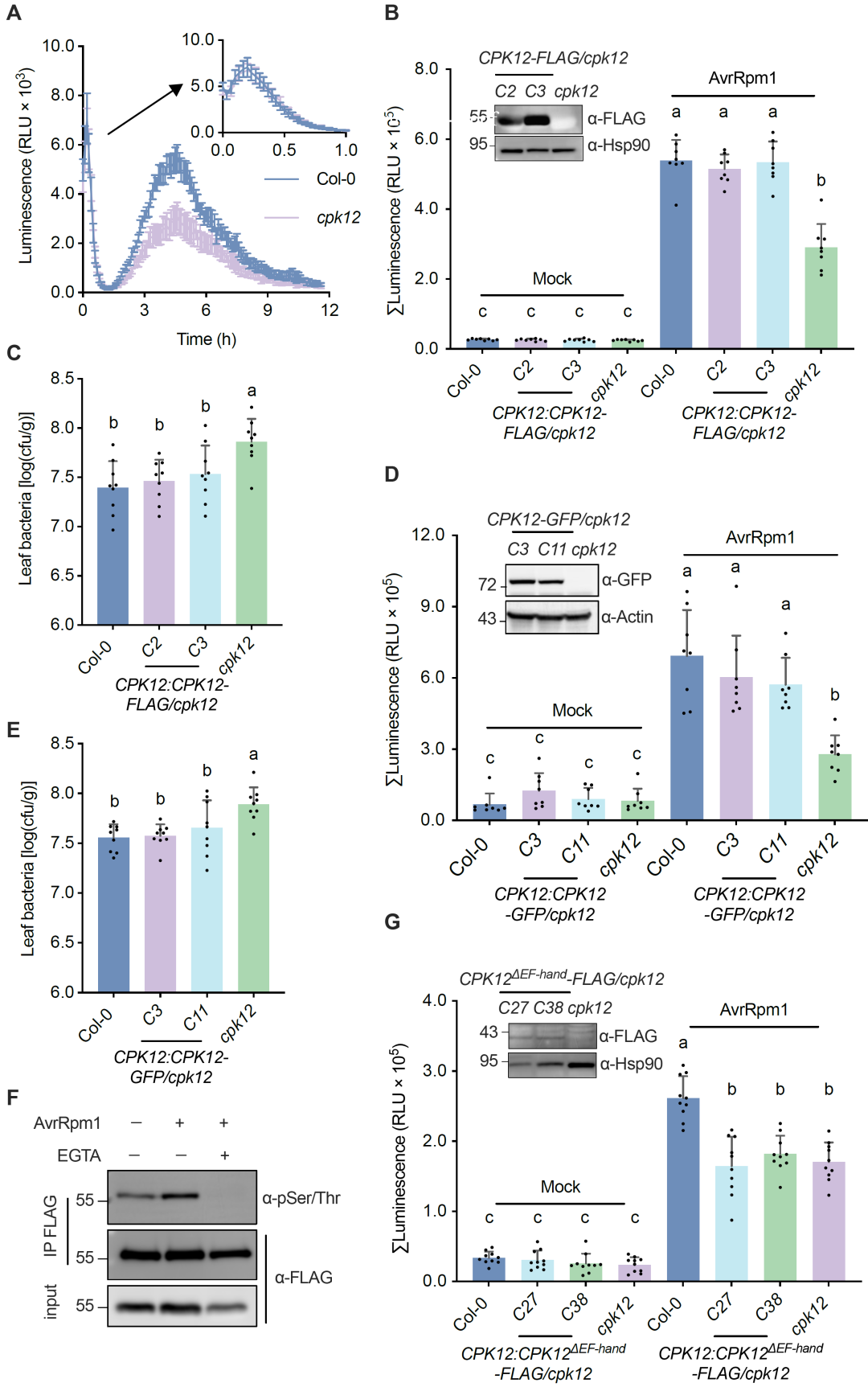
图1. 钙依赖性CPK12在调节ETI-ROS水平中发挥作用
为探究CPK12在ETI过程中的调控机制,研究团队基于转基因植株,检测了经无毒菌株Pst DC3000(avrRpm1)处理后的CPK12-FLAG磷酸化水平。通过FLAG磁珠IP富集CPK12-FLAG蛋白,并采用pSer/Thr抗体进行WB分析,发现无毒菌株处理显著增强了CPK12的磷酸化。此外,CPK蛋白通过其保守的EF-hand结构域结合Ca2+,研究也发现,完整的EF-hand结构域对于CPK12在ETI过程中依赖Ca2+激活并调控ROS爆发至关重要。
二、CPK12调节ETI-ROS转运
为了探究CPK12在ETI-ROS调控中的作用,研究对接种无毒菌株后4小时比较了cpk12突变体与野生型中RBOHD的蛋白丰度及其在S343/S347位点的磷酸化水平,但未发现显著差异。体外激酶实验也发现,CPK12并非通过调控RBOHD的活性来影响ETI-ROS信号。研究也讨论了氧化氢酶(CAT)、抗坏血酸过氧化物酶(APX)和谷胱甘肽过氧化物酶(GPX)等酶在这一过程中的作用,结果表明CPK12也不是通过调控ROS清除酶的表达来影响ETI-ROS信号。
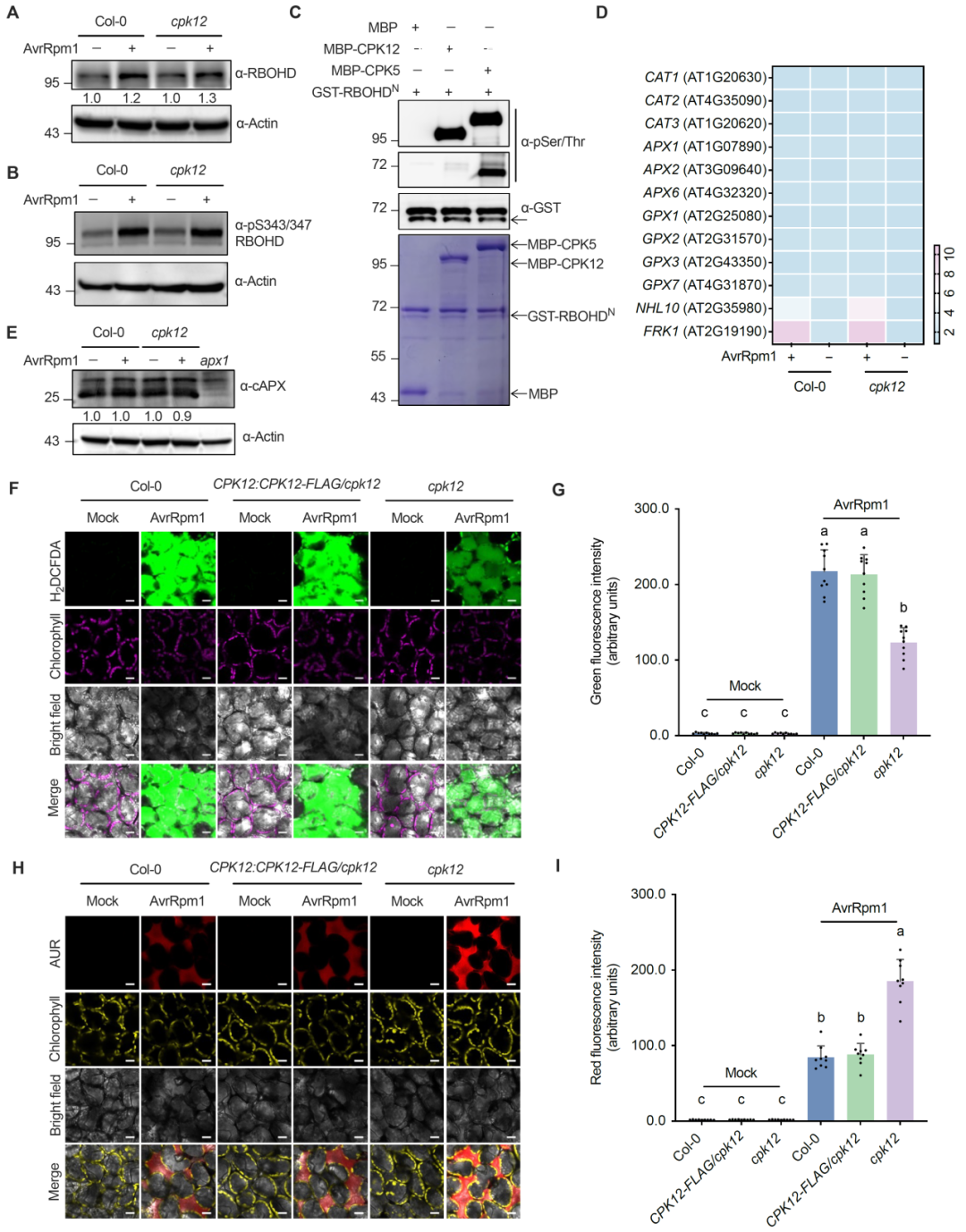
图2. 钙依赖性CPK12在调节ETI-ROS水平中发挥作用
基于上述发现,本文进一步探究了CPK12是否调控ROS从质外体向细胞质的转运,通过荧光标记(H2DCFDA)染色发现,野生型叶片经无毒菌株处理后呈现强烈的绿色荧光信号,而模拟接种对照组无此现象,同时cpk12突变体的胞质荧光强度显著低于野生型,而互补植株则完全恢复至野生型水平。结果表明,CPK12可能通过促进ROS从质外体向细胞质的转运来调控ETI-ROS信号,而非影响其产生或清除过程。
三、PIP2;1负责ETI-ROS的运输
水通道蛋白PIPs可介导质外体H2O2跨膜转运至细胞质。为探究PIP蛋白是否与CPK12互作,研究通过免疫共沉淀富集CPK12-FLAG蛋白复合物,并利用液相色谱-串联质谱(LC-MS/MS)进行分析,鉴定到四个水通道蛋白家族成员:PIP1;1、PIP1;3、PIP1;5和PIP2;1。其中,仅PIP2;1被证实具有H2O2转运能力。随后研究显示显示,无毒菌株诱导的ETI-ROS水平在pip2;1-1突变体中显著低于野生型,而由其自身启动子驱动的PIP2;1-HA转基因可完全恢复ROS至野生型水平。通过染色分析也发现,pip2;1-1突变体表现为胞内ROS降低而质外体ROS积累的区室化失衡特征,说明PIP2;1确有可能参与调控ETI-ROS从质外体向细胞质的转运过程。
随后研究利用CRISPR/Cas9技术构建了另外两种pip2;1突变体株系,pip2;1-4和pip2;1-17的转录水平略高于pip2;1-1突变体,但所有pip2;1突变体中PIP2;1蛋白均低于免疫印迹检测阈值,且都表现出显著降低的ETI-ROS水平以及对无毒菌株感染的感病性增强。这些结果共同表明,PIP2;1通过介导ETI-ROS转运,正向调控植物对无毒菌株的抗性。
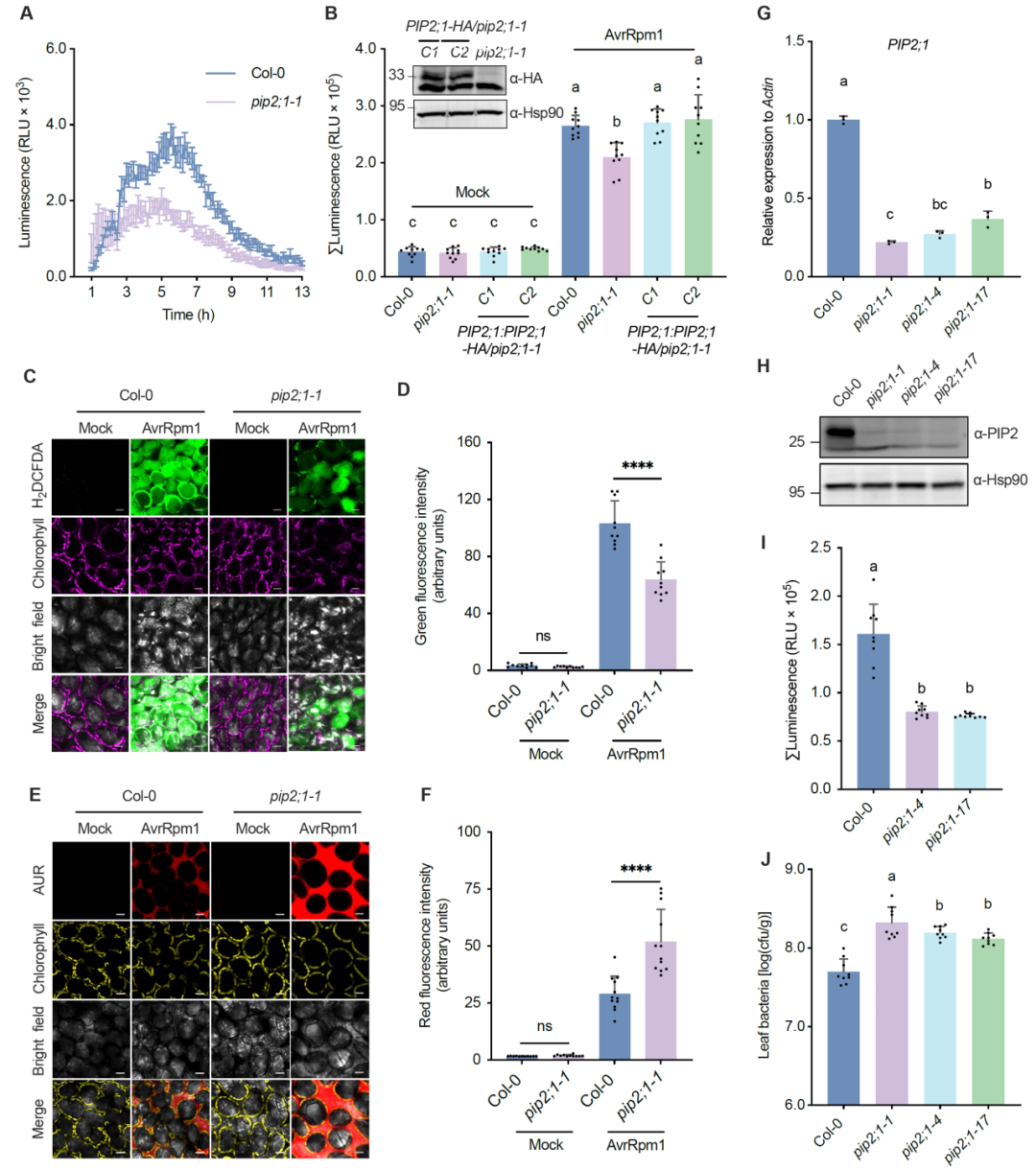
图3. PIP2;1负责ETI-ROS的运输
四、在ETI过程中CPK12-PIP2;1相互作用增强
为探究PIP2;1与CPK12的蛋白互作关系,研究在本氏烟草叶片中进行了分裂荧光素酶(LUC)互补实验,证实了有强烈的阳性信号,也通过抗LUC抗体免疫印迹验证了蛋白表达。而双分子荧光互补(BiFC)技术也同样证实了这两个蛋白之前存在明显的相互作用。
研究进一步进行了coIP,发现PIP2;1可与CPK12-FLAG共沉淀,且不与阴性对照ALF5-FLAG结合。无毒菌株感染增强了PIP2;1与CPK12-FLAG的特异性互作,共沉淀的PIP2;1蛋白量显著增加,有毒力菌株则未对该互作产生影响。
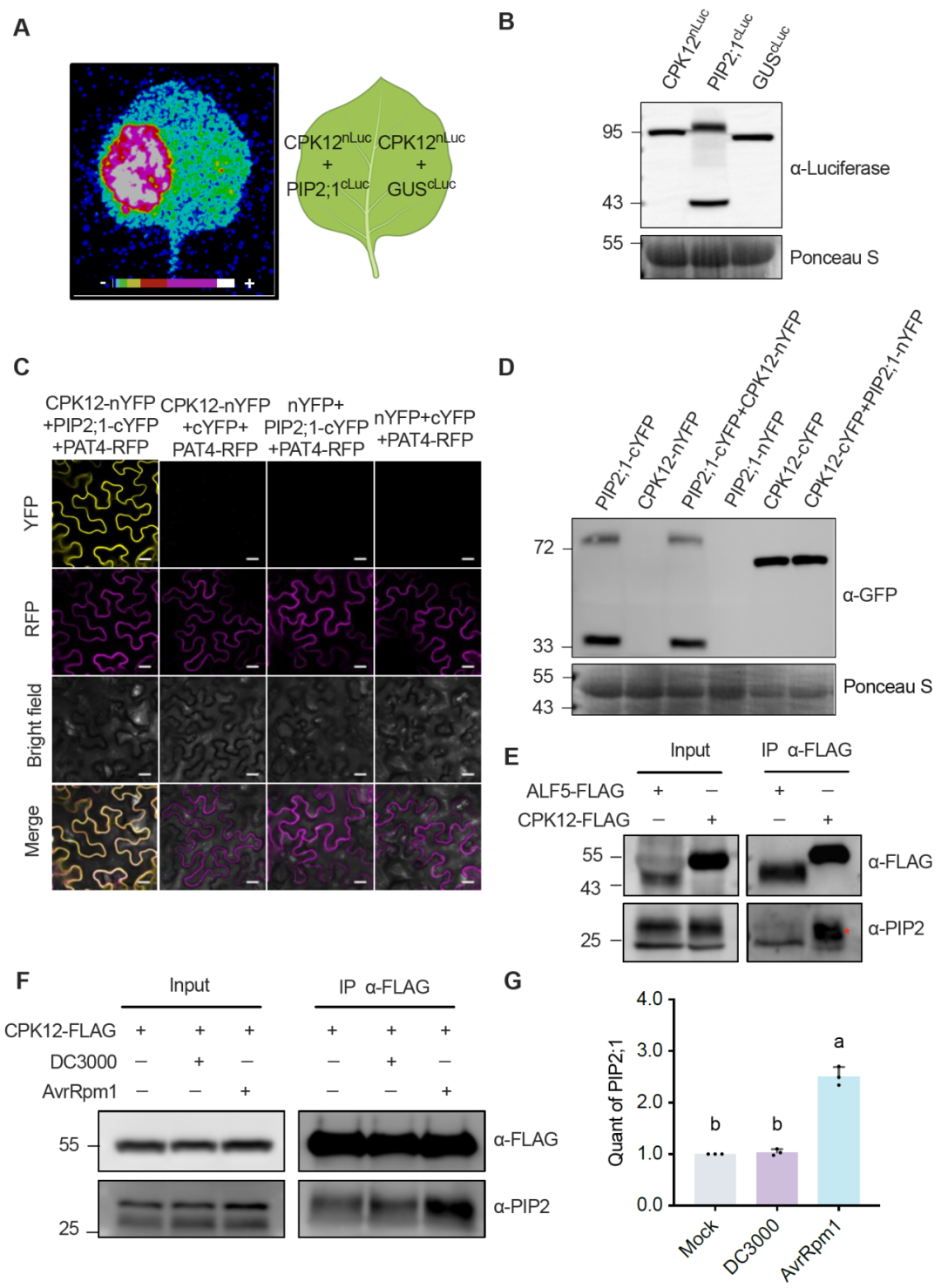
图4. 无毒菌株处理增强CPK12-PIP2;1相互作用
五、CPK12磷酸化PIP2;1的残基S280和S283
亚细胞定位显示,PIP2;1在cpk12突变体与野生型中均定位于细胞膜,接种无毒菌株后1小时的PIP2;1蛋白水平也无显著变化,说明在ETI早期阶段,CPK12既不调控PIP2;1的亚细胞定位,也不影响其蛋白丰度。为了鉴定CPK12磷酸化PIP2;1的具体区域,研究团队分别克隆并融合了PIP2;1的不同片段进行体外激酶实验,并通过抗pSer/Thr抗体免疫印迹检测磷酸化信号。结果显示,CPK12表现出强烈的自磷酸化活性,并能够特异性磷酸化PIP2;1的C端区域。PIP2;1的C端区域包含五个丝氨酸(S)残基,其中S280和S283在被子植物中高度保守,转基因也验证了这两个位点的磷酸化对PIP2;1在ETI-ROS转运中的功能至关重要。
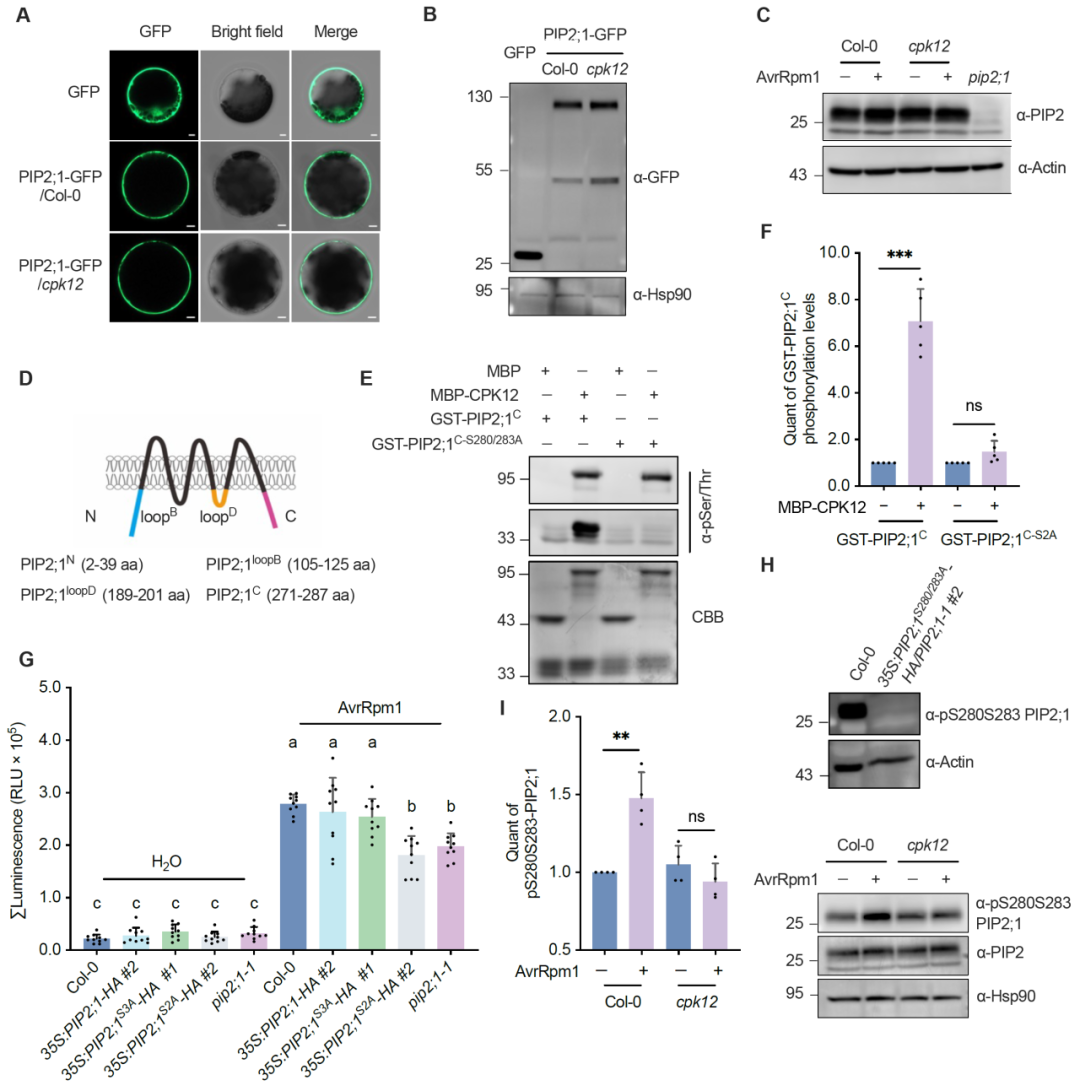
图5. CPK12磷酸化PIP2;1的残基S280和S283
进一步通过体外磷酸化实验探究发现,S280/S283位点突变完全消除了MBP-CPK12对PIP2;1C的磷酸化。PIP2;1 S280/S283磷酸化位点的特异性抗体分析也显示野生型植株中该位点的磷酸化水平在无毒菌株感染后显著升高。此外,CPK12基因功能的缺失完全阻断了无毒菌株诱导的PIP2;1 S280/S283磷酸化,胞内ROS水平则显示,PIP2;1的磷酸化可能先于ROS转运发生,并潜在促进该过程。综上所述,CPK12在ETI过程中通过磷酸化PIP2;1的S280/S283位点激活其功能。
六、PIP2;1在S280/S283位点的磷酸化促进了其在ROS区室化中的作用
研究评估了表达PIP2;1磷酸化缺陷和磷酸化模拟突变体的转基因植株中ROS的区室化分布。染色分析显示,接种无毒菌株后,pip2;1-1突变体和磷酸化缺陷植株的胞内ROS水平显著低于野生型及磷酸化模拟植株,同时质外体ROS水平则呈现相反的趋势。与胞内ROS积累模式一致,pip2;1-1突变体和磷酸化缺陷植株植株中的细菌生长量也高于野生型及磷酸化模拟植株。这些结果共同表明,S280和S283位点的磷酸化通过调控PIP2;1在ETI-ROS区室化中的功能,进而影响植物对无毒菌的抗性。
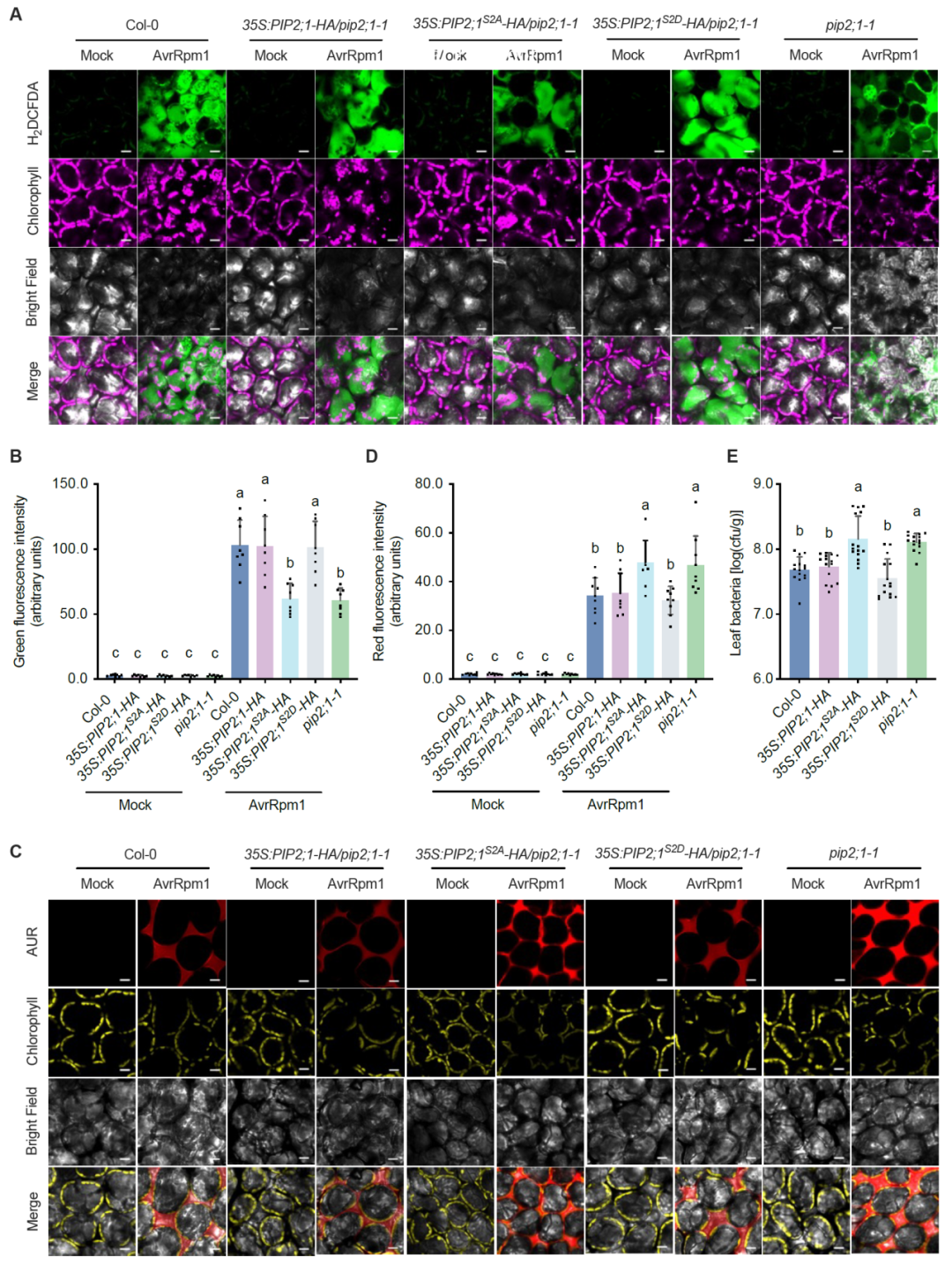
图6. PIP2;1在S280/S283位点的磷酸化促进了其在ROS区室化中的作用
研究结论
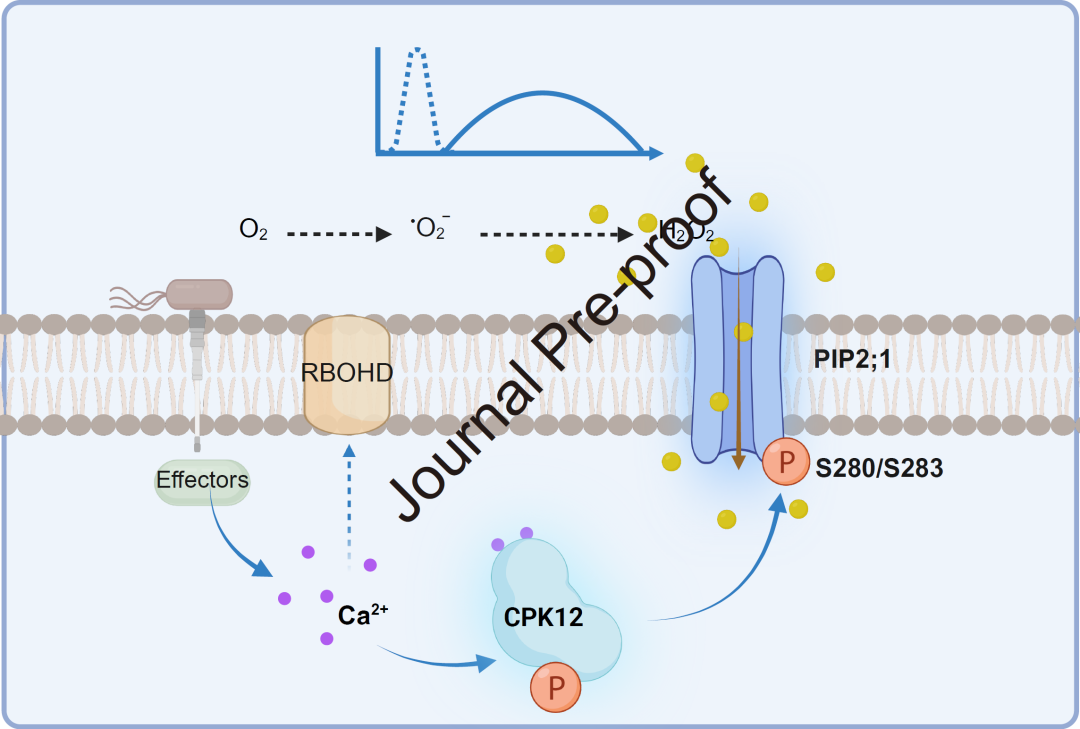
本研究发现,钙依赖蛋白激酶CPK12通过解码病原效应子触发的Ca2+信号,调控植物免疫过程中活性氧(ROS)的区室化分布。CPK12在无毒菌侵染后以Ca2+依赖方式被激活,并磷酸化质膜水通道蛋白PIP2;1的S280/S283位点。该磷酸化修饰介导质外体ROS向细胞质内转运,从而将效应子触发的Ca2+信号与ROS响应的空间调控偶联起来。
因此,本研究为CPK12特异性调控拟南芥ETI-ROS信号通路提供了有力证据。研究的发现凸显了植物免疫信号的复杂性以及不同CPK家族成员在介导免疫应答中的特异性功能。未来的研究应着重于解析调控CPK12活性及功能修饰的转录后机制,并进一步阐明连接Ca2+信号与ROS信号的下游级联通路,从而深化对植物免疫与生长平衡关系的理解。
参考文献
Jia Z, Yu W, Guo X, Li J, Qi F, Zhu Y, Cai X, Li X, Li N, Dong H, Lin F, Liang Y. CPK12 decodes effector-triggered calcium signaling and phosphorylates PIP2;1 to facilitate apoplastic ROS transport into the cytoplasm in Arabidopsis. Mol Plant. 2025 Sep 3:S1674-2052(25)00304-1.
青莲百奥合作文章
青莲百奥深度参与众多前沿研究,与中国医学科学院、中国科学院、军事医学研究院、国家蛋白质科学中心、四川大学华西医院等顶尖科研机构通力合作,累计发表SCI论文近200篇,累计影响因子(IF)超1500。多项重磅研究成果发表于《Nature》《Science Translational Medicine》《Nature Communications》等国际顶级期刊。
