暴露于高原缺氧环境(>2500 m)极易引发腹痛、腹泻及胃肠道出血等胃肠黏膜损伤,严重威胁人群健康。其发病与缺氧诱发的氧化应激相关,临床仅对症处理,缺乏有效的防治策略。以往研究发现,HIF-1α/HIF-2α介导的铁死亡是缺氧介导胃肠黏膜损伤的核心病理机制,靶向抑制HIF-α能够有效改善缺氧诱导的胃肠黏膜屏障损伤。马来沉香具有抗氧化,其植物源外泌体纳米颗粒可通过调节肠道菌群、修复黏膜发挥治疗作用,但其在缺氧胃肠损伤中的作用及靶点尚不明确。
近日,中国人民解放军总医院第七医学中心盛剑秋教授团队联合北京大学医学院常智杰教授团队在MedComm (IF=10.7)上发表题为“Ipriflavone From Aquilaria malaccensis Lam. Exosome-Like Nanoparticles Targets Prolyl Hydroxylase Domain Protein 2 (PHD2) to Enhance Hypoxia-Inducible Factor-α (HIF-α) Hydroxylation Thereby Alleviating Hypoxia-Induced Gastrointestinal Mucosal Ferroptosis”的研究论文。该研究依托限制性酶解-质谱分析(LiP-MS) 的无偏靶点筛选能力,直接锁定依普黄酮的作用靶点PHD2。进而,结合多组学与功能实验,揭示了马来沉香类外泌体纳米颗粒(AELNs)的活性成分依普黄酮,通过增强HIF-α羟化降解、抑制脂质过氧化,有效缓解高原胃肠铁死亡的新机制。
北京青莲百奥在本研究中提供了LiP-MS技术服务。
研究方法
样本类型 | 详细信息 |
动物模型 | C57BL/6小鼠,模拟海拔5000米低氧舱3天 |
| 细胞模型 | 正常人胃上皮细胞(NGEC)、小肠上皮细胞(HIEC) |
| 干预物质 | 沉香外泌体样纳米颗粒(AELNs)、依普黄酮 |
| 关键技术 | TEM、LC-MS、16S rRNA测序、脂质组学、Lip-MS、分子对接、分子动力学模拟、SPR |
研究亮点
1.首次发现:首次报道AELNs可有效缓解缺氧诱导的胃肠铁死亡;
2.活性成分:鉴定伊普黄酮为AELNs核心效应物,保护效果优于AELNs;
3.技术创新:借助LiP-MS无偏靶点筛选,首次直接锁定伊普黄酮作用靶标PHD2;
4.关键机制:阐明HIF-α→PUFA-PLs/NOX4/ALOX5 介导缺氧胃肠铁死亡;
5.转化潜力:伊普黄酮为已上市抗骨质疏松药物,老药新用,安全性明确。
研究结果
1、AELNs缓解缺氧小鼠胃肠黏膜损伤,并抑制铁死亡发挥保护作用
研究方法:小鼠灌胃不同剂量AELNs,低氧舱(模拟5000米高原缺氧)3天;检测组织病理、通透性、铁死亡指标。
研究结果:高剂量(1×10⁵颗粒)AELNs显著改善缺氧诱导的体重下降、腹泻、便潜血,明显修复胃肠黏膜充血糜烂、绒毛紊乱、隐窝变浅等病理损伤,减轻黏膜屏障破坏(图1)。透射电镜显示,AELNs逆转了线粒体萎缩、嵴破坏等铁死亡特征。分子水平上,AELNs降低 ROS、LPO、4-HNE 水平,对 Fe²⁺无明显影响;特异性下调HIF-1α,不影响HIF-2α及 SLC7A11/GPX4轴(图2),证实其通过抑制HIF-1α、减轻铁死亡实现黏膜保护。
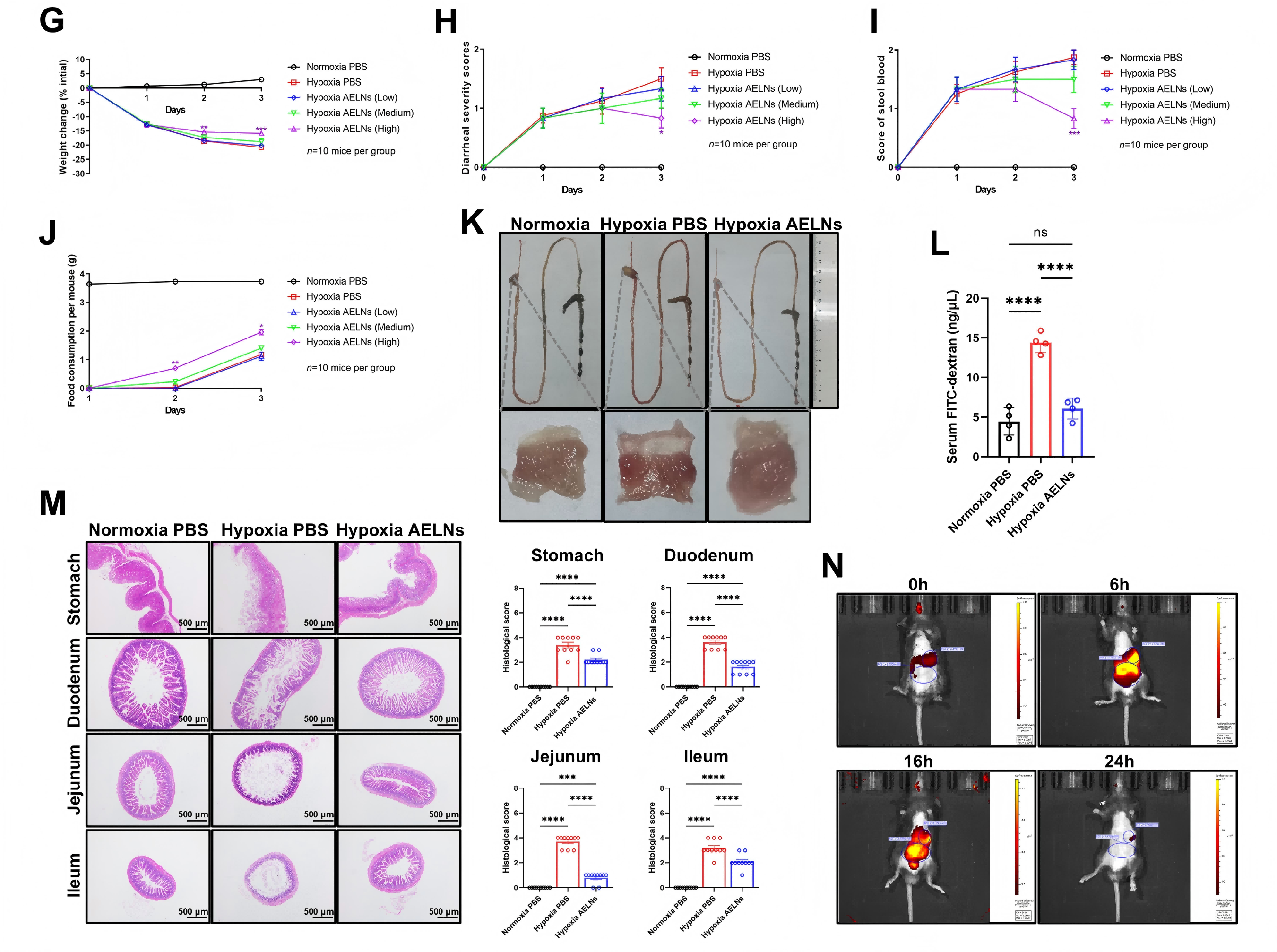
图1 AELNs缓解缺氧暴露小鼠胃和小肠黏膜损伤
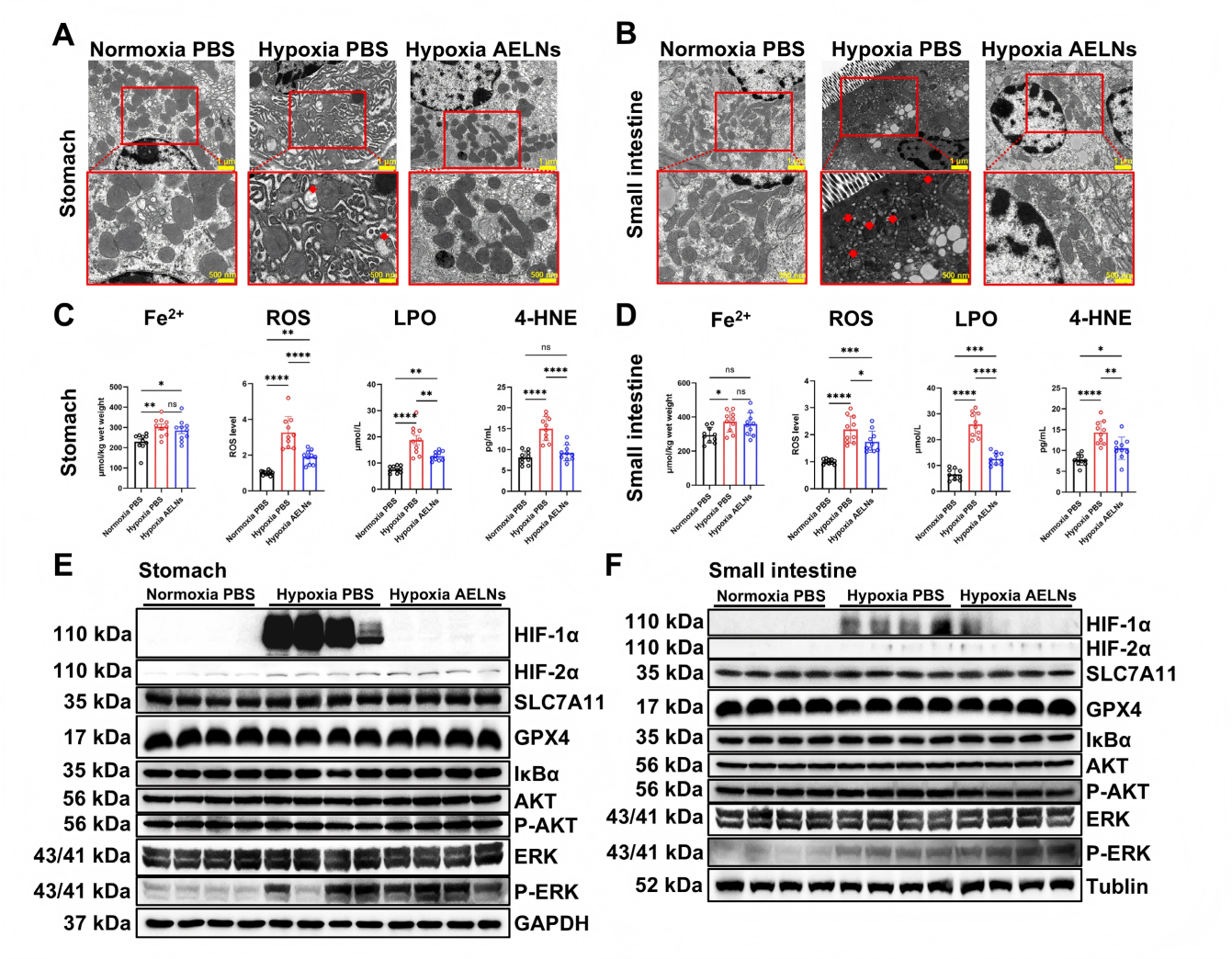
图2 AELINS可改善小鼠因缺氧引起的胃和小肠黏膜铁死亡
2、AELNs可部分恢复缺氧所致胃肠菌群与代谢紊乱
研究方法:16S rRNA测序+非靶向代谢组学分析胃/小肠内容物。
研究结果: 缺氧显著降低胃肠菌群α多样性,造成菌群失衡与代谢紊乱。AELNs干预部分恢复缺氧导致的α多样性下降,显著恢复Ilumatobacter、Lachnospiraceae(胃)及Kroppenstedtia、Enterococcus(小肠)等菌属(图3);同时逆转了3,4-二羟基扁桃醛、8-羟基喹啉等抗氧化代谢物以及棕榈酰-L-肉碱等有害代谢物(图4)。菌群–代谢物关联分析证实,AELNs通过调节微生态平衡减轻氧化应激,协同改善缺氧胃肠黏膜病变。
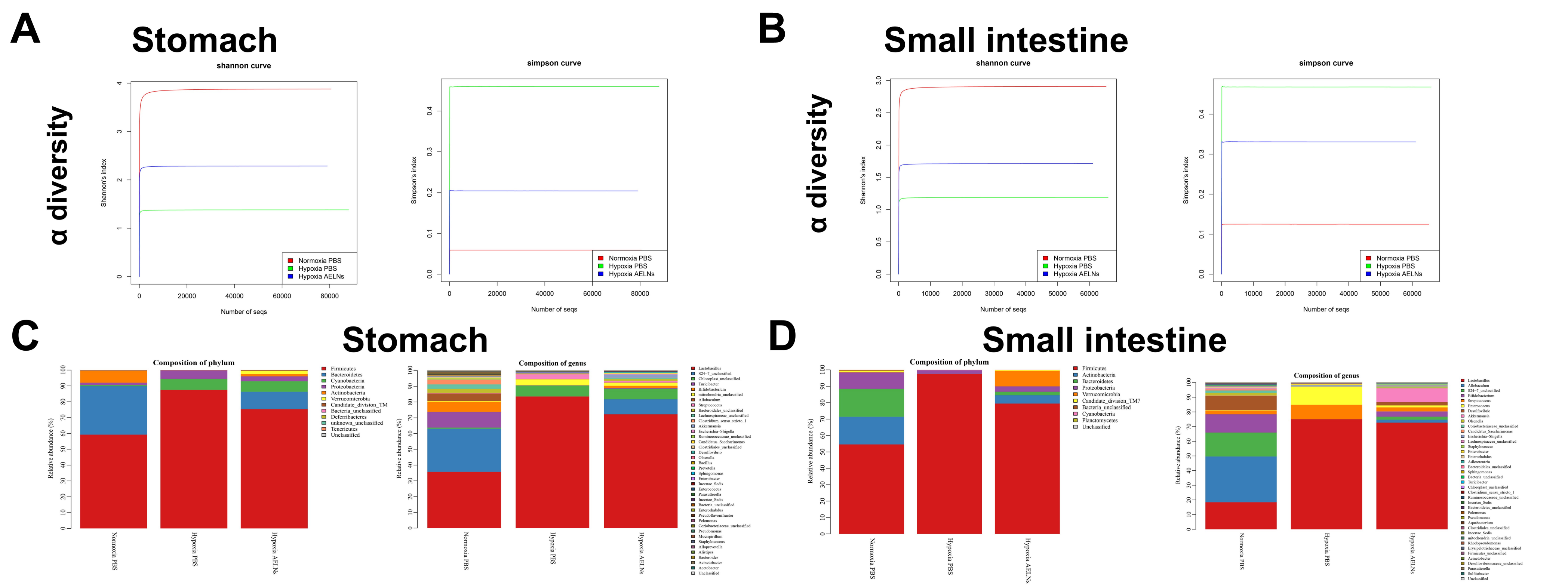
图3 AELINs可部分恢复小鼠因缺氧引起的胃和小肠黏膜肠道微生物群落改变
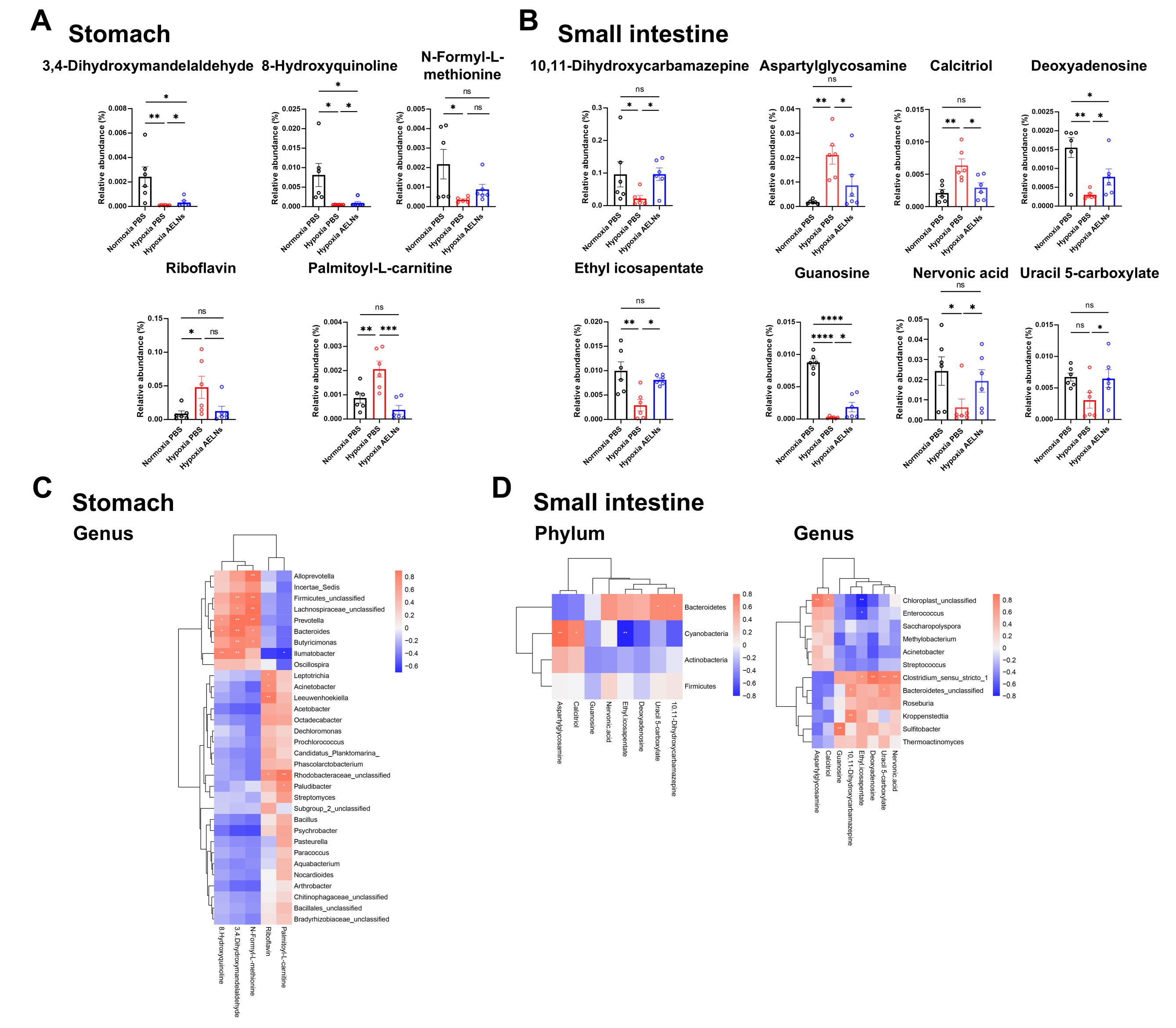
图4 AELINs可部分改善小鼠因缺氧引起的胃和小肠黏膜代谢功能障碍
3、伊普黄酮为AELNs核心活性成分,通过抑制HIF-α介导的脂质过氧化缓解铁死亡
研究方法:代谢组学鉴定AELNs成分;CCK-8、Western blot;脂质组学;NOX4/ALOX5抑制剂及过表达实验
研究结果:非靶向代谢组筛选显示,伊普黄酮占AELNs总代谢物40.39%,为第一主成分。细胞实验证实AELNs可被胃肠上皮细胞有效摄取,伊普黄酮呈浓度依赖性提升缺氧下NGEC、HIEC活力,效果显著优于AELNs。机制上,伊普黄酮可同时下调HIF-1α和 HIF-2α,降低ROS、4-HNE,修复线粒体损伤,且不影响GR表达。脂质组显示伊普黄酮显著下调 PUFA-PC、PUFA-PE;蛋白检测证实其抑制 HIF-α下游NOX4、ALOX5,减少脂质过氧化物。回复实验进一步确认,伊普黄酮通过HIF-α→PUFA-PLs/NOX4/ALOX5 轴抑制脂质过氧化,缓解缺氧诱导的铁死亡。
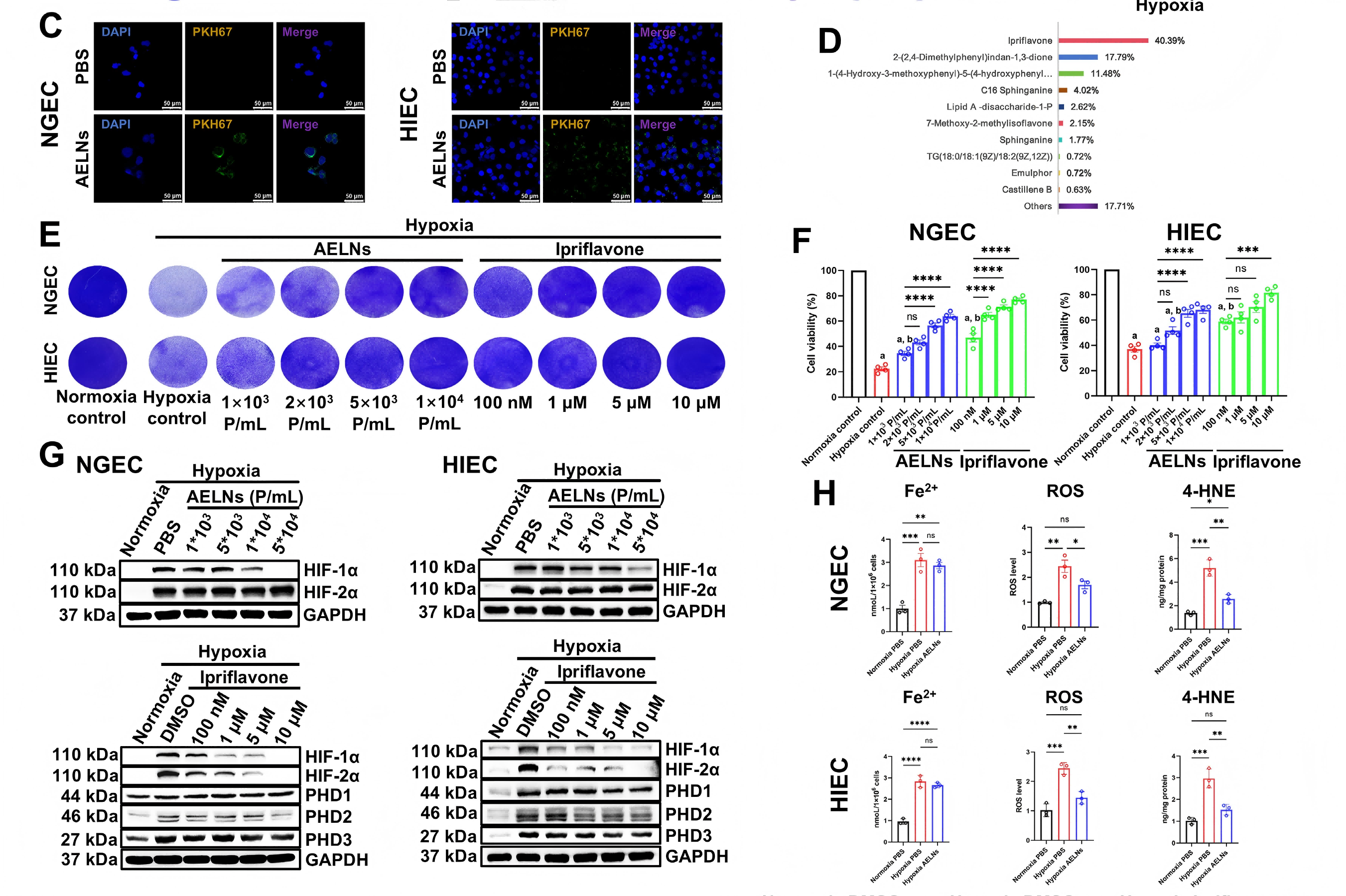
图5 伊普黄酮通过抑制HIF-1a和HIF-2a减轻NGEC和HIEC中缺氧诱导的铁死亡
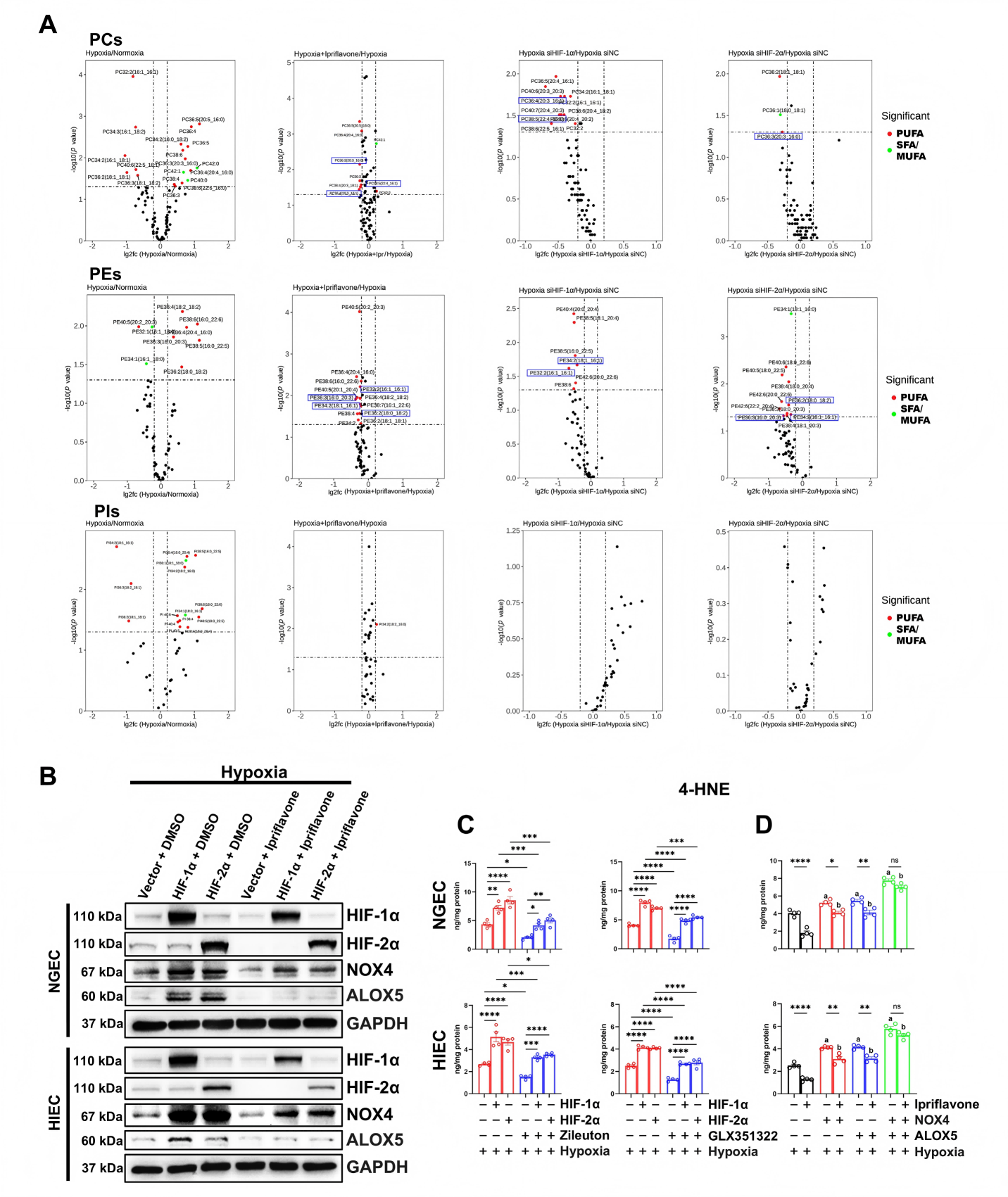
图6 伊普黄酮通过抑制HIF-α介导的脂质过氧化缓解铁死亡
4、LiP-MS鉴定伊普黄酮直接靶向PHD2,增强HIF-α羟化促进降解
研究方法:LiP-MS筛选靶点、分子对接、分子动力学模拟、SPR、PHD2 siRNA敲低、免疫沉淀
研究结果:研究采用LiP-MS无偏筛选,直接锁定PHD2为伊普黄酮的关键作用靶点。分子对接、SPR及分子动力学模拟显示,伊普黄酮与PHD2的MET299、TYR303、ILE327关键残基稳定结合,其中ILE327为最核心位点;结合后改变PHD2构象,增强其羟化活性。免疫共沉淀与蛋白检测表明,伊普黄酮不改变PHD2表达,而是通过增强PHD2介导的HIF-α羟化,促进HIF-α与VHL结合并经泛素-蛋白酶体降解;敲低PHD2后,伊普黄酮对HIF-α的调控及细胞保护作用完全消失。
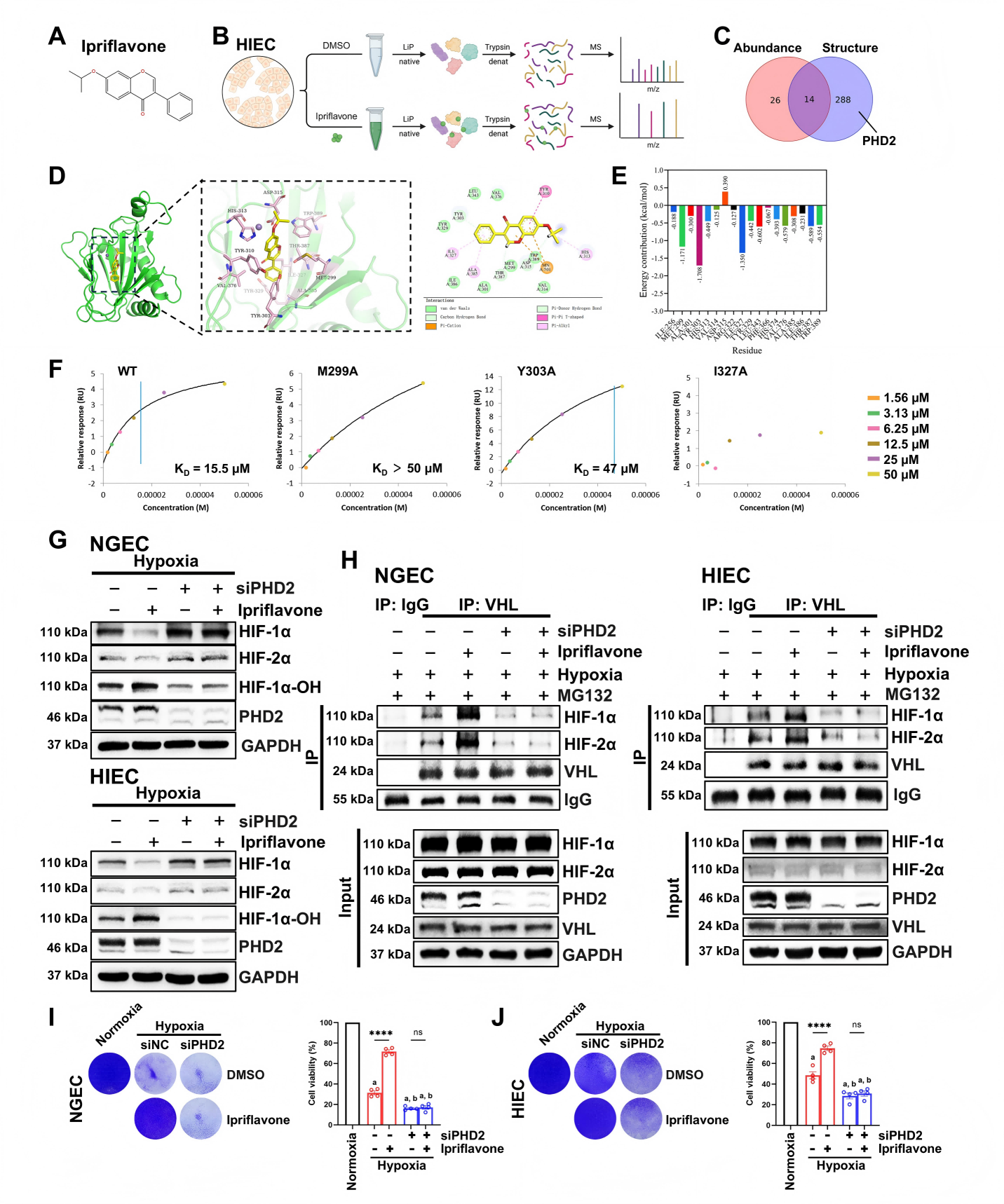
图7 伊普黄酮靶向PHD2增强HIF-α羟化,促进其降解
5、口服伊普黄酮显著减轻缺氧小鼠胃肠损伤
研究方法:小鼠口服伊普黄酮(5-15 mg/kg),检测临床指标及分子标志物
研究结果:体内动物实验验证,口服5~15 mg/kg伊普黄酮可剂量依赖性改善缺氧小鼠摄食减少、体重下降、腹泻、粪便潜血等症状,10~15 mg/kg 效果最优。病理结果显示,伊普黄酮明显修复胃肠黏膜损伤,降低通透性。分子检测证实,伊普黄酮显著下调胃肠黏膜HIF-1α、HIF-2α、NOX4、ALOX5,降低ROS、4-HNE,与体外机制完全一致,证实伊普黄酮体内安全有效。
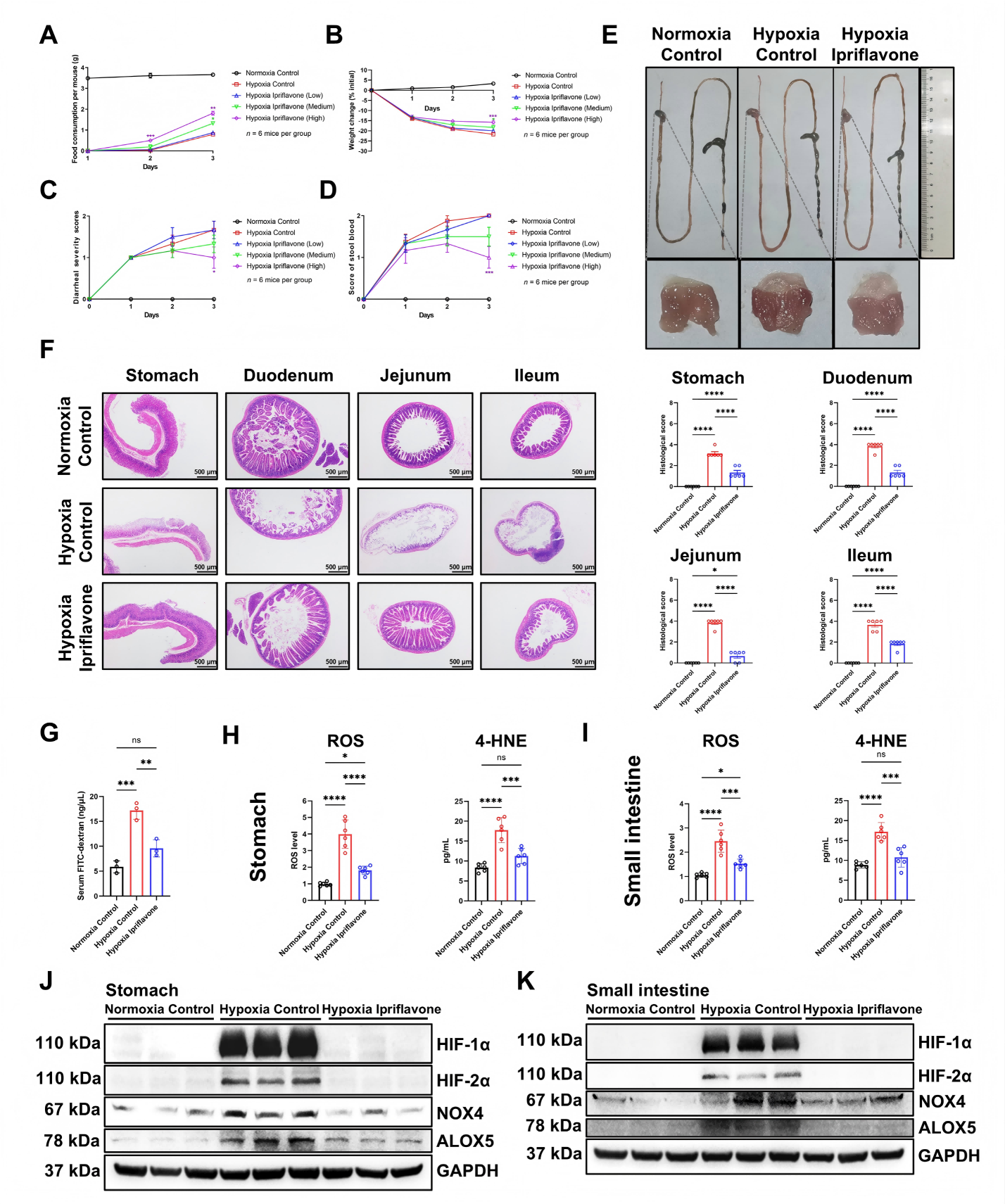
图8 口服伊普黄酮可显著减轻缺氧小鼠胃肠黏膜损伤
研究结论
本研究首次揭示沉香外泌体样纳米粒(AELNs) 对高原缺氧诱导胃肠黏膜损伤的保护作用,并精准锁定伊普黄酮为核心活性成分。通过限制性酶解-质谱分析(LiP-MS)发现伊普黄酮通过靶向 PHD2→增强 HIF-α 羟化降解→抑制 PUFA-PLs/NOX4/ALOX5 介导的脂质过氧化铁死亡的全新分子机制,为高原胃肠损伤提供了新的防治靶点与策略。
伊普黄酮作为已上市药物,安全性明确,为高原胃肠病、HIF-α 相关炎症及肿瘤等疾病提供了快速可转化的治疗方案。
参考文献与全文链接
[1] Wang D, Liao X, Wang Y, et al. Ipriflavone From Aquilaria malaccensis Lam. Exosome-Like Nanoparticles Targets Prolyl Hydroxylase Domain Protein 2 (PHD2) to Enhance Hypoxia-Inducible Factor-α (HIF-α) Hydroxylation Thereby Alleviating Hypoxia-Induced Gastrointestinal Mucosal Ferroptosis. MedComm (2020). 2026 Apr 9;7(4): e70722. doi: 10.1002/mco2.70722.
青莲百奥解决方案
作为国内推广限制性酶解-质谱分析(LiP-MS)技术的先驱,青莲百奥致力于提供全面的“一站式”LiP-MS服务。利用尖端的全流程高精密仪器和先进的生物信息分析流程,青莲百奥确保了LiP-MS分析的高精度、高重复性和高准确性(>>>点击查看LiP-MS解决方案全面升级详解)【青莲百奥LiP-MS解决方案全新升级】。该技术的应用显著提高了药物靶点筛选的效率,并为生物标志物的发现提供了坚实的基础。通过这一技术,研究人员能够更快速地识别和验证潜在的药物作用机制和疾病相关标志物,从而推动精准医疗和个性化治疗策略的发展。
