肿瘤侵袭转移是恶性肿瘤致死的主要原因,而细胞骨架动态重构是肿瘤细胞获得迁移侵袭能力的关键。肌动蛋白(Actin)作为细胞骨架核心成分,其单体G-actin与聚合态F-actin的动态平衡直接决定细胞运动能力。液液相分离(LLPS)是调控蛋白功能的重要机制,但其与肌动蛋白动态转换、肿瘤侵袭的关系尚不明确,且目前缺乏精准靶向G/F-actin平衡的手段,成为肿瘤靶向治疗的重要瓶颈。
近日,天津大学联合天津医科大学生物医学工程与技术学院贺慧宁院长研究团队在化学领域的顶级期刊《Journal of the American Chemical Society》(JACS,IF=15.7)上发表题为“Hijacking Actin-Pre-Liquid-Liquid Phase Separation Suppresses Malignant Tumor Invasion and Growth”的研究论文。该研究首次揭示了肌动蛋白(Actin)在细胞内的预液液相分离(Pre-LLPS)机制,并基于此开发了一种新型四臂交联分子4Arm-Pen,通过靶向G-actin液滴实现对肿瘤细胞迁移和侵袭的有效抑制。
北京青莲百奥在本研究中提供了蛋白质组学技术支持,助力解析4Arm-Pen在细胞内的交联蛋白靶点谱。

样本信息
细胞样本:小鼠结肠癌细胞CT-26、小鼠胚胎成纤维细胞NIH-3T3,构建eGFP-actin标记稳转细胞株;
组织样本:BALB/c小鼠皮下肿瘤组织、血管旁肿瘤组织;
体外样本:纯化兔肌动蛋白、体外重构相分离体系样本。
实验技术
类别 | 技术方法 |
| 力学与成像检测 | 纳米压痕技术、激光共聚焦延时成像、FRAP荧光漂白恢复实验 |
| 体外相分离重构 | PEG/DEX双水相体系诱导LLPS |
| 交联蛋白检测 | 生物素标记4Arm-Pen交联蛋白质组学、靶向蛋白质定量组学 |
| 分子与细胞功能检测 | Western Blot、G/F-action分离、基因突变构建;划痕愈合、侵袭共培养、全息细胞成像 |
| 数理模拟分析 | CytoSIM细胞骨架模拟、肌动蛋白聚合动力学建模 |
研究亮点速递
1.机制首创:首次发现并定义Actin-Pre-LLPS,明确其作为G-actin储存池调控肿瘤细胞运动的全新机制。
2.靶向精准:研发4Arm-Pen分子,特异性靶向肌动蛋白Cys374位点,正交二硫键交联不干扰正常细胞功能。
3.效果显著:通过逆转Actin-Pre-LLPS,阻断G-actin活化与F-actin聚合,强效抑制肿瘤细胞侵袭、迁移与增殖。
4.技术支撑:通过蛋白质组学技术精准锁定靶向蛋白,验证分子作用特异性,为成果提供硬核数据支撑。
研究结果
1、“储存型”肌动蛋白在细胞片状伪足附近产生液-液相分离
研究方法:构建小鼠皮下肿瘤模型,通过H&E染色、纳米压痕技术检测血管旁(PV)与肿瘤实体(IT)组织细胞密度与有效杨氏模量;构建eGFP-actin标记细胞株,激光共聚焦观测肌动蛋白聚集状态,关联细胞运动能力。
研究结果:高侵袭性血管旁肿瘤组织细胞密度显著高于肿瘤内部,且组织刚度更低(杨氏模量<50kPa);高迁移肿瘤细胞伪足区域出现高浓度肌动蛋白聚集区,形成动态液滴结构,首次证实Actin-Pre-LLPS现象,切该现象与肿瘤细胞迁移表型密切相关。
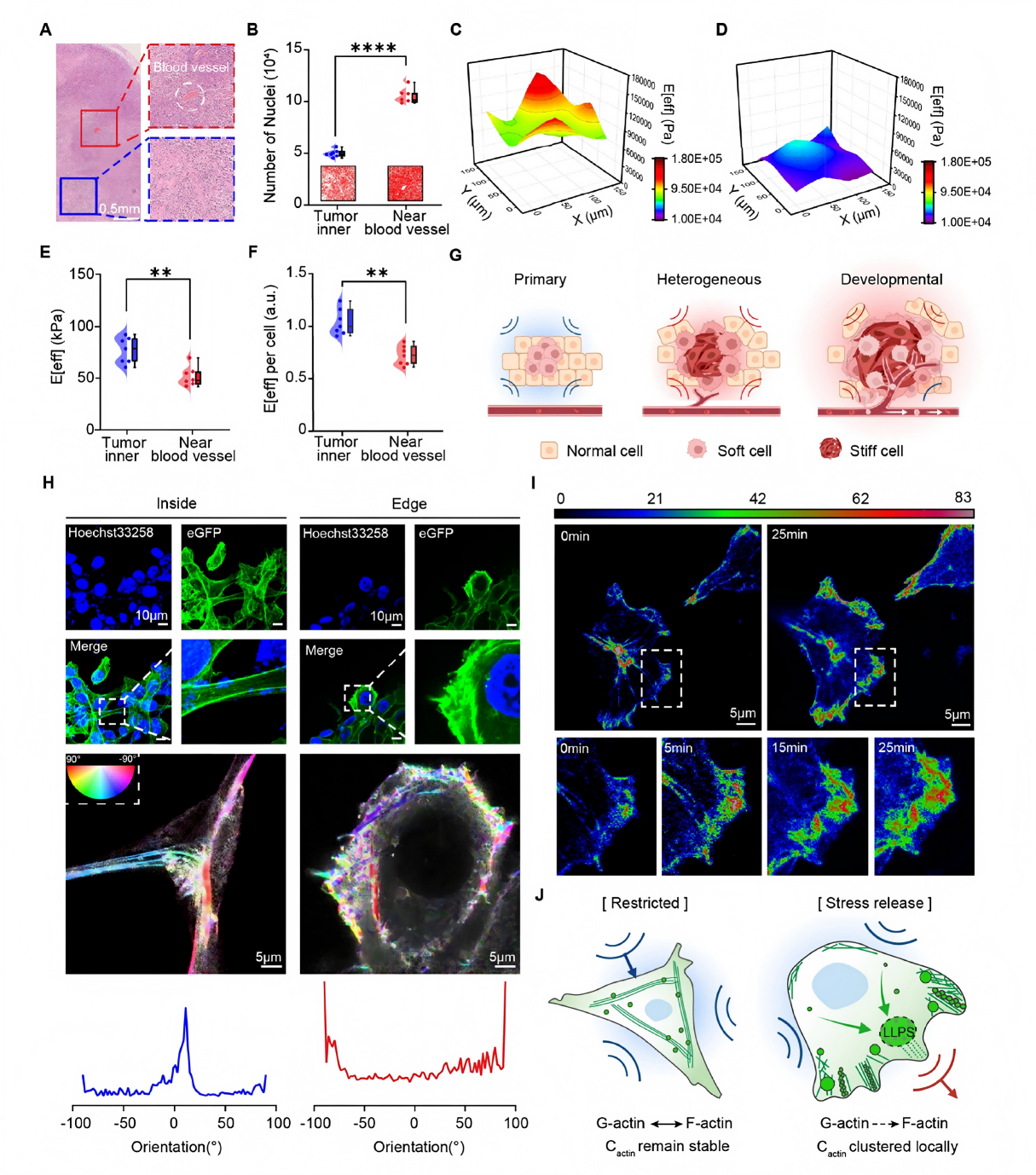 图1 肿瘤细胞簇通过肌动蛋白Pre-LLPS改变细胞刚性实现表型转换
图1 肿瘤细胞簇通过肌动蛋白Pre-LLPS改变细胞刚性实现表型转换
2、Actin-Pre-LLPS是调控细胞运动的“调度”策略
研究方法:纯化G-actin并体外诱导相分离,结合延时成像、FRAP实验验证液滴流动性;双相富集分离不同状态肌动蛋白,透射电镜观察蛋白形态。
研究结果:体外成功重构Actin-Pre-LLPS体系,在活细胞及体外体系中均观察到动态、可融合的肌动蛋白液滴,该过程具有浓度依赖性和可逆性(1,6-己二醇可消除液滴),且液滴内分子具备快速迁移能力(图2)。首次证实存在储存型G-actin与活化型G-actin两种状态,储存型G-actin存在于相分离液滴中,不自发聚合,但在ATP浓度升高时可被激活并组装成F-肌动蛋白。证实Actin-Pre-LLPS液滴为肌动蛋白储存池,可按需为细胞运动提供骨架原料(图3)。
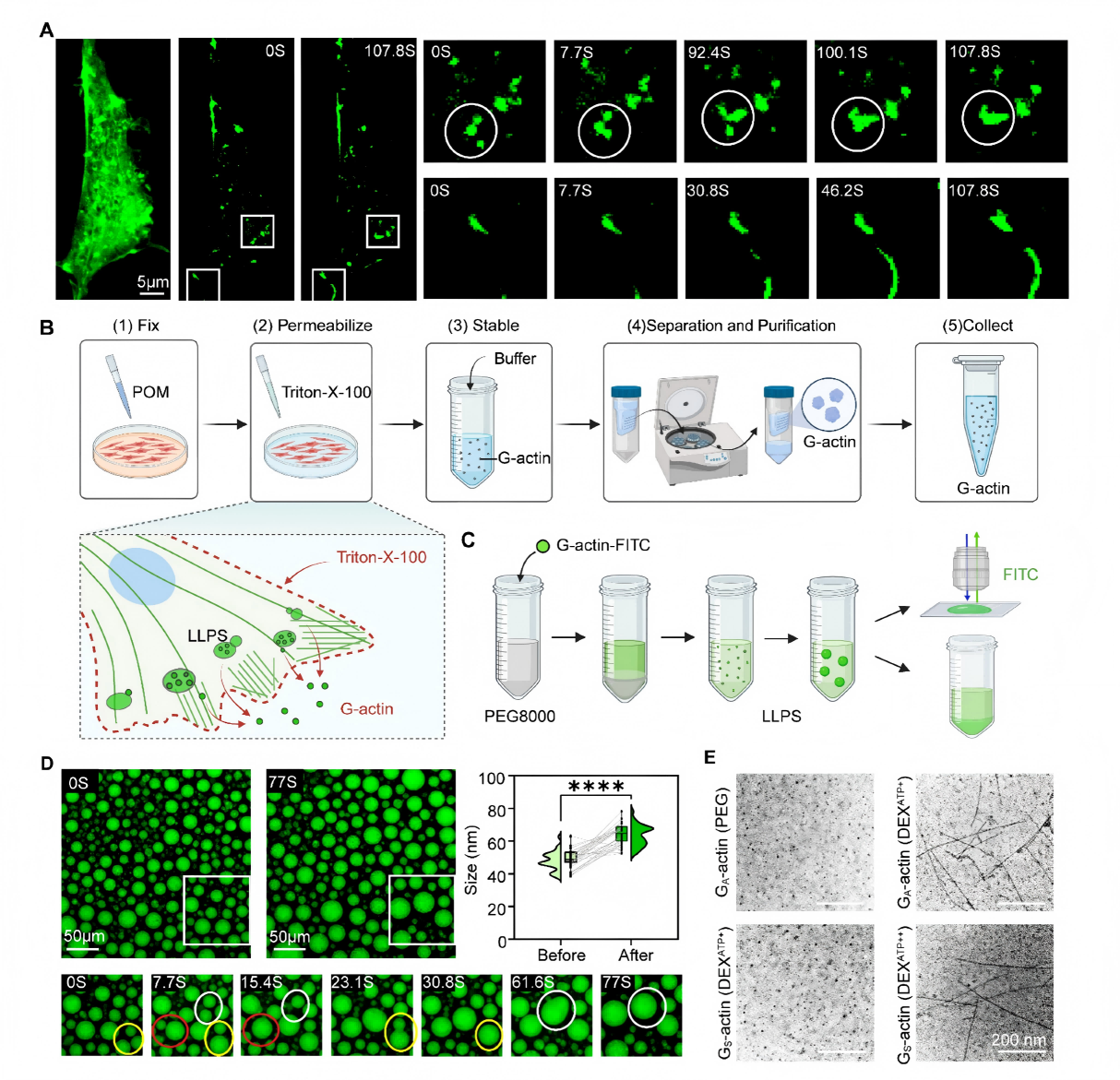 图2 储存型G-肌动蛋白诱导Pre-LLPS并形成非聚合活性液滴
图2 储存型G-肌动蛋白诱导Pre-LLPS并形成非聚合活性液滴
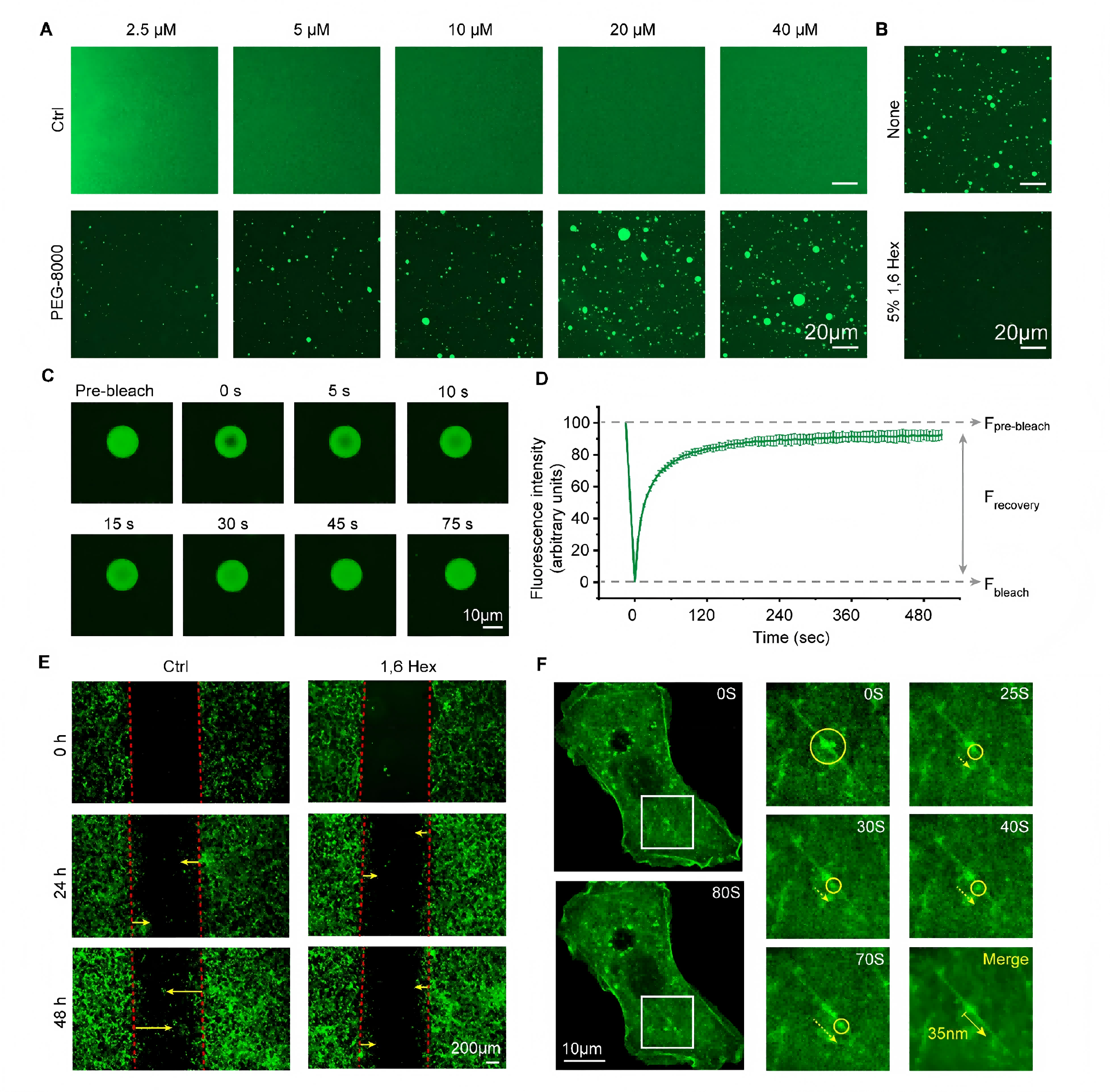
图3 Actin-Pre-LLPS遵循LLPS规则,调控细胞运动和F-肌动蛋白的形成
3、蛋白质组学揭示Pre-LLPS形成的肌动蛋白液滴可作为4Arm-Pen的靶点
研究方法:基于半胱氨酸正交二硫键化学原理,设计合成靶向分子4Arm-Pen,构建C374A突变体验证作用靶点;构建肌动蛋白C374A突变细胞株,结合荧光共定位成像、生物素标记4Arm-Pen交联蛋白质组学技术(青莲百奥提供蛋白质组学分析),验证分子靶向特异性与精准作用位点。
研究结果:成功合成高纯度靶向分子4Arm-Pen,分子结构与理化性质符合后续实验要求(图4)。该分子可特异性结合肌动蛋白Cys374位点,C374A突变可完全阻断二者结合作用,荧光共定位显示其可精准富集于伪足相分离液滴区域(图5);交联蛋白质组学数据证实,4Arm-Pen仅优先靶向结合肌动蛋白,无明显非特异性结合,靶点专一性极强。
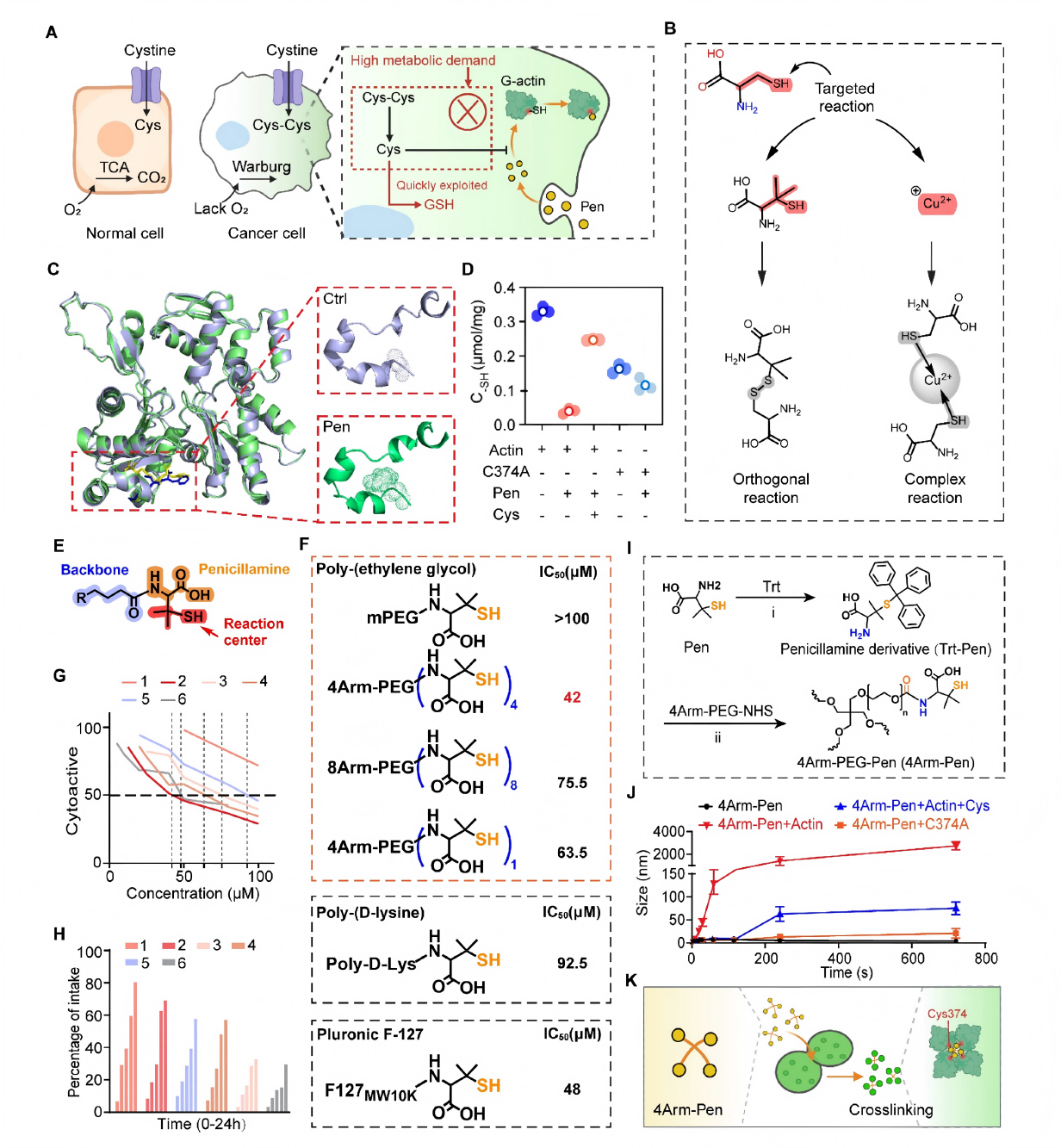 图4 4Arm-PEG-Pen可以针对肌动蛋白液滴形成交联效应
图4 4Arm-PEG-Pen可以针对肌动蛋白液滴形成交联效应
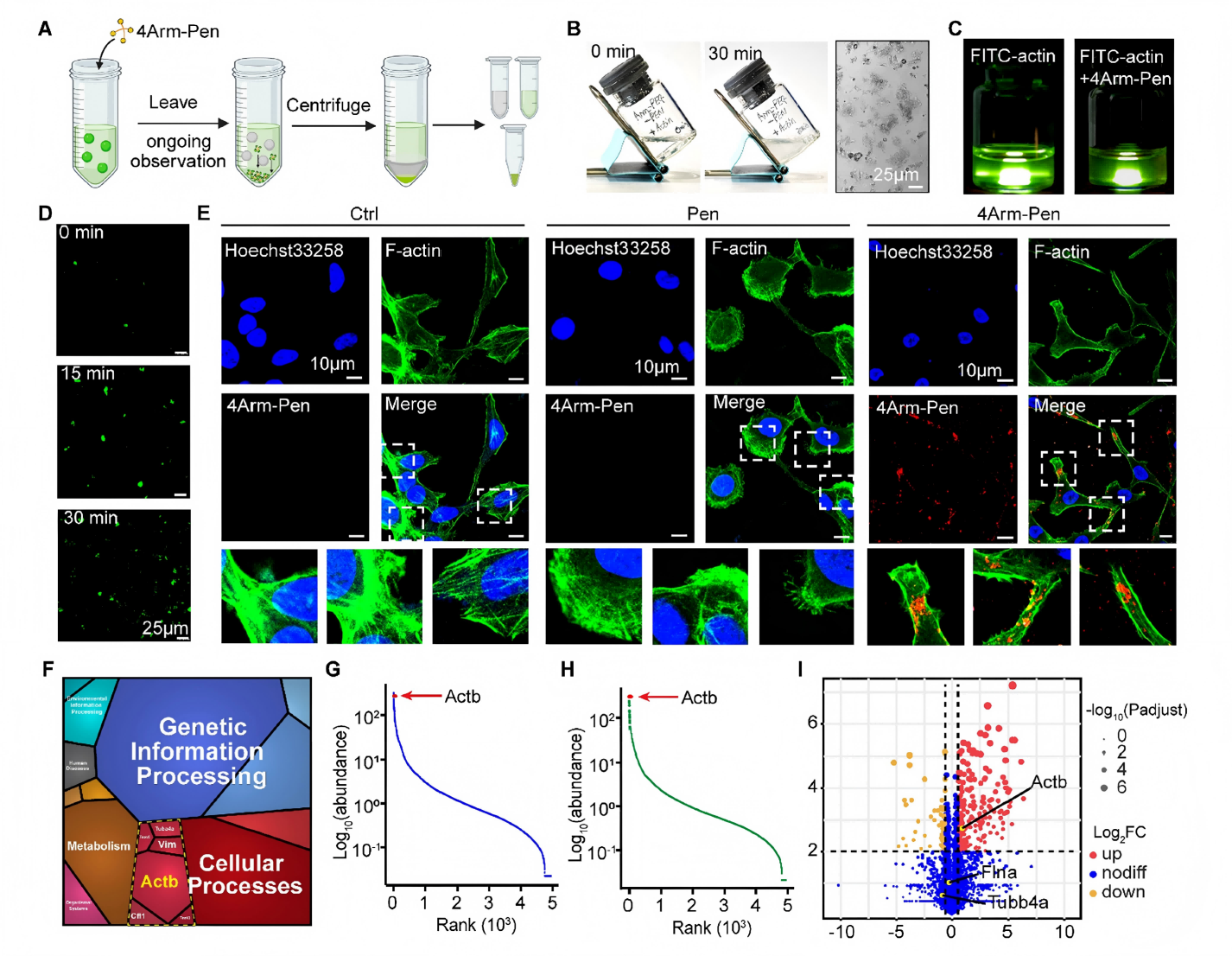
图5 4Arm-Pen能清除肌动蛋白液滴,并偏好细胞内肌动蛋白交联
4、4Arm-Pen显著改变细胞骨架聚合动力学
研究方法:透射电镜观察4Arm-Pen处理后G-actin聚合形态;G/F-actin分离试剂盒检测单体与聚合态肌动蛋白比例;构建Actin-Pre-LLPS、正常聚合、4Arm-Pen干预三种模型,通过数学建模与CytoSIM模拟分析聚合动力学。
研究结果:4Arm-Pen处理后,G-actin形成四聚体或无序聚集体,无法正常聚合成F-actin丝;胞内储存型G-actin大量消耗,G/F-actin比值显著降低,正常微丝结构重构受阻;数学建模与模拟证实,4Arm-Pen改变肌动蛋白聚合动力学常数,阻断活化型G-actin生成,将肌动蛋白锁定为非功能性四聚体,而非传统微丝稳定剂。以上结果表明,4Arm-Pen通过交联G-actin改变其聚合动力学,阻止F-actin的正常形成。
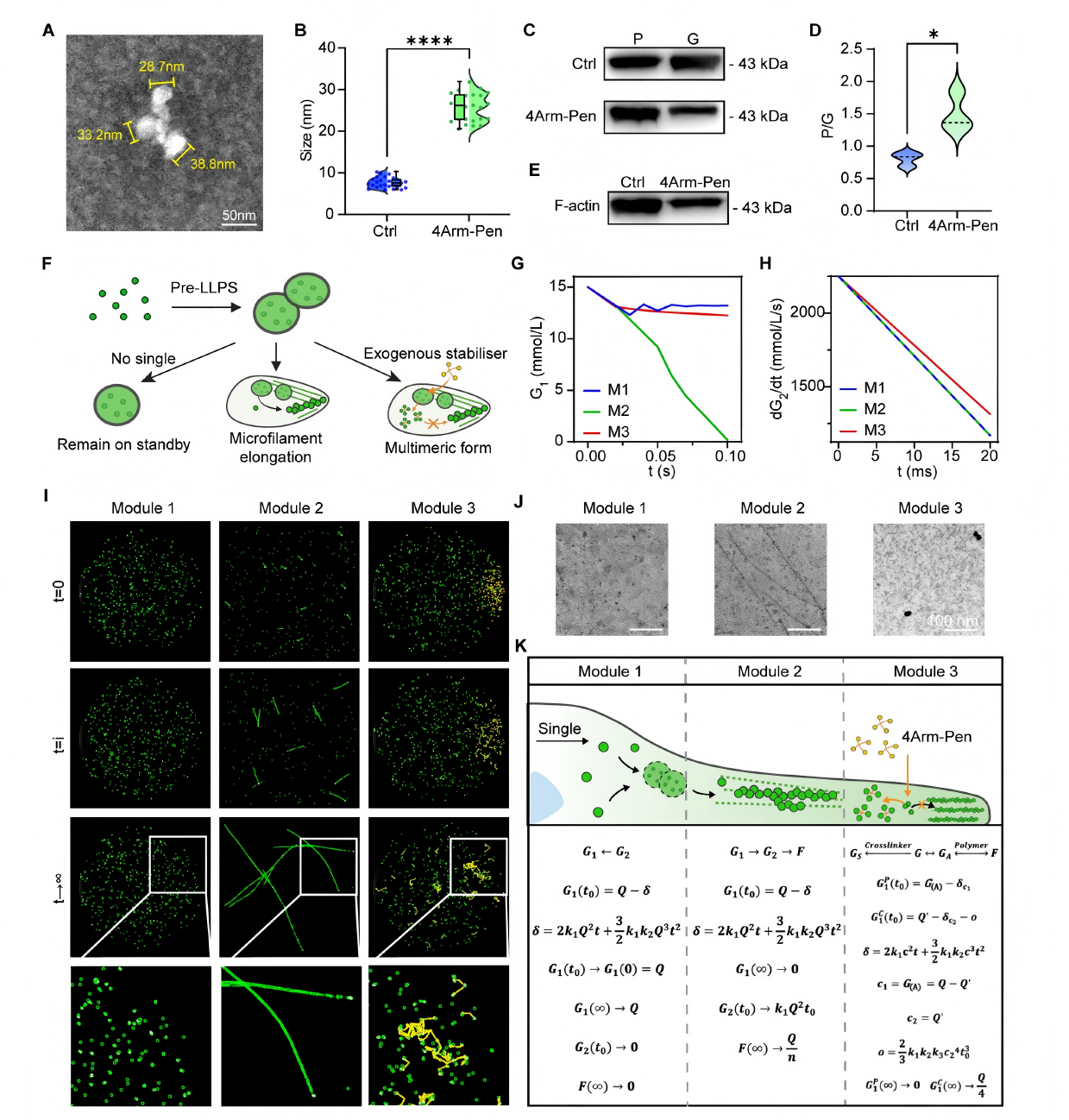
图6 4Arm-Pen通过修饰G-actin影响肌动蛋白聚合动力学
5、4Arm-Pen介导G-actin耗竭,强效抑制肿瘤细胞迁移与侵袭
研究方法:细胞划痕实验、全息细胞成像检测细胞迁移速率与运动轨迹;肿瘤细胞与成纤维细胞共培养侵袭实验,检测肿瘤侵袭能力;建立CT-26与NIH-3T3共培养侵袭模型评估细胞侵袭能力,并构建C374A突变细胞株验证靶点特异性。
研究结果:4Arm-Pen处理后,CT-26肿瘤细胞24h迁移距离及细胞运动速度均显著下降;肿瘤细胞侵袭NIH-3T3成纤维细胞单层的能力和侵袭速率显著下降;游离半胱氨酸可竞争性逆转4Arm-Pen的抑制作用,C374A突变肿瘤细胞完全耐受该分子,进一步证实其作用靶点为肌动蛋白Cys374,且对正常成纤维细胞无明显影响,选择性优异。以上结果表明,4Arm-Pen通过靶向G-actin Cys374位点,特异性抑制肿瘤细胞的迁移与侵袭。
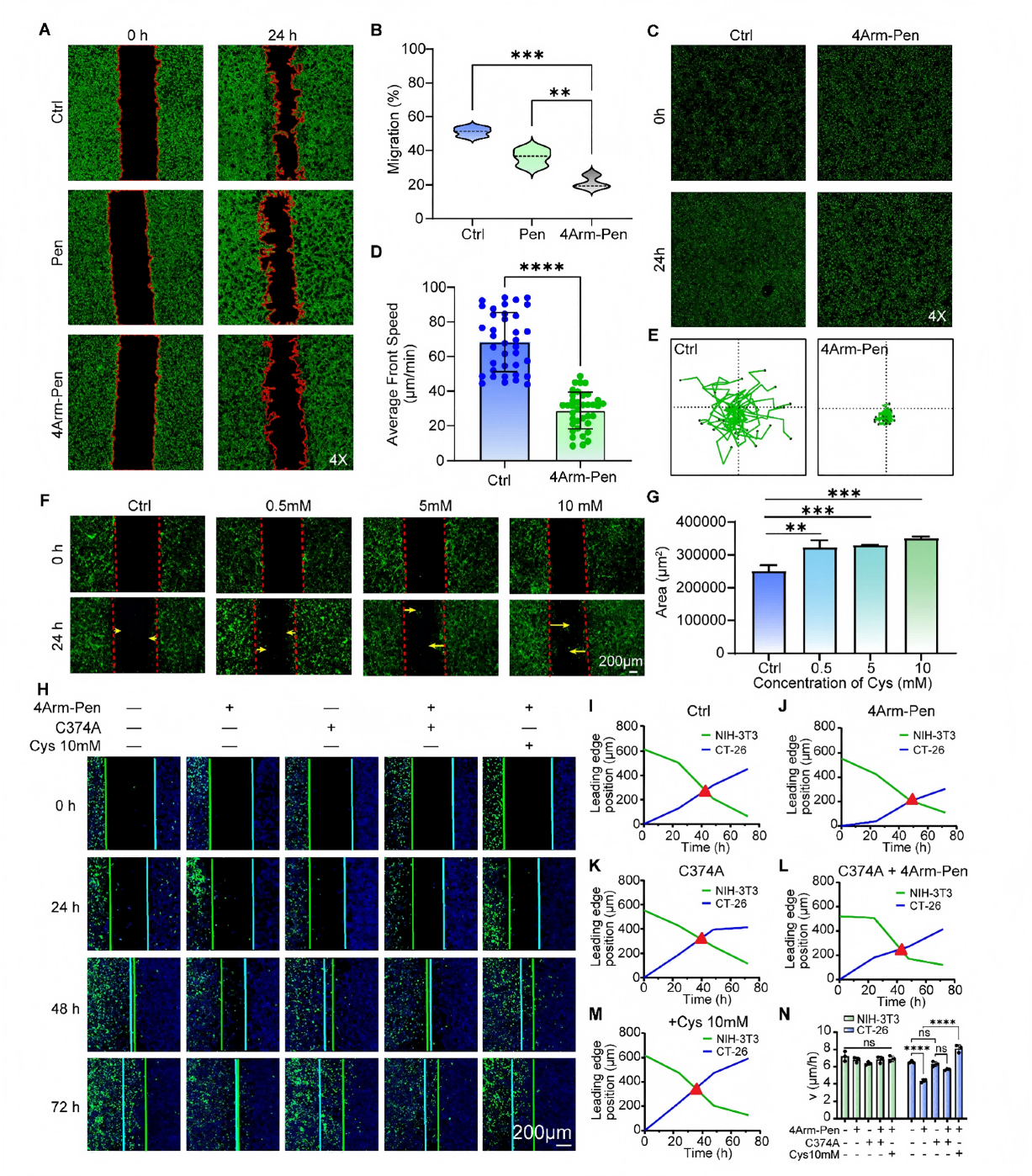
图7 4Arm-Pen通过介导G-actin耗竭抑制肿瘤细胞迁移与侵袭的功能验证
6、4Arm-Pen可抑制恶性肿瘤侵袭与生长
研究方法:建立CT-26皮下荷瘤小鼠模型,进行瘤内注射4Arm-Pen(5 mg/kg),监测肿瘤体积、小鼠体重及生存期,组织纳米压痕技术测定肿瘤硬度,H&E染色评估肿瘤及主要器官的病理变化。
研究结果:4Arm-Pen处理组肿瘤生长显著受抑,生存期延长,各组小鼠体重无显著差异,表明药物耐受性良好;4Arm-Pen处理组肿瘤组织硬度显著增加,力-位移曲线发生改变;H&E染色显示肿瘤组织坏死区域增加,而主要器官(心、肝、脾、肺、肾)未见明显损伤。研究提出4Arm-Pen可能通过改变肿瘤力学微环境间接抑制肿瘤进展,表明4Arm-Pen体内应用安全有效,通过靶向Actin-Pre-LLPS抑制肿瘤生长并改变组织力学特性。
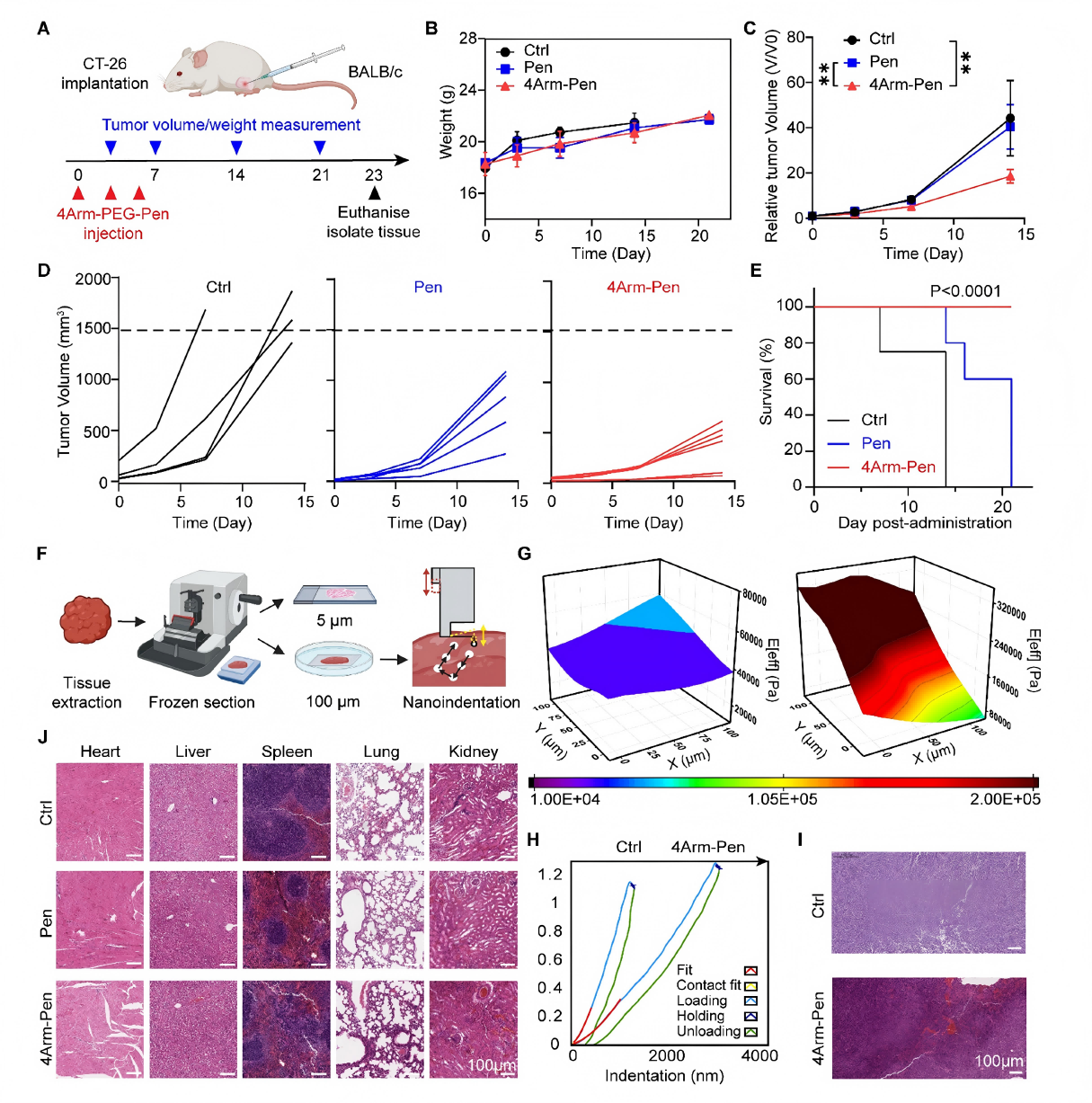
图8 4Arm-Pen可抑制恶性肿瘤侵袭与生长
研究结论
本研究首次突破性揭示了Actin-Pre-LLPS作为肌动蛋白储存池调控肿瘤细胞侵袭、迁移的核心机制,明确了该过程是恶性肿瘤获得高侵袭性的关键环节。团队基于正交二硫键化学成功研发的靶向分子4Arm-Pen,可特异性结合肌动蛋白Cys374位点,逆转Actin-Pre-LLPS过程,耗竭胞内储存型G-actin,阻断F-actin正常聚合,最终强效抑制肿瘤细胞的侵袭、迁移与增殖能力。
参考文献与全文链接
[1] Zhang Z, Yin K, Li B, et al. Hijacking Actin-Pre-Liquid-Liquid Phase Separation Suppresses Malignant Tumor Invasion and Growth. J Am Chem Soc. 2026 Mar 7. doi: 10.1021/jacs.5c19435.
青莲百奥合作文章
青莲百奥深度参与众多前沿研究,与中国医学科学院、中国科学院、军事医学研究院、国家蛋白质科学中心、四川大学华西医院等顶尖科研机构通力合作,累计发表SCI论文近200篇,累计影响因子(IF)超1500。多项重磅研究成果发表于《Nature》《Science Translational Medicine》《Nature Communications》等国际顶级期刊。
