膀胱癌是一种常见的泌尿系统恶性肿瘤,目前的免疫治疗手段如抗PD-1/PD-L1疗法对多数患者效果有限。CD47作为一种重要的免疫检查点蛋白,通过与信号调节蛋白α(SIRP-α)结合释放“别吃我”信号,帮助肿瘤细胞逃避免疫,而其过度糖基化是这一逃逸机制的重要因素。然而,CD47糖基化的调控机制及其在膀胱癌中的作用尚不明确。
2025年6月10日,浙江大学邵逸夫医院丁国庆/余燕岚/陈艺成/张杰团队在《Cancer Communications》(IF=20.1)期刊上发表了一篇题为“Targeting MAN1B1 potently enhances bladder cancer antitumor immunity via deglycosylation of CD47”的研究文章,本研究通过质谱分析、基因编辑和动物模型实验等技术方法,首次发现糖基转移酶MAN1B1通过调控CD47糖基化促进免疫逃逸,并揭示ERK-HRD1通路对MAN1B1稳定性的调控作用,为膀胱癌免疫治疗提供了新靶点。
青莲百奥为该研究提供了质谱检测及分析服务。

样本信息
临床样本:膀胱癌、肾癌及前列腺癌患者的肿瘤及癌旁组织
细胞系:人膀胱癌细胞(J82、T24、5637)、小鼠膀胱癌细胞(MB49)、HEK293T细胞
动物模型:NSG小鼠(皮下移植J82/T24细胞)
患者来源肿瘤类器官(PTCs):原代膀胱癌组织培养模型
实验技术
基因编辑技术(CRISPR/Cas9)、IP-MS、动物模型实验、分子对接、免疫组化(IHC)、凝集素富集(LCA)糖基化检测
研究亮点
创新机制:首次发现MAN1B1是CD47糖基化的关键酶,其通过增强CD47-SIRPα互作促进免疫逃逸。
靶向治疗突破:DHT I抑制MAN1B1可显著促进巨噬细胞吞噬,且不引起贫血(红细胞缺乏MAN1B1表达)。
调控通路:ERK磷酸化通过抑制E3泛素连接酶HRD1的活性,稳定MAN1B1蛋白水平。
临床转化潜力:患者来源PTCs模型证实DHT I的疗效优于CD47抗体,克服了单抗穿透性差的局限。
研究结果
一、CD47在膀胱癌中的糖基化对其免疫逃逸至关重要
研究发现CD47在膀胱癌中存在两种分子量形式,通过PNGase F处理确认其为糖基化和非糖基化形式,其中糖基化形式在肿瘤组织中更为显著。通过基因敲除CD47,观察到肿瘤负担显著减少,证实了CD47在膀胱癌发展中的关键作用。通过突变分析,确定了CD47的五个N-糖基化位点(N23、N34、N50、N73和N111),这些位点的糖基化对CD47与SIRP-α的结合至关重要。此外,在体外和体内实验中,CD47-5NQ(非糖基化形式)显著减弱了CD47介导的抗吞噬作用,降低了肿瘤生长速度。
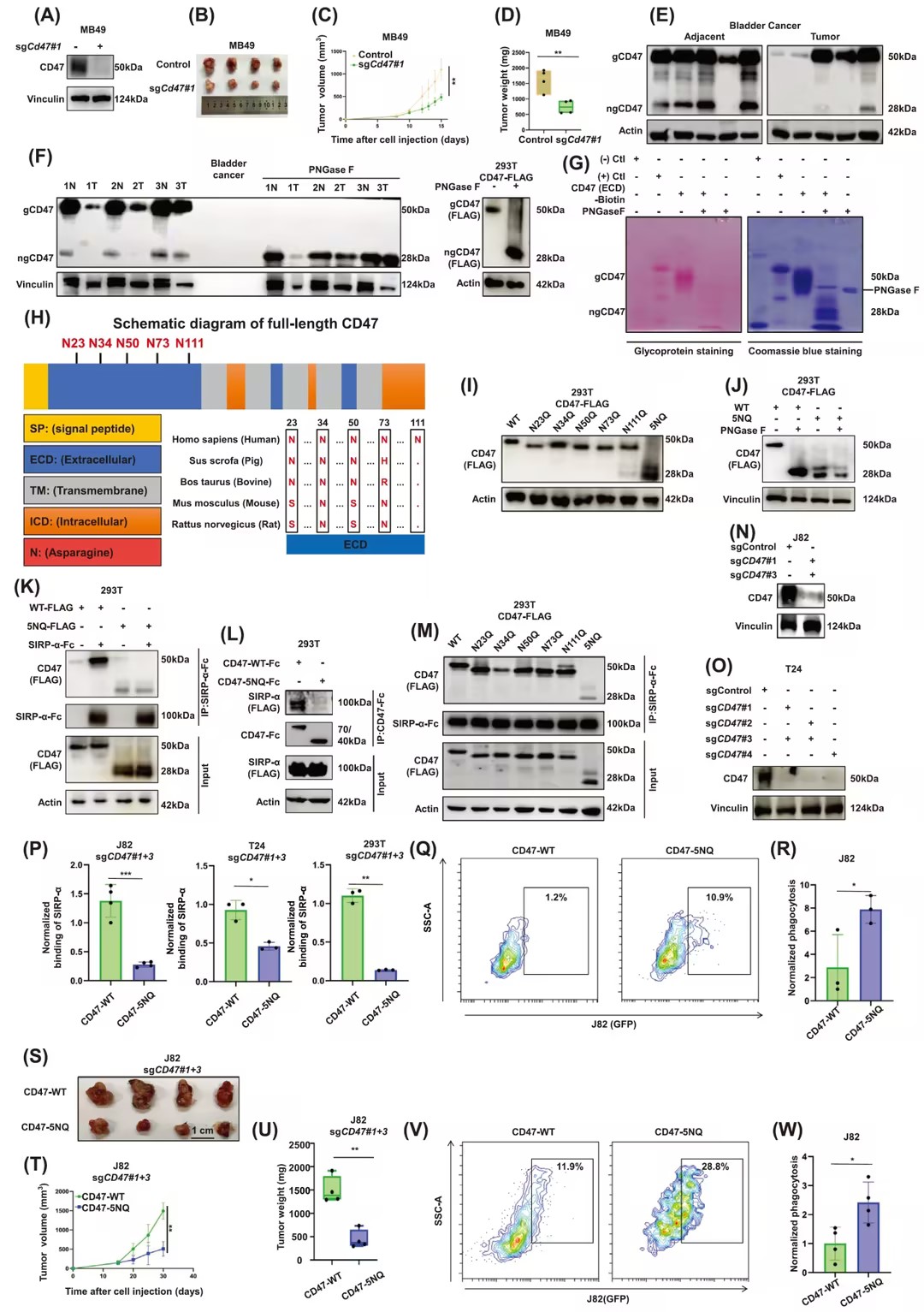
图1 CD47糖基化对于其与SIRP-α的相互作用至关重要
二、MAN1B1参与CD47的糖基化过程,并在膀胱癌中高表达
通过质谱分析和分子对接实验,发现MAN1B1、MOGS、MGAT2和GANAB可能参与CD47的糖基化,其中MAN1B1与CD47的结合最为稳定,表明MAN1B1是CD47的主要糖基转移酶。进一步实验显示,MAN1B1敲除或抑制可以减弱CD47与SIRP-α的结合,从而增强巨噬细胞对肿瘤细胞的吞噬作用。Western blotting和免疫组化结果显示MAN1B1在膀胱癌组织中显著高表达,而CD47的表达水平变化不大。MAN1B1的高表达与膀胱癌患者的不良预后相关。这些发现揭示了MAN1B1作为CD47糖基化修饰酶在膀胱癌免疫逃逸中的关键作用。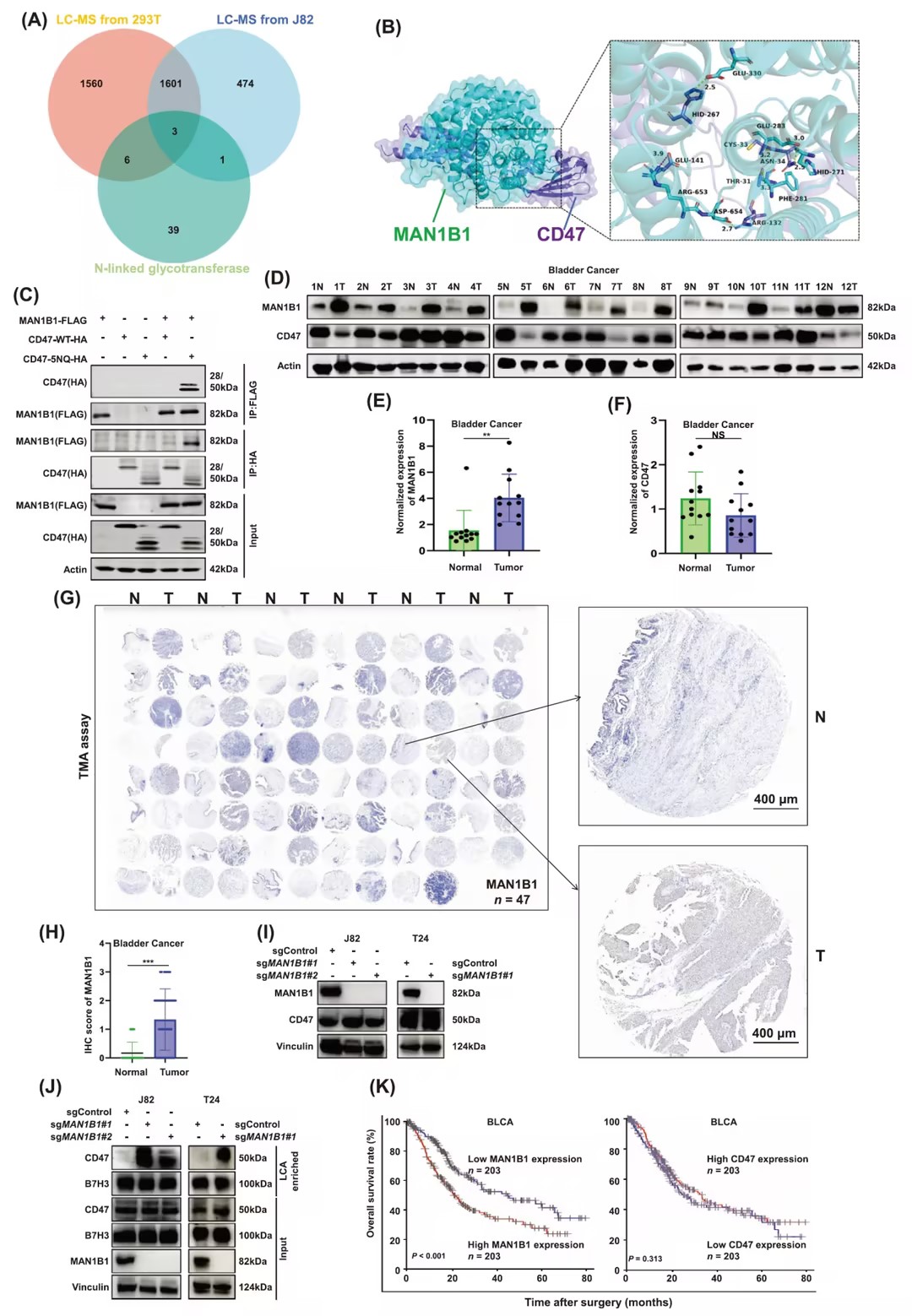 图2 MAN1B1参与CD47的糖基化过程,并在膀胱癌中高表达
图2 MAN1B1参与CD47的糖基化过程,并在膀胱癌中高表达
三、MAN1B1是CD47-SIRP-α轴的关键调节因子
通过免疫共沉淀(IP)实验,发现MAN1B1的减少显著降低了CD47与SIRP-α之间的亲和力,但不影响CD47在细胞膜上的表达。此外,MAN1B1基因敲除抑制了CD47介导的抗吞噬作用,并在体外和体内实验中均显示出一致的效果。在小鼠模型中,MAN1B1基因敲除显著减缓了肿瘤生长,并增加了巨噬细胞对肿瘤细胞的吞噬作用,与对照组相比,肿瘤负担明显减轻。这些发现表明MAN1B1是CD47-SIRP-α轴的关键调节因子,在CD47介导的膀胱癌免疫抑制中发挥了关键作用。
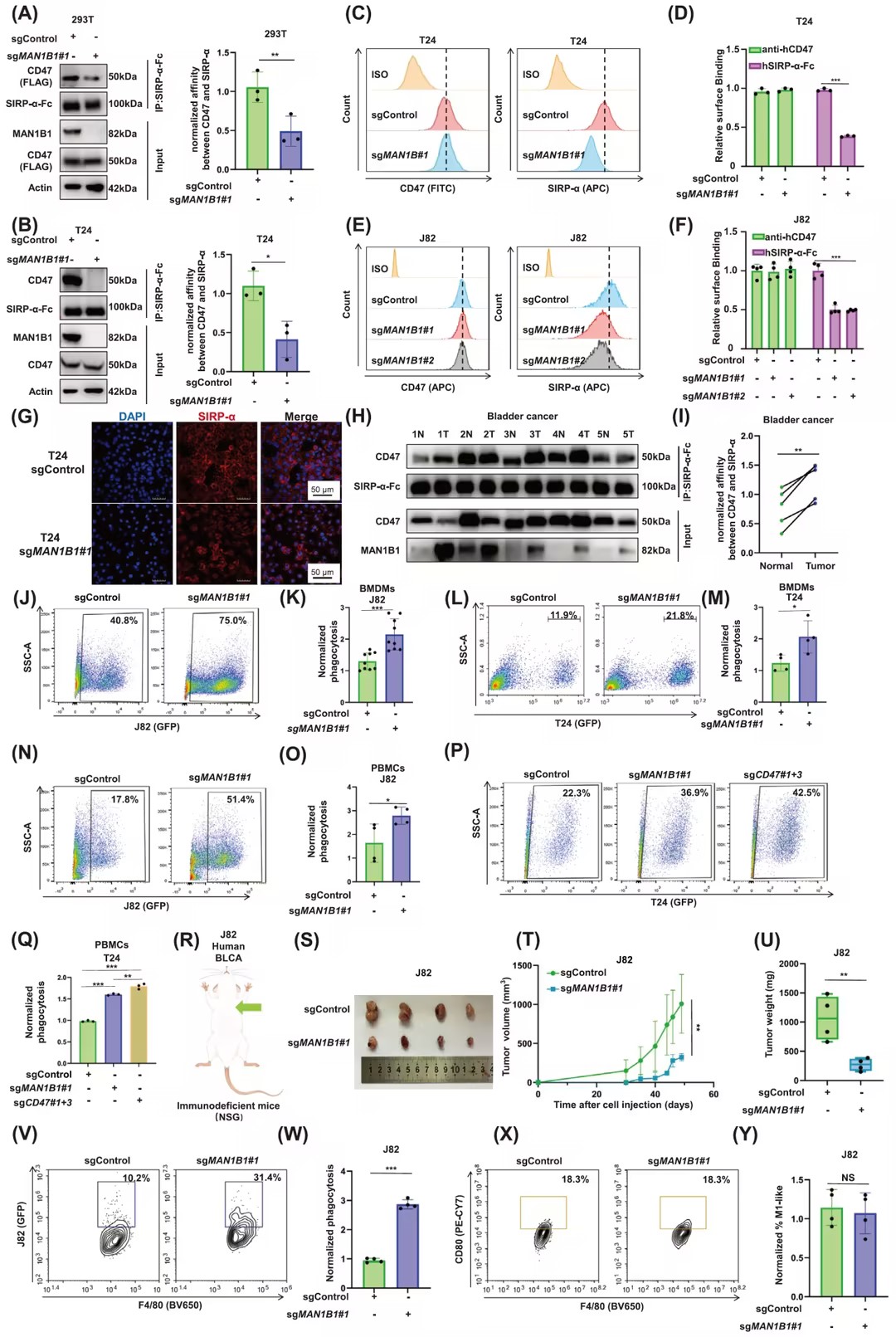 图3 MAN1B1是CD47-SIRP-α轴的关键调节因子
图3 MAN1B1是CD47-SIRP-α轴的关键调节因子
四、靶向MAN1B1抑制剂DHT I通过降低CD47与SIRP-α的亲和力促进巨噬细胞吞噬
通过分子对接实验发现,靶向MAN1B1的抑制剂DHT I能够有效抑制CD47与SIRP-α的结合,并促进巨噬细胞对膀胱癌细胞的吞噬作用。DHT I在非细胞毒性浓度下使用时,能够增加CD47与凝集素的亲和力,但不改变MAN1B1的表达水平。在体内外实验中,DHT I处理显著降低了肿瘤负担,并增加了肿瘤细胞的吞噬率。此外,DHT I在红细胞中的表达水平很低,因此在小鼠模型中未引起贫血等不良反应。这些结果表明,通过DHT I靶向MAN1B1可以显著抑制膀胱癌中的CD47介导的免疫逃逸。
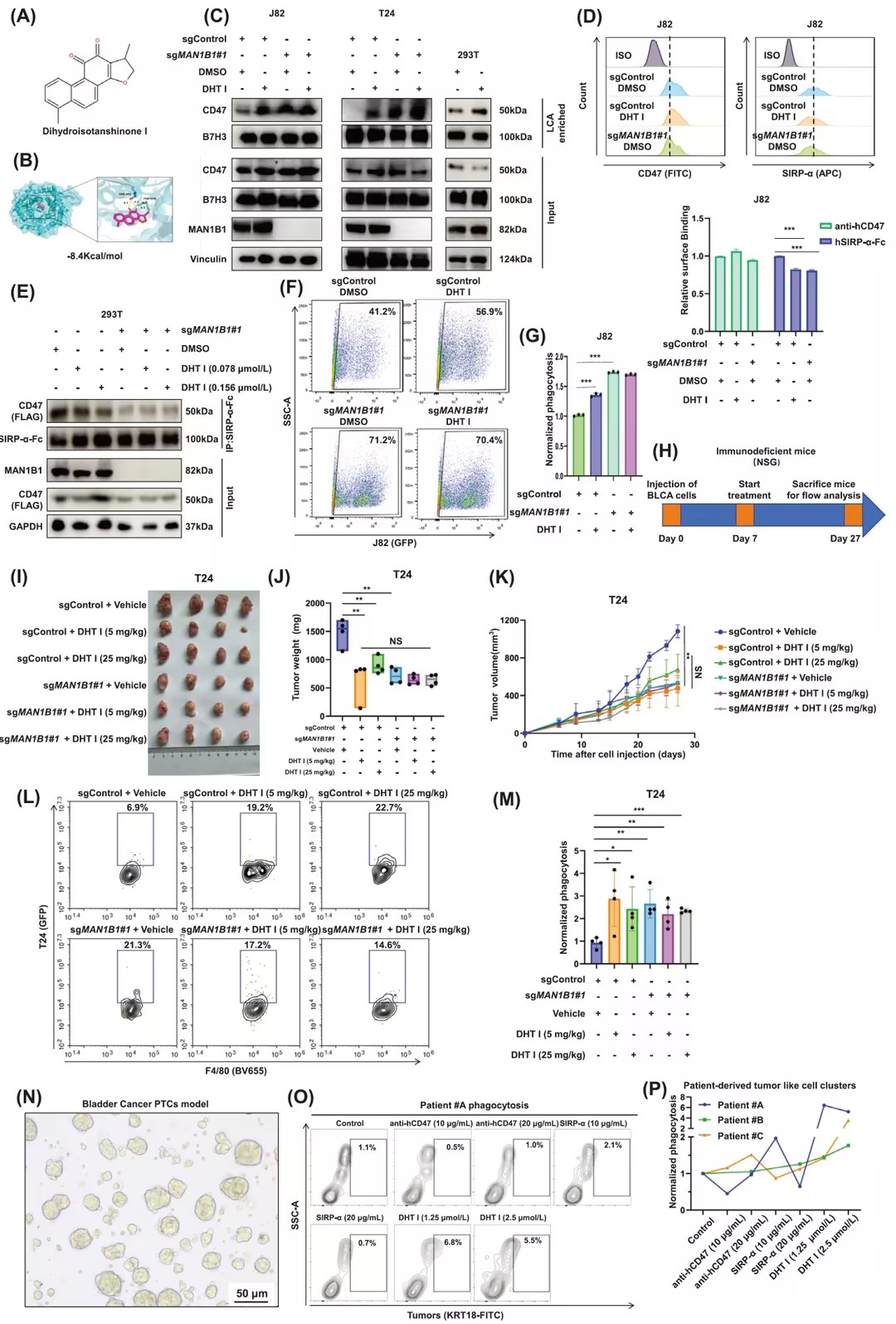 图4 MAN1B1抑制剂DHT I在体外和体内降低CD47与SIRP-α之间的亲和力,促进膀胱癌细胞通过巨噬细胞的吞噬作用
图4 MAN1B1抑制剂DHT I在体外和体内降低CD47与SIRP-α之间的亲和力,促进膀胱癌细胞通过巨噬细胞的吞噬作用
五、靶向MAN1B1的治疗对红细胞无不良影响
在小鼠和人类红细胞中,DHT I处理未引起贫血或红细胞功能障碍。Western blotting和流式细胞术结果显示,红细胞中MAN1B1表达水平极低,DHT I对红细胞CD47与SIRP-α的结合无影响。研究结果表明,DHT I这种MAN1B1抑制剂在小鼠体内没有引起贫血,也没有对小鼠的肝肾功能产生不良影响。
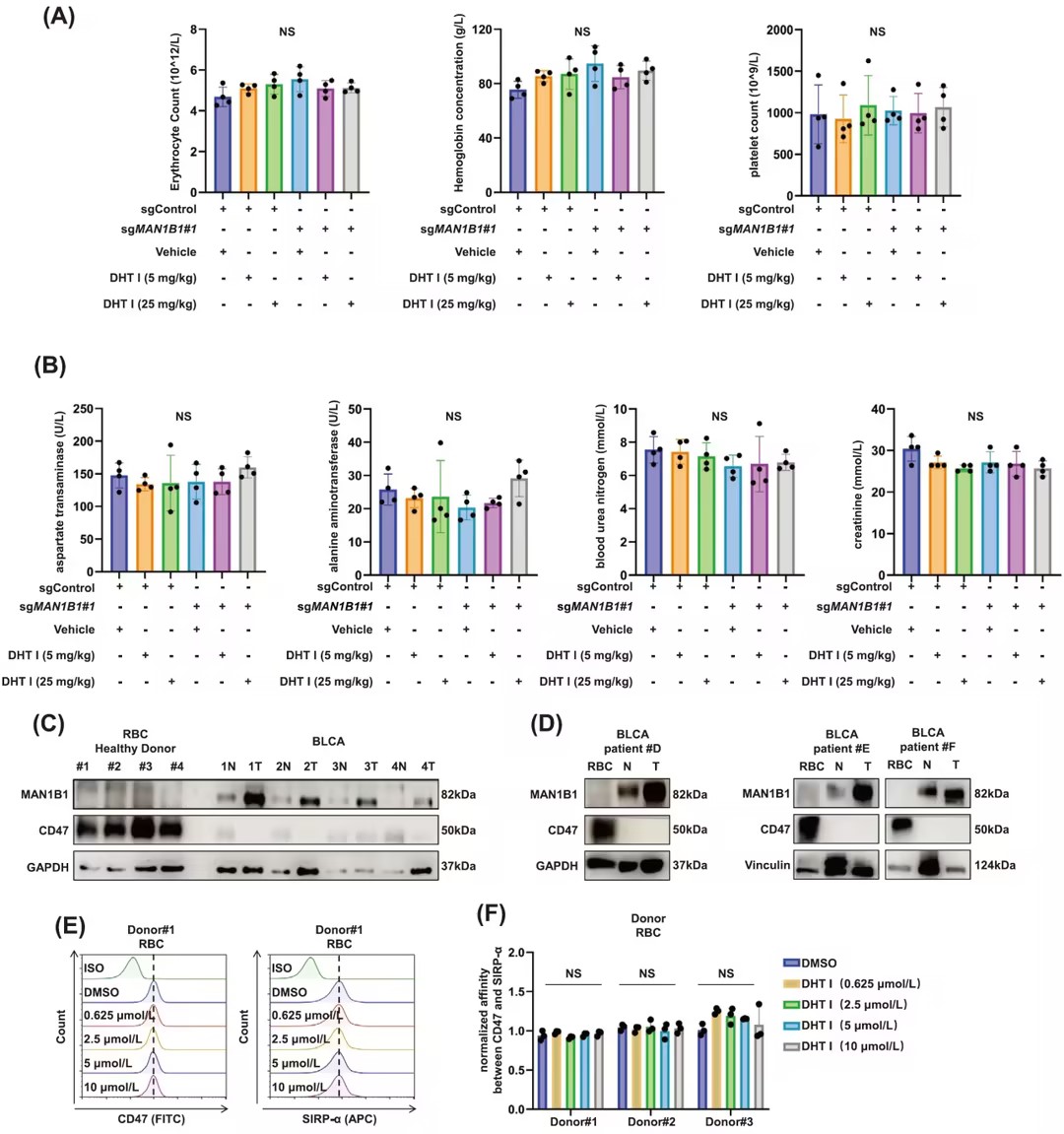 图5靶向MAN1B1的治疗对红细胞无不良影响
图5靶向MAN1B1的治疗对红细胞无不良影响
六、ERK激活通过调节MAN1B1与HRD1的相互作用稳定MAN1B1
研究发现,ERK(细胞外信号调节激酶)的激活通过调节MAN1B1与E3泛素连接酶HRD1(也称为SYVN1)的相互作用来稳定MAN1B1,从而促进了膀胱癌的免疫逃逸。具体来说,ERK的激活降低了MAN1B1与HRD1的亲和力,导致MAN1B1的稳定性增加。此外,HRD1的敲除显著增加了MAN1B1的表达,且这种表达与膀胱癌患者的不良预后相关。这些发现揭示了ERK激活通过影响MAN1B1稳定性的分子机制,为膀胱癌的免疫治疗提供了新的靶点。
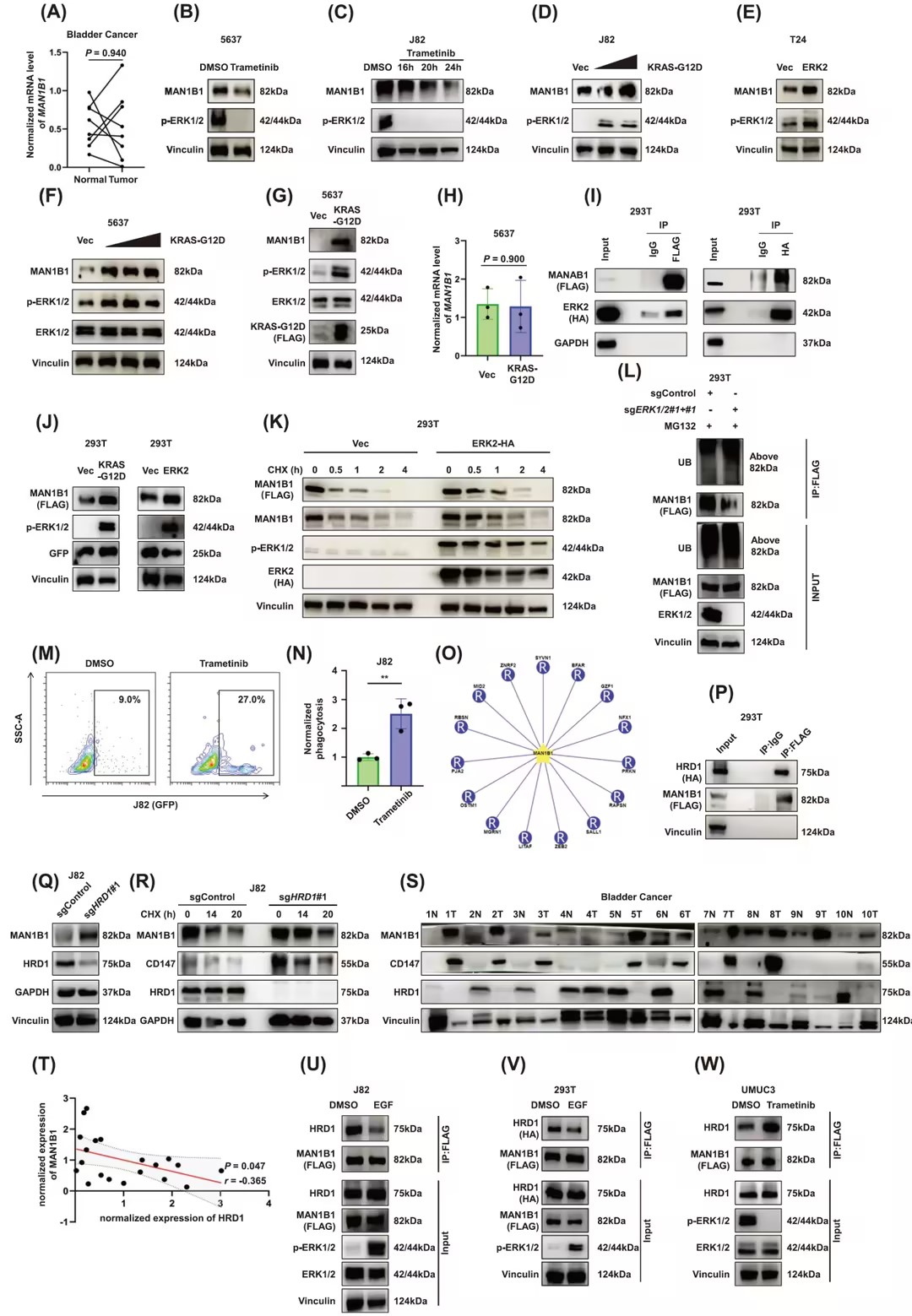 图6 ERK通过调节MAN1B1与膀胱癌中E3连接酶HRD1的相互作用来稳定MAN1B1
图6 ERK通过调节MAN1B1与膀胱癌中E3连接酶HRD1的相互作用来稳定MAN1B1
研究结论
本研究首次阐明MAN1B1通过糖基化CD47促进膀胱癌免疫逃逸的分子机制,并揭示ERK-HRD1通路对MAN1B1稳定性的调控作用。靶向MAN1B1的小分子抑制剂DHT I在体内外均表现出显著抗肿瘤活性,且避免了传统CD47抗体导致的贫血副作用,为膀胱癌免疫治疗提供了全新策略。
该研究不仅揭示了CD47糖基化的临床意义,还提出了联合靶向ERK-MAN1B1-CD47轴的治疗潜力,为克服肿瘤免疫耐药提供了理论依据。
参考文献
[1] Zhang J, Zhang C, Zang R, et al. Targeting MAN1B1 potently enhances bladder cancer antitumor immunity via deglycosylation of CD47. Cancer Commun (Lond)[J]. 2025 Jun 10. doi: 10.1002/cac2.70040.
青莲百奥合作文章
青莲百奥深度参与众多前沿研究,与中国医学科学院、中国科学院、军事医学研究院、国家蛋白质科学中心、四川大学华西医院等顶尖科研机构通力合作,累计发表SCI论文近200篇,累计影响因子(IF)超1500。多项重磅研究成果发表于《Nature》《Science Translational Medicine》《Nature Communications》等国际顶级期刊。
